Clear Sky Science · sv
Kitostan-dextransulfat-nanokapslar för förbättrad tigecyklin‑effekt mot icke‑tyfoida Salmonella enterica
Varför detta spelar roll för livsmedelssäkerhet
De flesta känner till Salmonella som en elak orsak till matförgiftning, ofta kopplad till underkokt fågel. Färre inser att vissa stammar blivit så resistenta mot antibiotika att även kraftfulla ”sista‑utvägs”läkemedel kan svikta. Denna studie undersöker en nanoteknikbaserad metod för att rädda ett sådant läkemedel, tigecyklin, genom att paketera det inne i små sockerbaserade kapslar som hjälper det att smyga in i infekterade celler och stänga av centrala resistensmekanismer i Salmonella.
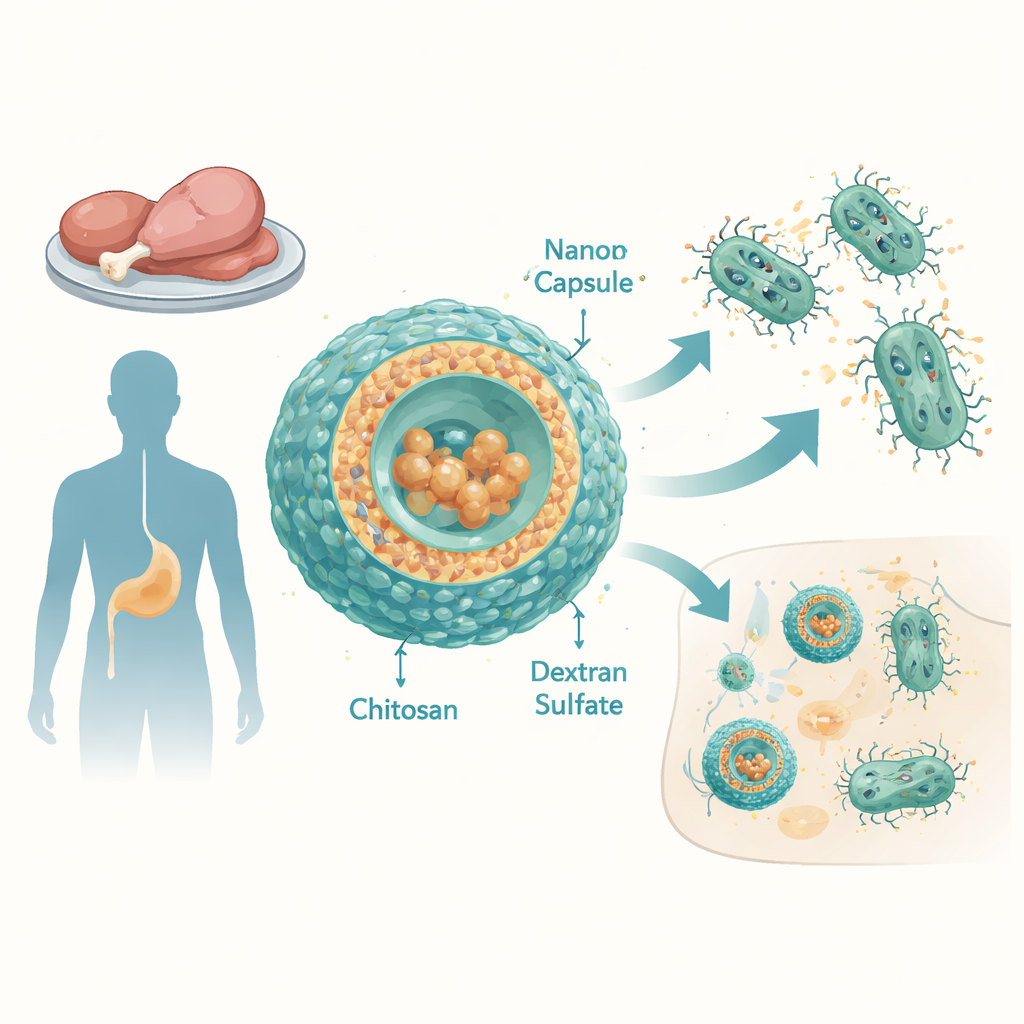
Det växande hotet från svårbekämpad Salmonella
Icke‑tyfoida Salmonella (NTS) serovarianter är en ledande orsak till diarré och blodförgiftningsliknande infektioner världen över, särskilt i låg‑ och medelinkomstländer. Forskarna undersökte 12 Salmonella enterica‑stammar tagna från kyckling‑ och ank‑kött i Egypten. Dessa stammar var resistenta mot många vanliga antibiotika, inklusive penicilliner, cefalosporiner, tetracykliner och andra, och visade höga poäng för mångdagsresistens. Även tigecyklin, ett bredspektrumläkemedel reserverat för svåra fall, fungerade dåligt: bakterierna tolererade mycket höga koncentrationer. En huvudorsak var överaktiva ”effluxpumpar” — molekylära maskiner i bakteriemembranet som ständigt pumpar ut antibiotika ur cellen.
Att bygga en smartare läkemedelskapsel
För att övervinna detta konstruerade teamet nanoskaliga kapslar gjorda av två naturhärledda polymerer: kitostan, framställt från kitin (materialet i skalfiskens skal), och dextransulfat, en förgrenad sockerstruktur. Genom att noggrant stämma av proportionerna av dessa komponenter framställdes stabila partiklar på ungefär 100–150 nanometer med en positiv ytladdning som hjälper dem att interagera med bakterie‑ och värdcellsmembran. Tigecyklin lastades i dessa partiklar med anmärkningsvärt hög effektivitet — i praktiken hamnade nästan allt läkemedel inne i kapslarna. I labbtester som efterliknade förhållanden i blodbanan frigjorde kapslarna större delen av sitt tigecyklin inom några timmar, vilket tyder på att de kan leverera ett kraftfullt utbrott av antibiotikum vid infektionsställen.
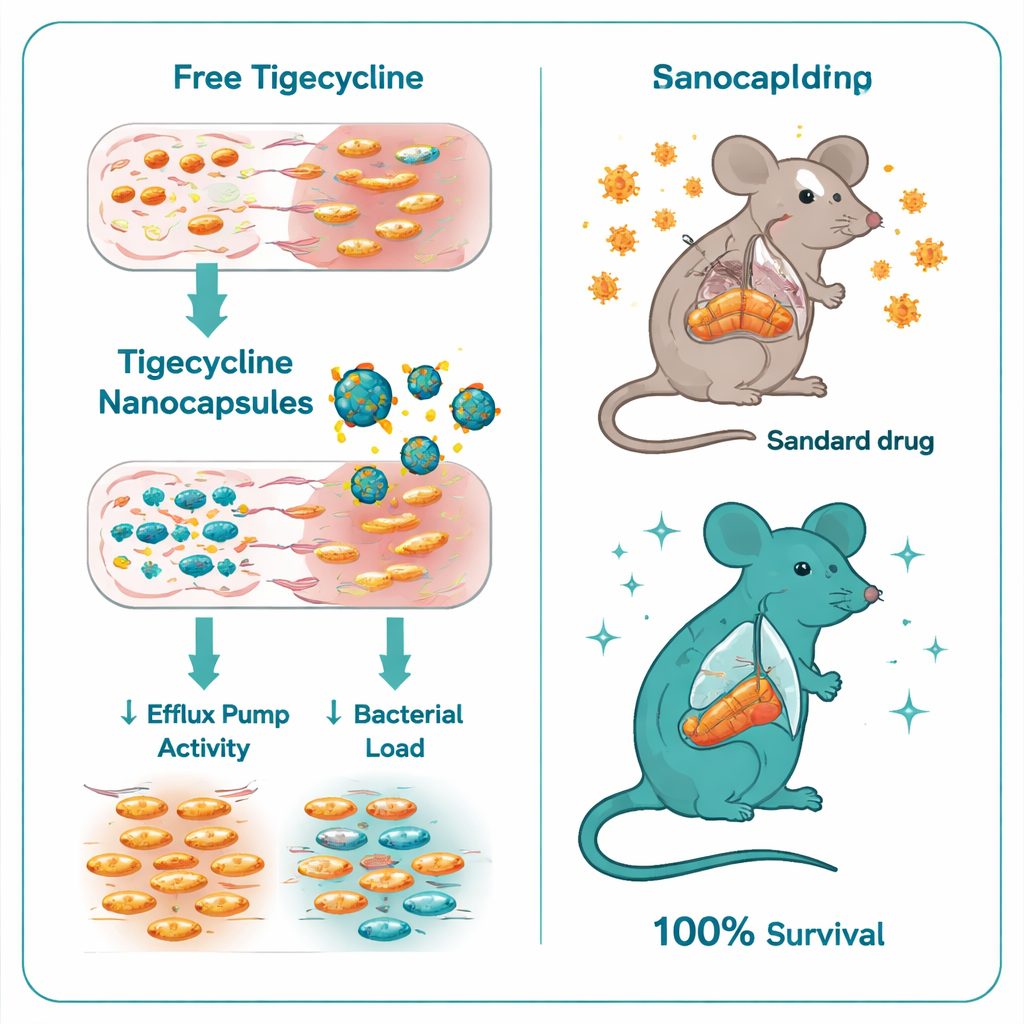
Nedreglering av bakteriella försvar
När forskarna jämförde rent tigecyklin med tigecyklin laddat i kitostan–dextransulfat‑nanokapslar var skillnaden slående. Den minsta läkemedelskoncentration som krävdes för att stoppa bakterietillväxt sjönk från 32–128 mikrogram per milliliter för rent tigecyklin till endast 0,5–1 mikrogram per milliliter med nanokapslarna — en sex‑ till sju‑faldig förbättring. Time‑kill‑experiment visade att den inkapslade formen dödade Salmonella mycket snabbare och grundligare. På genetisk nivå dämpade nanokapslarna också viktiga resistensregulatorer: uttrycket av generna ramA och acrB, som hjälper till att kontrollera och bilda stora effluxpumpar, föll flera gånger i behandlade bakterier. Med andra ord levererade kapslarna inte bara mer läkemedel; de hjälpte till att stänga av en av bakteriernas huvudflyktvägar.
Skydd av infekterade möss från dödlig sjukdom
Teamet testade sedan den nya formuleringen i en musmodell för svår Salmonella Typhimurium‑infektion. Obehandlade infekterade möss dog alla inom åtta dagar. Möss som fick standardtigecyklin klarade sig bättre men hade fortfarande hög dödlighet, med endast 40 % överlevnad. I skarp kontrast överlevde varje mus som behandlades med tigecyklin‑laddade nanokapslar. Dessa djur hade avsevärt färre bakterier i lever och tarmar, blodvärden som låg närmare normal lever‑ och njurfunktion, och mycket lindrigare vävnadsskador vid mikroskopisk undersökning. Även de ”tomma” kitostan–dextransulfat‑kapslarna utan antibiotikum gav visst skydd, sannolikt eftersom kitostan i sig har måttliga antimikrobiella och antiinflammatoriska effekter, men kombinationen med tigecyklin var klart överlägsen.
Vad detta kan betyda för framtida behandlingar
För icke‑specialister är huvudbudskapet att inneslutning av ett befintligt antibiotikum i en smart, biokompatibel nanokapsel kan återställa dess effekt mot högresistent Salmonella. Genom att hjälpa läkemedlet nå bakterier som gömmer sig inne i celler och genom att dämpa pumparna som normalt spottar ut läkemedlet, förvandlade kitostan–dextransulfat‑systemet ett kämpande sista‑utvägsantibiotikum till en mycket effektiv behandling hos möss, med 100 % överlevnad. Även om mer arbete krävs innan denna metod kan användas på människor eller i lantbruksdjur, erbjuder den en lovande väg för att förlänga livslängden för viktiga antibiotika och förbättra vår livsmedelssäkerhet utan att behöva uppfinna helt nya läkemedel från grunden.
Citering: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Nyckelord: Salmonella, antibiotikaresistens, nanopartiklar, läkemedelsleverans, tigecyklin