Clear Sky Science · sv
Integrerad proteomik och metabolomik visar att fytosesquiterpenlactoner hämmar TNBC-cellaktivitet genom att tömma ATP-syntes och omprogrammera primärmetabolism
Växtföreningar som svälter ut aggressiv bröstcancer
Trippelnegativ bröstcancer är en av de svåraste formerna att behandla eftersom den saknar de vanliga hormonella ”handtagen” som många läkemedel riktar sig mot. I den här studien undersöks två molekyler utvunna ur en medicinsk växt som verkar stänga ner dessa cancercellers inre kraftverk, och därigenom avskära deras energiförsörjning samtidigt som normala bröstceller i högre grad skonas. Att förstå hur detta fungerar kan öppna dörren för mildare, mer riktade behandlingar för patienter som idag har begränsade alternativ.
Varför det spelar roll att rikta in sig på cancercellers energikälla
Varje cell är beroende av små strukturer kallade mitokondrier för att producera ATP, cellens grundläggande bränsle. Cancerceller, särskilt de aggressiva, är ofta ovanligt beroende av sina mitokondrier för att stödja snabb tillväxt, spridning och överlevnad under stress. Forskarna fokuserade på trippelnegativa bröstcancerceller, som står för cirka 15–20 % av bröstcancerfallen och tenderar att återkomma och metastasera oftare än andra typer. De studerade en naturlig molekyl, deoxyelefantopin (DET), och dess förfinade kusin DETD-35, båda sesquiterpenlactoner från den medicinska växten Elephantopus. Tidigare arbete visade att dessa föreningar utlöser oxidativ stress och ovanliga former av celldöd i cancerceller, men hur de stör cellernas energifabriker var inte väl kartlagt.
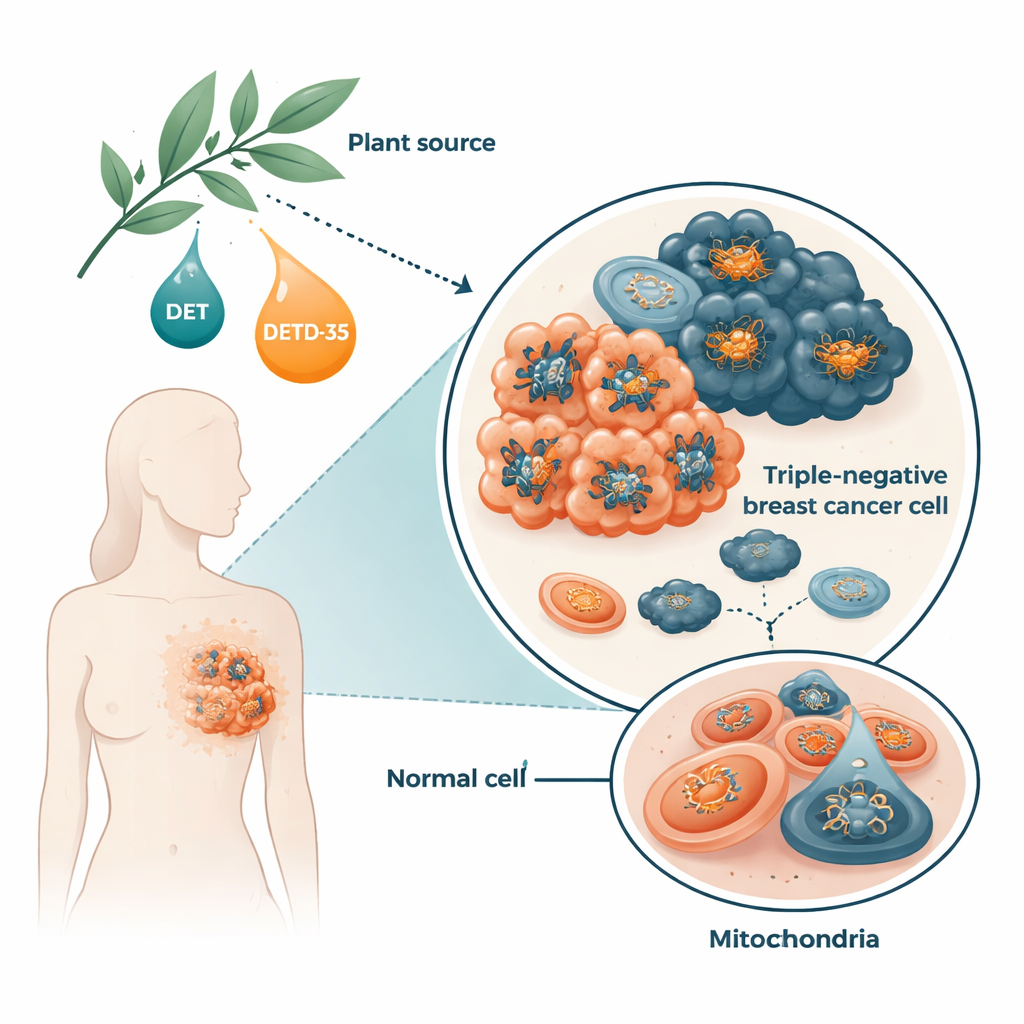
Hur växtmolekylerna stör cancercellernas mitokondrier
Med mänskliga trippelnegativa bröstcancerceller odlade i laboratorium fann teamet att DET och DETD-35 snabbt ökade produktionen av reaktiva syrearter, en typ av kemiskt reaktivt ”avgaser” som bildas under energiproduktionen. Som svar ökade cellerna vissa skyddande enzymer, men inte tillräckligt för att återställa balansen. Föreningarna tvingade också öppning av en kanal i mitokondriemembranet som kallas permeabilitetstransitionsporen, en förändring kopplad till svällning, förlust av membranpotential och de tidiga stegen i celldöd. Redan inom några timmar sjönk ATP-nivåerna inne i cancercellerna kraftigt. När forskarna tillsatte en antioxidant i förväg återställdes dessa skadliga effekter till stor del, vilket visar att oxidativ stress var en nyckelkomponent i processen.
Kartläggning av skadorna på proteiner och metabolism
För att förstå helhetsbilden kombinerade forskarna två kraftfulla ”omiks”-metoder. De katalogiserade tusentals mitokondriella proteiner och mätte många små metaboliter i behandlade jämfört med obehandlade celler. Denna integrerade vy visade att DET och DETD-35 störde proteiner som är involverade i oxidativ fosforylering, den huvudsakliga väg mitokondrier använder för att tillverka ATP, och aktiverade dödsrelaterad signalering. Samtidigt omprogrammerades centrala metaboliska vägar som hanterar aminosyror, fetter och byggstenar för DNA. Vissa lipider som hjälper till att forma det inre mitokondriemembranet, liksom molekyler kopplade till antioxidantförsvar och glukosnedbrytning, förändrades på sätt förenliga med stressade, energibristande cancerceller. Avgörande var att dessa utbredda förändringar inte sågs i normala bröstceller exponerade för samma doser, vilket tyder på en viss selektivitet för tumörceller.
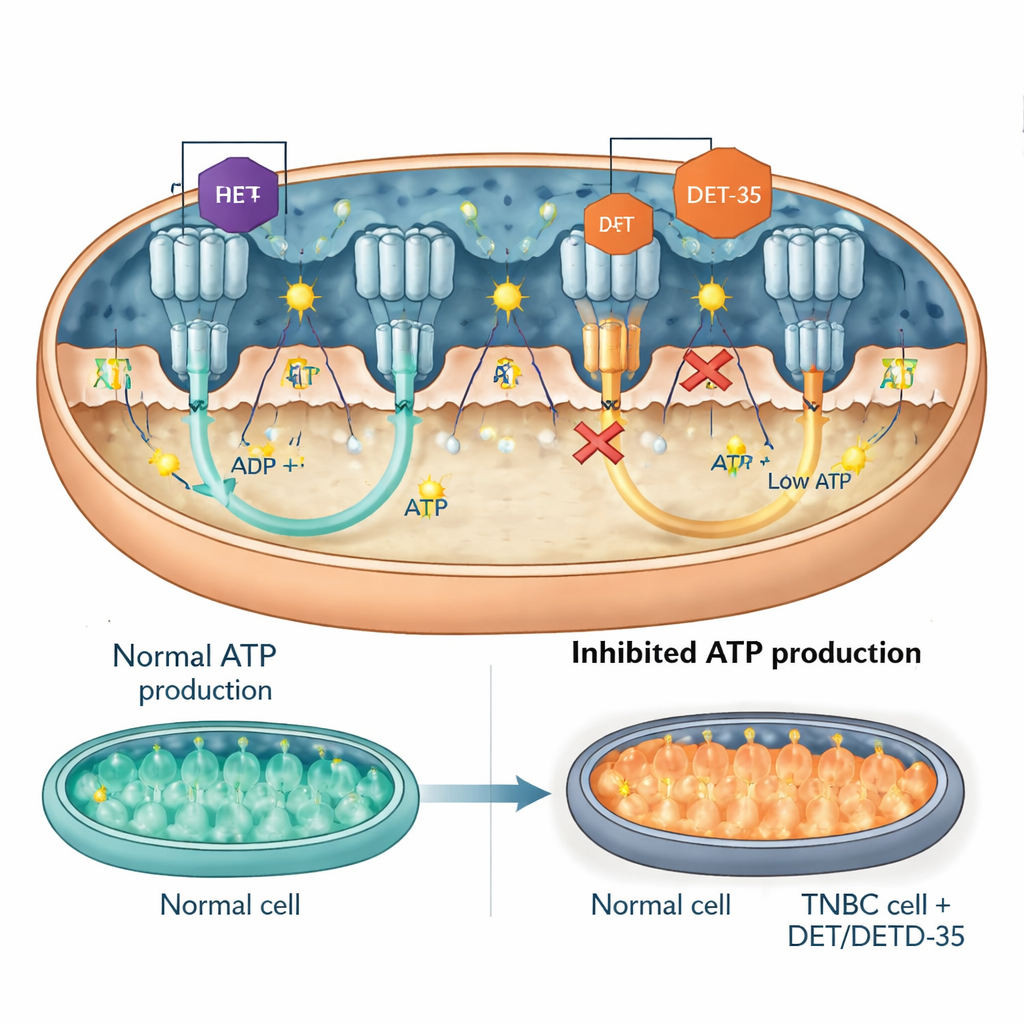
Ett nyckelprotein i signalering och ATP-turbinen själv
Teamet fokuserade sedan in på specifika aktörer inom dessa störda nätverk. En var PRKCA, ett signalprotein som kan förflytta sig in i mitokondrier och påverka både energiproduktion och stresssvar. DET och DETD-35 ökade PRKCA-nivåerna i cancercellerna. När forskarna genetiskt sänkte PRKCA blev läkemedlen mindre giftiga: cancercellerna hade större chans att överleva, producerade mer ATP och visade färre tecken på mitokondriedysfunktion och apoptos. Ett annat fokus var ATP-syntas, det molekylära ”turbinen” som snurrar för att skapa ATP. Mätningar visade att DET och DETD-35 direkt minskade ATP-syntasaktiviteten i cancercellernas mitokondrier. Datorbaserade dockningsmodeller antydde att båda föreningarna fastnar vid kritiska gränssnitt på enzymet, samma allmänna områden där kända ATP-syntas-hämmande läkemedel binder, vilket fysiskt hindrar dess rörelse och sänker ATP-produktionen. I möss med mänskliga trippelnegativa brösttumörer minskade behandling med någon av föreningarna nivåerna av ATP-syntas-komponenter i tumörvävnaden, vilket stöder fynden från cellkulturerna.
Vad detta kan innebära för framtida cancerbehandlingar
Sammantaget målar studien upp en sammanhängande bild: dessa växtbaserade föreningar pressar trippelnegativa bröstcancerceller in i en energikris genom att överbelasta dem med oxidativ stress, prångla upp mitokondriella porer och direkt blockera ATP-tillverkande maskineri. När ATP tar slut och metabolismen rörs om förlorar cancercellerna förmågan att växa och överleva, medan normala bröstceller förblir i högre grad opåverkade under samma förhållanden. För en lekmannaläsare innebär detta att forskare kan utnyttja cancercellers starka beroende av sina interna kraftstationer och använda noggrant designade molekyler — vissa inspirerade av växter — för att tömma tumörcellernas batterier utan att slå av strömmen för frisk vävnad. Mer arbete krävs innan sådana ämnen kan nå kliniken, men denna integrerade bild av proteiner, metaboliter och energiflöde erbjuder en lovande färdplan.
Citering: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Nyckelord: trippelnegativ bröstcancer, mitokondrier, ATP-syntas, naturprodukter, cancermetabolism