Clear Sky Science · sv
Bakterier från mat och tarmmikrobiota producerar methylglyoxal och denna metabolit leder till bildning av bioaktiva 1‑acetyl‑β‑carbolin‑alkaloider
Varför tarmens kemilaboratorium spelar roll
Inuti våra tarmar och i många fermenterade livsmedel omvandlar biljoner bakterier ständigt de sockerarter vi äter till en mängd kemiska biprodukter. Denna studie undersöker en sådan väg i detalj: hur vissa vanliga bakterier omvandlar socker till en mycket reaktiv förening kallad methylglyoxal, och därefter till en familj bioaktiva molekyler kallade 1‑acetyl‑β‑carboliner. Eftersom dessa ämnen både kopplats till sjukdomsprocesser och till potentiella nya läkemedel kan förståelsen av när och hur bakterier tillverkar dem förändra hur vi ser på mat, mikrobiomet och hälsa.
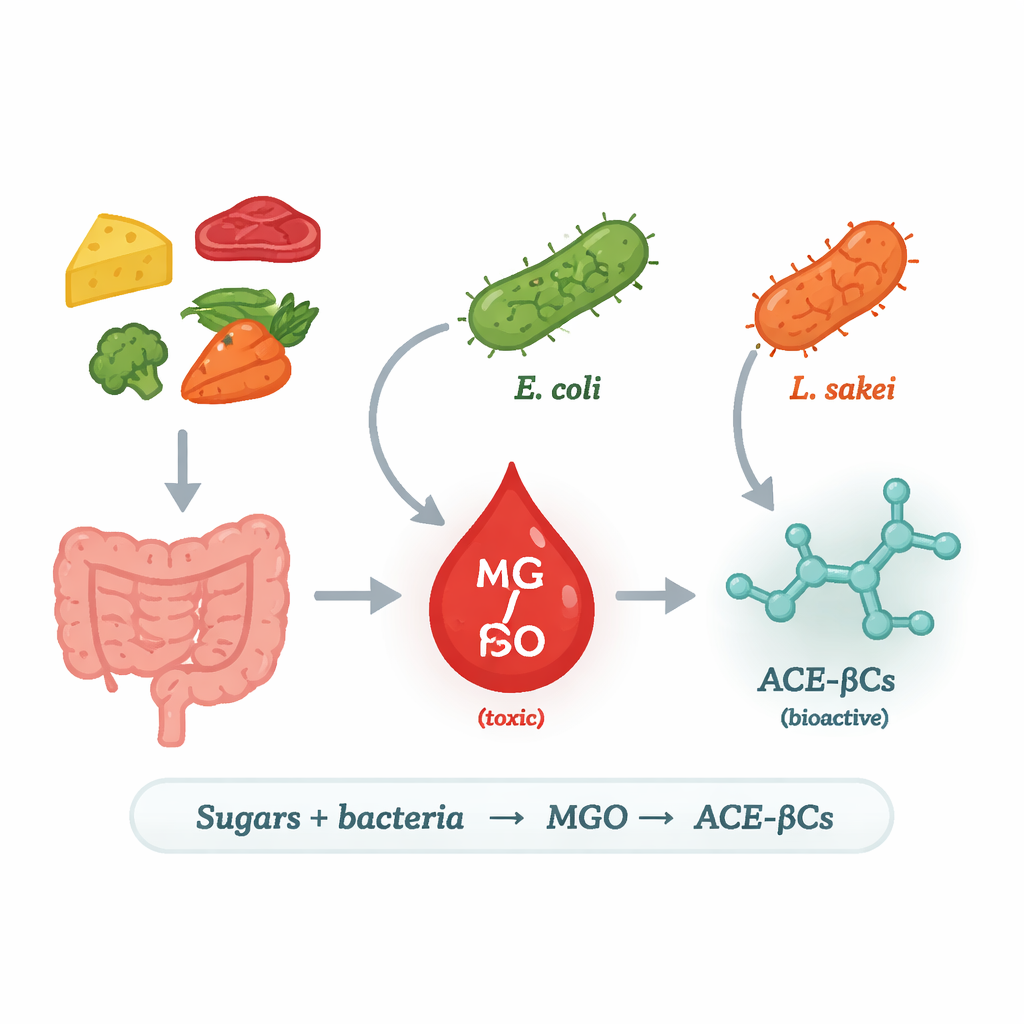
Från vardagliga sockerarter till en riskabel molekyl
Forskningen fokuserade på methylglyoxal (MGO), en mycket reaktiv, toxisk biprodukt av sockernedbrytning. Hos människor är förhöjda MGO‑nivåer associerade med diabetes, hjärtsjukdom och neurodegeneration eftersom det kan skada proteiner och DNA. Våra celler håller normalt MGO i schack med avgiftningssystem, men de är inte den enda källan: bakterier kan också producera MGO. I vissa mikrober omvandlar ett enzym kallat methylglyoxal synthase (MgsA) ett socker‑nedbrytningsintermediat direkt till MGO och skapar därmed en "genväg" i energimetabolismen. Teamet frågade vilka mat‑ och tarmbakterier som använder denna väg, under vilka förhållanden, och vad som händer med det MGO de släpper ut.
Vilka är de bakterieproducenterna?
För att svara på detta odlade forskarna flera stammar av mjölksyrabakterier som ofta finns i livsmedel, tillsammans med en laboratoriestam av Escherichia coli, i ett kontrollerat medium innehållande antingen glukos eller galaktos. De följde sedan MGO och två närbesläktade alkaloider i odlingsvätskan över tid med hjälp av högprecisionskromatografi och massespektrometri. Endast E. coli och den köttassocierade arten Lactilactobacillus sakei producerade påtagliga mängder MGO och alkaloiderna; andra testade mjölksyrabakterier gjorde det inte. En genomsökning visade den avgörande skillnaden: E. coli och L. sakei bär genen för MgsA, medan de flesta av deras mjölksyrarelaterade inte gör det. När forskarna infogade mgsA‑genen från L. sakei i en icke‑producerande stam började den konstruerade bakterien producera både MGO och alkaloiderna, vilket tydligt knöt MgsA till denna väg.
Hur toxisk MGO blir bioaktiva alkaloider
Nästa fråga var vad som händer med MGO när det väl bildats. Teamet fokuserade på 1‑acetyl‑β‑carbolin‑alkaloider (ACE‑βC), små molekyler med rapporterade antimikrobiella, antiinflammatoriska och anticanceraktiviteter. De visade att när MGO‑producerande bakterier odlades i närvaro av aminosyran L‑tryptofan ökade nivåerna av två ACE‑βC—1‑acetyl‑β‑carbolin och dess 3‑karboxylsyraform—markant. Tillsats av extra MGO till mediet ökade också deras bildning. Detta indikerar att MGO läcker ut ur cellerna och reagerar spontant med L‑tryptofan i den omgivande vätskan, utan ytterligare enzymer, för att generera dessa bioaktiva föreningar. Med andra ord: samma kemi som gör MGO farligt omvandlar det också till mer komplexa molekyler som kan ha användbara effekter.
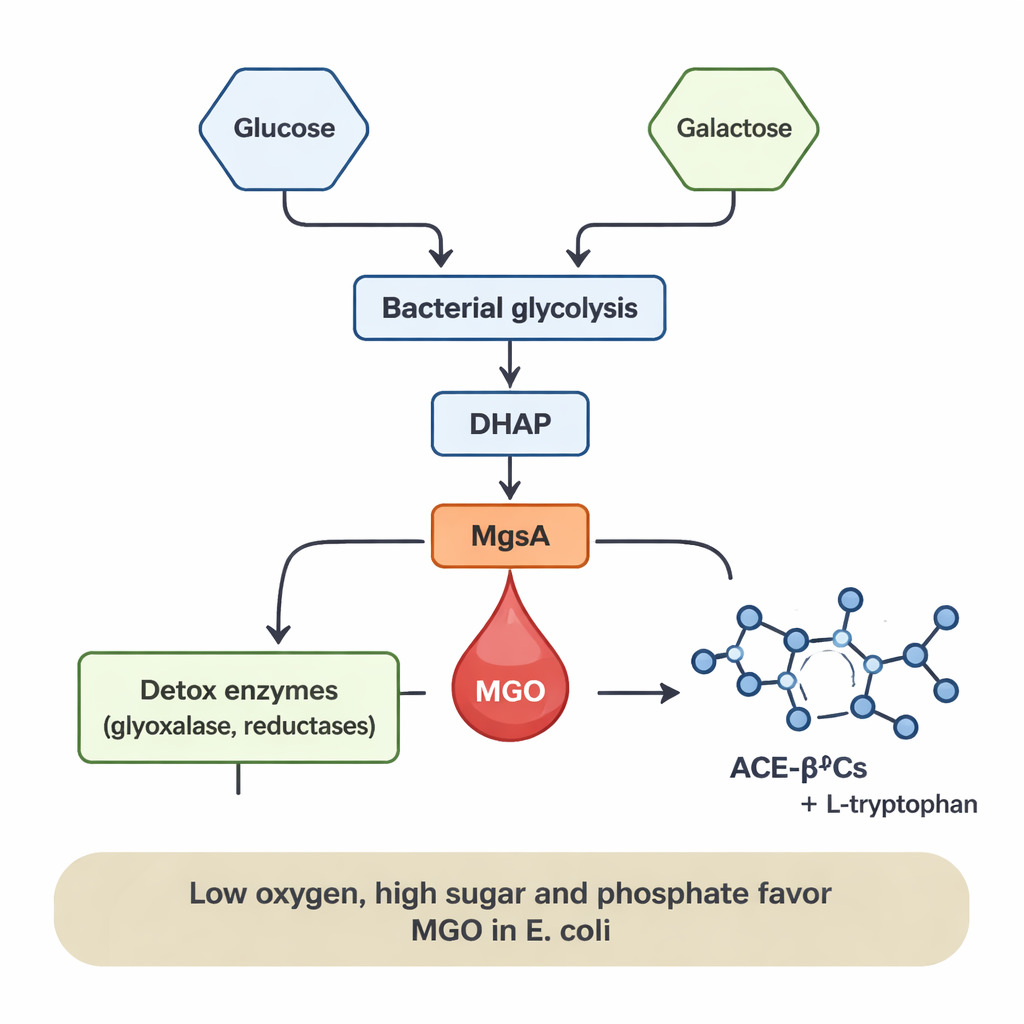
Vad som skruvar upp eller ner produktionen
MGO‑produktionen var inte konstant; den berodde starkt på bakteriernas diet och omgivning. I E. coli framträdde MGO endast när glukos var närvarande, och nivåerna ökade i takt med högre glukoskoncentration. Tillsats av fosfat, ett vanligt mineralnäringsämne, förstärkte ytterligare MGO‑bildningen flera gånger om, sannolikt eftersom det främjar uppbyggnad av fosforylerade sockerintermediater som matar in i MgsA‑genvägen. Låga syreförhållanden (anaeroba)—liknande de i den mänskliga tarmen—gynnade också MGO‑frigörelse, medan hög‑syre, väl‑aeroba förhållanden kraftigt minskade den trots att bakterierna fortfarande växte väl. I kontrast genererade L. sakei främst MGO när den odlades på galaktos, och produktionen ökade med högre galaktoshalt. Dessa mönster tyder på att när sockerflödet genom bakteriell metabolism är högt och syre är begränsat kan MGO fungera som en "tryckventil" som lättar på belastningen av ackumulerande sockerintermediater.
Vad detta kan innebära för mat och hälsa
Resultaten tyder på att inte alla tarm‑ eller matbakterier är lika benägna att bilda MGO och ACE‑βC. Arter som bär enzymet MgsA, såsom vissa L. sakei‑stammar och E. coli, kan vara betydande bidragsgivare, särskilt i socker‑rika, syrefattiga miljöer som tarmen eller vissa fermenteringar. Det MGO de utsöndrar kan öka den kemiska bördan på värdens vävnader, men dess omvandling till ACE‑βC‑alkaloider kan också delvis "ta hand om" denna reaktiva förening samtidigt som det genererar molekyler med egna biologiska effekter. Även om denna studie utfördes i laboratoriekulturer belyser den en plausibel väg där kost, sammansättning av mikrobiotan och bakteriell metabolism tillsammans formar balansen mellan skadliga och potentiellt fördelaktiga kemikalier i våra kroppar, och den pekar på ACE‑βC som möjliga markörer för bakteriell MGO‑produktion i livsmedel och tarmen.
Citering: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Nyckelord: tarmmikrobiota, methylglyoxal, bakteriell metabolism, matfermentering, beta‑carbolin‑alkaloider