Clear Sky Science · sv
Design- och prestandaanalys av en vertikalt staplad gate-all-around nanosheet-FET med inbyggd nanokavitet för biosensorapplikationer
Mindre sensorer för tidigare varningar
Att upptäcka cancer tidigt beror ofta på hur snabbt och exakt vi kan hitta mycket små spår av sjukdom i blod eller andra kroppsvätskor. Denna artikel undersöker en ny typ av ultrasmå elektroniska sensor — byggd med samma teknik som används i avancerade datorchip — som kan detektera cancerrelaterade molekyler med betydligt högre känslighet än många befintliga enheter, samtidigt som den använder mycket lite energi.
Att förvandla en transistor till en canceravkännare
I kärnan av arbetet ligger en omdesignad transistor, den grundläggande brytarelementet i elektronik. Författarna utgår från en toppmodern enhetstyp kallad nanosheet-FET, som redan används av stora chiptillverkare för 3 nm-processorer. De återanvänder den som en biosensor genom att karva ut små ihåliga regioner, eller nanokaviteter, runt den isolerade porten som styr strömflödet. När cancerkopplade biomolekyler — såsom celler från kolorektala eller njurtumörer, DNA-strängar eller gelatinlika proteiner — hamnar i dessa kaviter förändrar de subtilt hur elektrisk laddning rör sig i enheten. Transistorn ”känner” denna förändring som en förskjutning i strömmen och omvandlar en biokemisk händelse till en elektrisk signal som kan mätas.
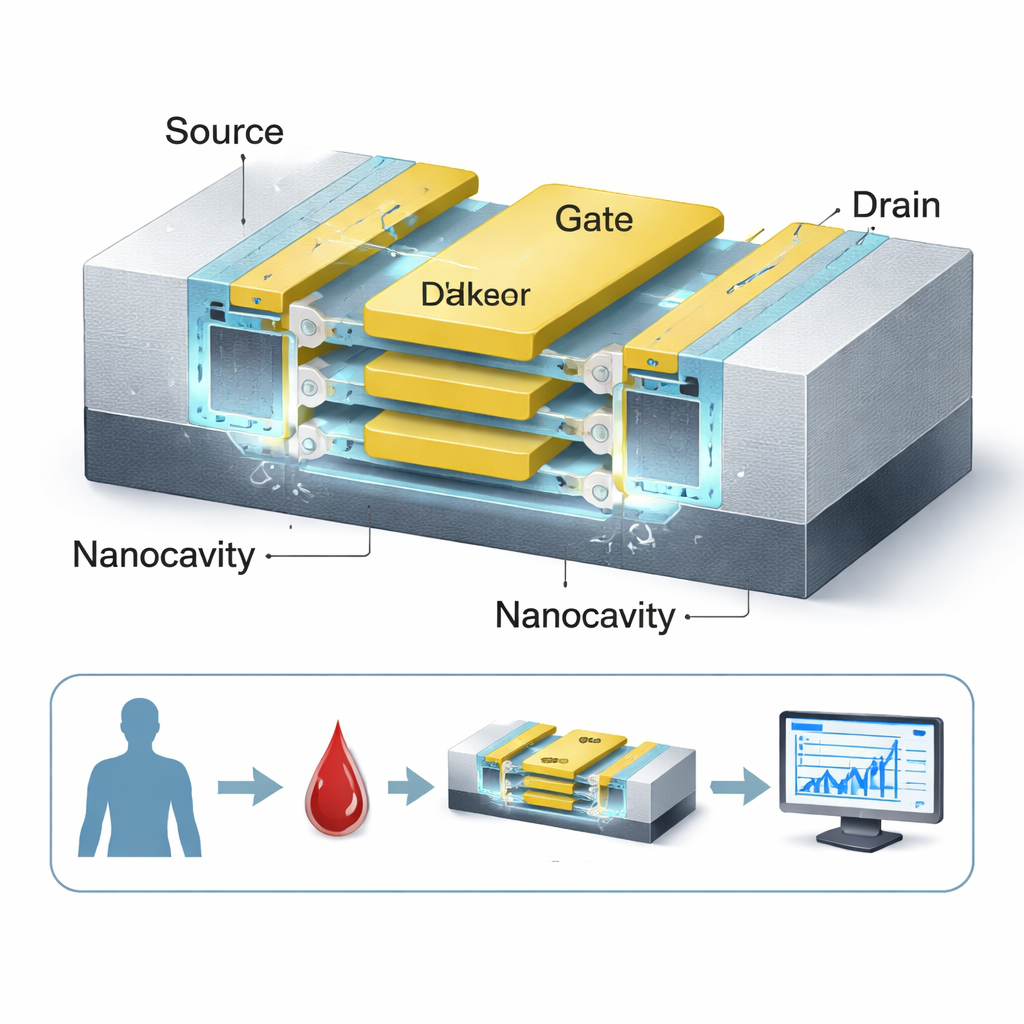
Stapling av lager för starkare signaler
En viktig vändning i designen är att sensorkanalen inte är en enda ledare utan tre ultratunna kiselark staplade vertikalt, alla omslutna av en gemensam port. Denna gate-all-around-struktur ger porten mycket tajtare kontroll över kanalen än i traditionella platta transistorer, vilket skärper enhetens av- och på-styrning och förstärker den mätbara förändringen när biomolekyler finns närvarande. Två nanokaviteter är placerade på vardera sidan om ett hög-k isolerande lager (HfO₂), vilket maximerar det område där molekyler kan interagera med det elektriska fältet. Eftersom kanalen är ”dopingfri”, det vill säga undviker tunga kemiska föroreningar, blir sensorernas respons mer enhetlig och mindre känslig för variationsfel i tillverkningen — en fördel för pålitlig medicinsk testning.
Finjustering av små kaviter för maximal respons
Genom detaljerade datorsimuleringar (TCAD) justerar forskarna systematiskt kaviteternas geometri: deras längd, tjocklek och hur fullt de är fyllda med molekyler. Kortare och tunnare kaviter för dem porten och kanalen i närmare elektrostatisk kontakt, vilket höjer on-strömmen och minskar så kallad subthreshold swing — ett mått på hur brant enheten slår på. I deras optimala design når sensorn en anmärkningsvärt låg swing på cirka 28 millivolt per dekad, långt under 60 mV/dec-gränsen för standardtransistorer. Det innebär att enheten reagerar kraftigt på mycket små spänningsförändringar, en avgörande egenskap för att upptäcka låga koncentrationer av biomolekyler. De visar också att när en större del av kavitetens volym upptas — eller när molekylerna sitter närmare den punkt där strömmen börjar — blir signalen starkare, vilket klargör hur trängsel och placering av mål påverkar prestandan.
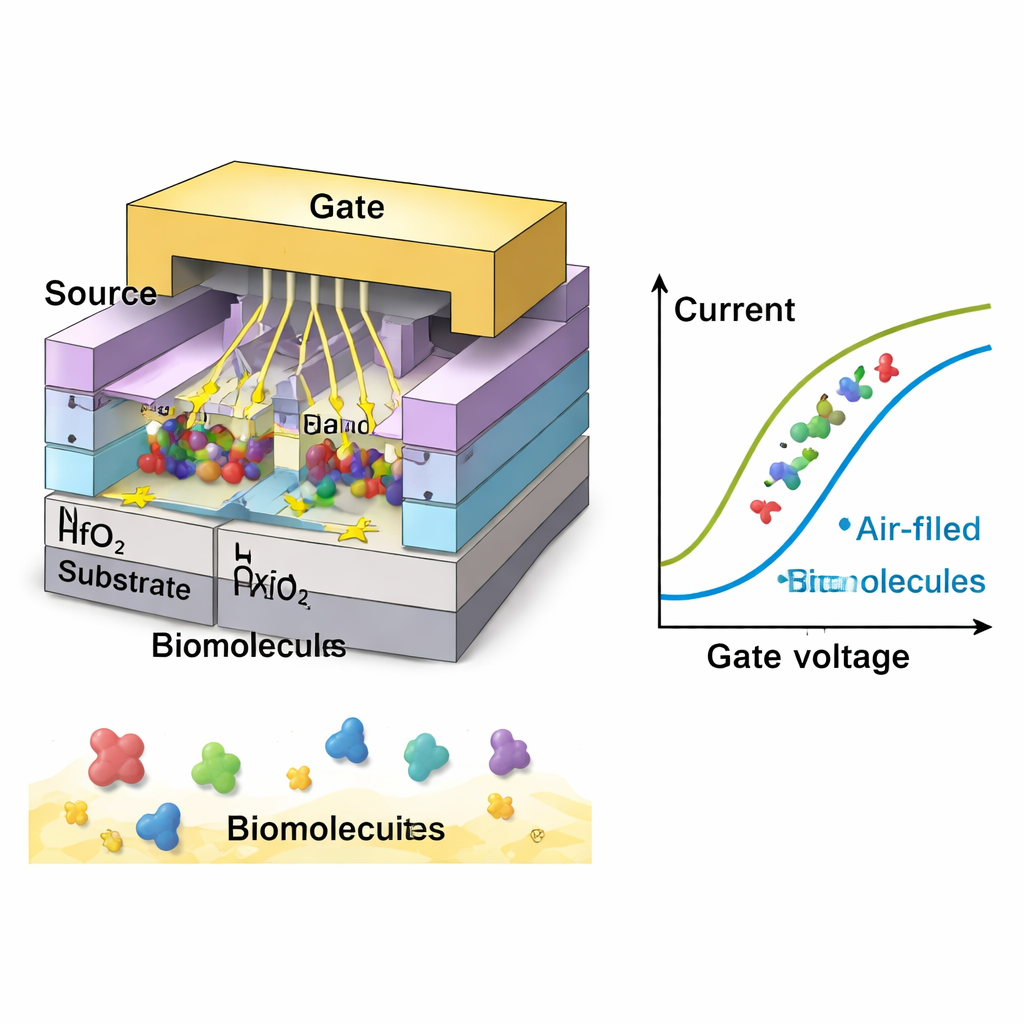
Läsa cancerledtrådar i elektriska signaler
Teamet undersöker sedan hur olika typer av biomolekyler skulle te sig elektriskt. Neutrala arter med högre inneboende permittivitet (en elektrisk egenskap relaterad till hur de polariseras i ett fält) ger större strömförändringar och bättre känslighet, med starkast respons vid ett värde typiskt för gelatin och vissa täta biologiska vävnader. Laddade molekyler, såsom DNA eller vissa cellytor, kan förstärka signalen ännu mer. I simuleringarna ger negativt laddade biomolekyler den största strömskiftningen, följt av positiva laddningar och därefter neutrala. Under optimala förhållanden uppnår enheten en strömkänslighet mer än 3 000 gånger högre än grundnivån och över 9 000 för starkt negativt laddade arter — vilket överträffar flera tidigare nanosheet-baserade biosensorer. Sensorn visar också snabba responstider, stabil drift nära rumstemperatur och god specificitet, vilket betyder att den kan skilja målmolekyler från liknande men oönskade ämnen.
Mot praktiska cancerprov på chipnivå
För att säkerställa att konceptet är realistiskt beskriver författarna ett tillverkningsflöde som i hög grad följer dagens avancerade chipframställning, med användning av standard silicon-on-insulator-wafers, välkända oxid- och metallager samt vanliga etssteget för att forma nanokaviterna. Eftersom strukturen förblir kompakt och kompatibel med mainstream CMOS-processer kan den i princip integreras i täta matriser på en enda bricka. För en icke-expert är slutsatsen att detta arbete för transistorbaserade biosensorer närmare praktiska lab-on-a-chip-enheter som en dag kan screena för cancermarkörer snabbt, med hög känslighet och utan behov av märkning eller komplex kemi, med teknik som liknar den som redan driver modern elektronik.
Citering: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Nyckelord: cancercellsensor, nanosheet-FET, lab-on-a-chip, nanokavitetsensor, tidig upptäckt