Clear Sky Science · sv
Laktat reglerar YTHDF2–FTH1-axeln för att främja kardiomyocyt-ferroptos och förvärra hjärtats ischemi–reperfusionsskada
Varför hjärtpatienter bör bry sig om denna kemi
När läkare öppnar en blockerad kranskärl efter en hjärtinfarkt räddar det strömmande friska blodet muskel, men kan också orsaka ytterligare skada, känd som ischemi–reperfusionsskada. Denna studie avslöjar en oväntad bov inne i hjärcellerna: det vanliga metabola biproduktet laktat. Författarna visar att laktat kan slå om en molekylär brytare som driver hjärtceller mot en särskild typ av järndriven celldöd och förvärrar skadan. Att förstå denna dolda väg kan peka ut nya läkemedel som bättre skyddar hjärtat vid akut behandling.
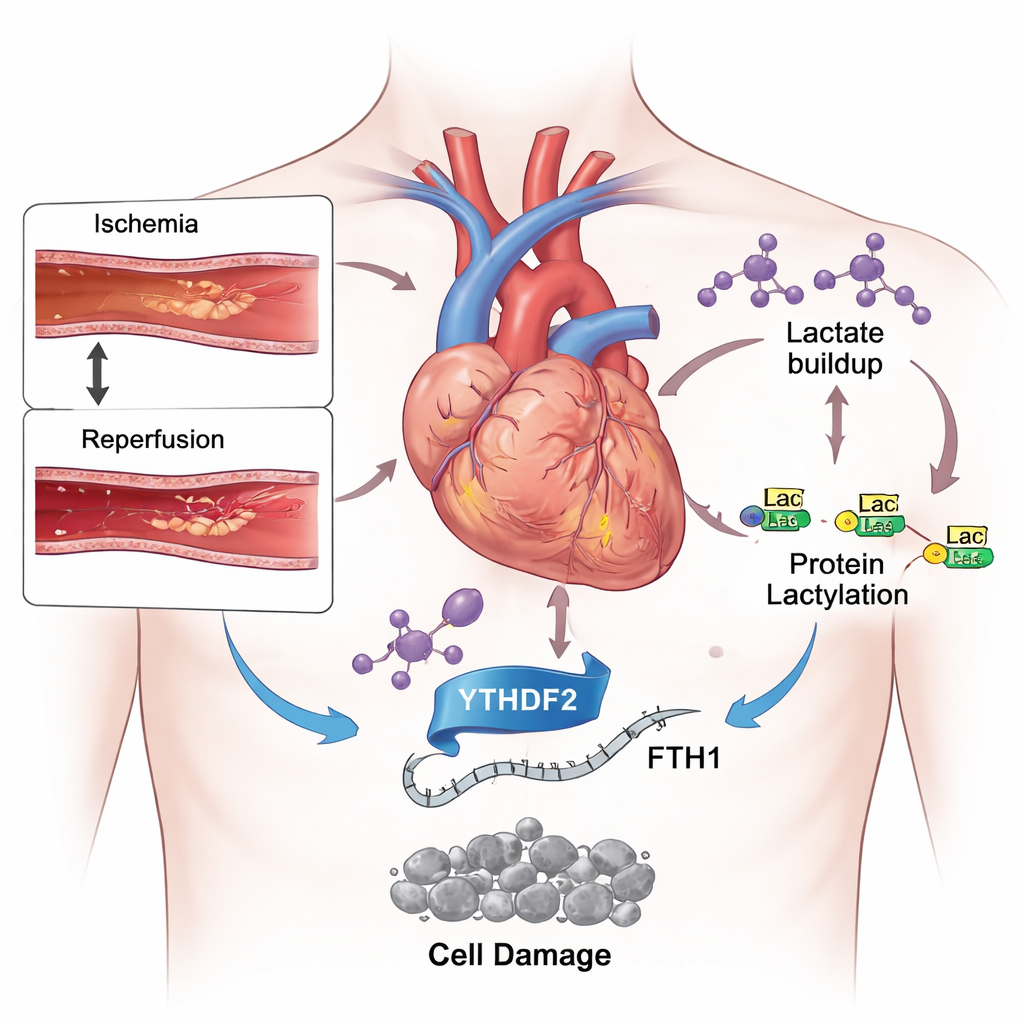
Ett tveeggat svärd i behandlingen av hjärtinfarkt
Modern medicin har blivit mycket bra på att snabbt öppna igentäppta kranskärl och därigenom begränsa den initiala skadan vid en hjärtinfarkt. Ändå kan patienter fortfarande förlora stora områden av hjärtmuskel efter att blodflödet återställts. En orsak är att den plötsliga återkomsten av syre och näring skapar en storm av kemisk stress i hjärcellerna. Bland flera typer av celldöd som utlöses i detta sammanhang har en nyare form, ferroptos, fått uppmärksamhet. Till skillnad från mer bekanta former som apoptos beror ferroptos på järn och okontrollerad oxidation av fetter i cellmembran, vilket kan försvaga hjärtat permanent.
Hur laktat blir mer än bara “mjölksyra-känsla”
Under en hjärtinfarkt skiftar den utsvultna hjärtmuskeln sin energianvändning mot glykolys, ett reservsystem som snabbt bryter ner socker men producerar stora mängder laktat. Genom att använda möss som utsattes för kortvarig blockering och återöppning av ett kranskärl, och odlade hjärtliknande celler exponerade för lågt syre följt av reoxygenering, fann forskarna kraftigt förhöjda laktatnivåer. Samtidigt upptäckte de fler kemiska märken kallade laktolyleringar på många proteiner och på histoner, de byggnadsstommar som organiserar DNA. När de gav djuren ett läkemedel som saktar ner glykolysen och minskar laktatproduktion krympte hjärtskadan, blodmarkörer för skada föll och balansen mellan skadligt järn och skyddande antioxidanter förbättrades. Dessa resultat tyder på att överskott av laktat inte bara är en biprodukt av stress utan en aktiv drivkraft för skada.
En molekylär brytare som lossar järnets koppel
När de grävde djupare fokuserade teamet på YTHDF2, ett protein som läser kemiska märken på RNA och avgör hur snabbt vissa budskap förstörs. De upptäckte att ischemi–reperfusion och tillsatt laktat båda ökade YTHDF2-nivåerna och ökade laktolylering kring genen som kodar för det, vilket förstärkte dess produktion. Ett av YTHDF2:s nyckelmål visade sig vara RNA för ferritin heavy chain 1 (FTH1), en central del av cellens järnlagringsbur. FTH1 brukar binda upp järn i en säker form och förhindra att det driver skadliga reaktioner. I stressade hjärceller band YTHDF2 tätare till FTH1-RNA och påskyndade dess nedbrytning, vilket lämnade cellerna med färre ferritinburar, mer fritt järn, ökad oxidativ stress och klassiska tecken på ferroptos.
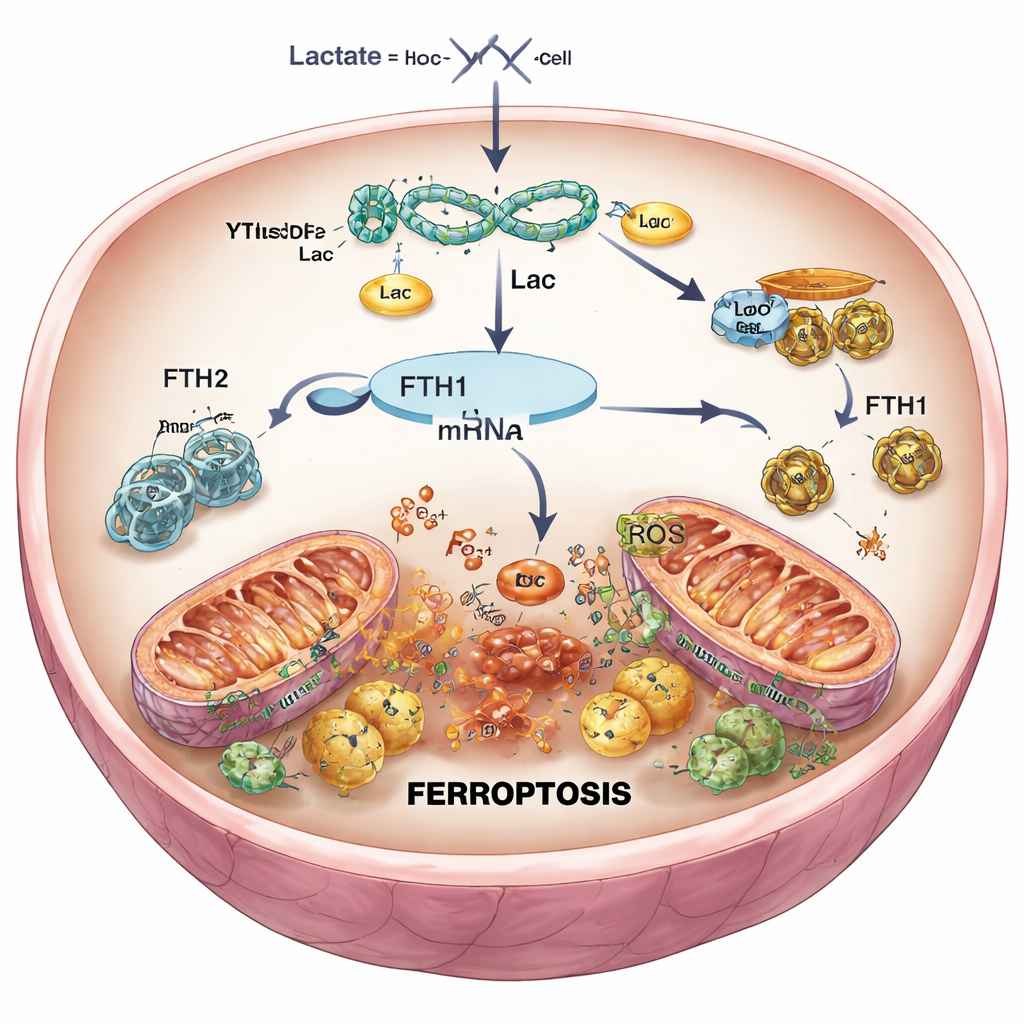
Dämpa dödssignalen i hjärceller
För att testa orsak och verkan använde forskarna genetiska verktyg för att selektivt minska YTHDF2 i hjärceller och i möss. När YTHDF2 slog ned, återhämtade sig FTH1-nivåerna, järn och reaktiva syrearter sjönk, mitokondrierna behöll en mer normal form och den övergripande cellöverlevnaden förbättrades efter simulerad reperfusion. Hos möss innebar mindre YTHDF2 mindre ärrbildning efter hjärtinfarkt och friskare vävnad. När FTH1 samtidigt reducerades försvann dock dessa fördelar i hög grad: järnet steg igen, oxidativ skada återkom och infarktstorleken ökade. Detta bekräftade att YTHDF2 främjar ferroptos huvudsakligen genom att undertrycka FTH1 och därigenom lösa kontrollen över järn i hjärcellerna.
Vad detta betyder för framtida hjärtterapier
Sammanfattningsvis beskriver studien en ny händelsekedja: ett blockerat och sedan återöppnat kärl driver på laktatansamling; laktat ökar YTHDF2 via laktolylering; YTHDF2 förstör sedan RNA-instruktionerna för det järnvakande proteinet FTH1; och den resulterande järnöverdosen utlöser ferroptos och fördjupar hjärtskadan. För patienter är budskapet hoppfullt: denna väg erbjuder flera nya punkter för intervention. Läkemedel som begränsar skadlig laktatsignalering, blockerar den specifika modifieringen av YTHDF2 eller bevarar FTH1-funktionen skulle kunna göra akut reperfusion säkrare och skydda mer hjärtmuskel. Även om dessa fynd fortfarande behöver bekräftas i mänskliga vävnader öppnar de en lovande väg mot mildare och mer effektiva behandlingar för hjärtinfarktöverlevare.
Citering: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
Nyckelord: hjärtinfarkt, laktat, järndriven celldöd, ischemi reperfusionsskada, skydd av hjärtmuskelceller