Clear Sky Science · sv
Dual-specificity fosfataskinas 6 stör forkhead box O1:s repressiva aktivitet mot CYP4A11 som medierar fettansamling i levern
Varför fett i levern spelar roll
Alltför mycket fett i levern, ofta benämnt fettleversjukdom, blir allt vanligare i moderna kostmönster rika på socker och fett. Medan många känner till kolesterol eller blodsocker vet färre att små molekylära brytare inne i levercellerna hjälper avgöra om fett förbränns eller lagras. Denna studie undersöker tre sådana brytare — proteinerna DUSP6, FOXO1 och CYP4A11 — och avslöjar hur deras maktkamp kan driva leverceller att lagra överskott av fett. Att förstå detta dolda kontrollsystem kan peka ut nya behandlingsvägar för fettleversjukdom och relaterade metabola problem.
En dold trafikreglerare inne i leverceller
Forskarna fokuserade på ett protein kallat DUSP6, som huvudsakligen är känt för att stänga av en cellsignalväg kallad ERK‑vägen. Tidigare arbete visade att möss utan DUSP6 överraskande nog var motståndskraftiga mot dietinducerad fettleversjukdom, och deras lever hade lägre nivåer av CYP4A‑enzymer, som är involverade i fettmetabolism. Här ställde teamet frågan vad DUSP6 gör i humana leverderiverade celler och hur det kan påverka en mänsklig form av dessa enzymer kallad CYP4A11. De använde två vanliga levercancercellsinjer, HepG2 och HuH‑7, som ersättning för mänskliga leverceller och mättade dem med en blandning av fettsyror (palmitinsyra och oljesyra) för att efterlikna en ohälsosam, högfettig miljö. 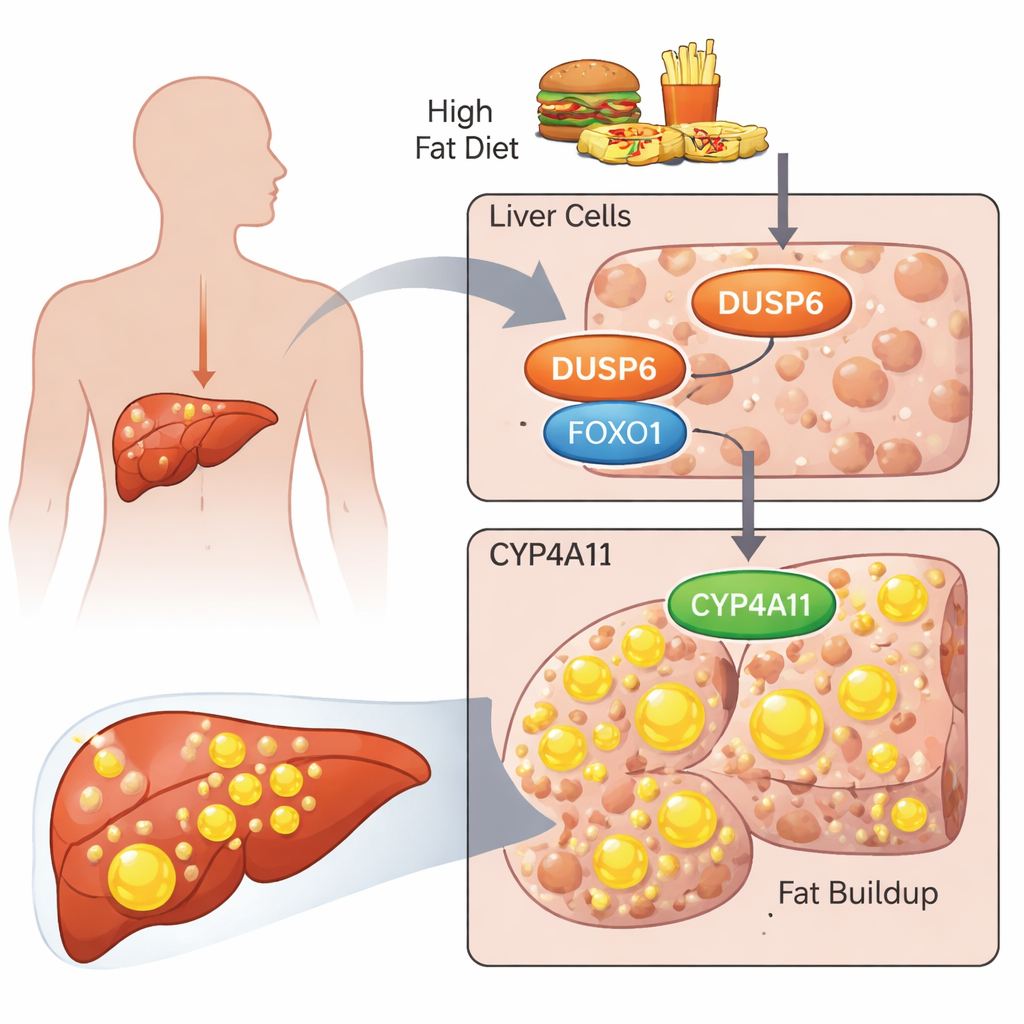
Från fettsyror till en fettfylld cell
När cellerna utmanades med dessa fettsyror samlade de synligt på sig fettdroppar, vilka forskarna färgade och mätte. Samtidigt steg nivåerna av DUSP6 och CYP4A11, tillsammans med aktiverade former av två stora signalproteiner, AKT och FOXO1. Nedreglering av DUSP6 med riktade RNA‑molekyler vände detta mönster: cellerna lagrade mindre fett, CYP4A11‑nivåerna sjönk, men aktiverade ERK, AKT och FOXO1 ökade. Att blockera ERK‑vägen ensam gjorde faktiskt fettansamlingen värre, medan att blockera AKT ensam minskade den. När både ERK och AKT hämmdes samtidigt minskade fettansamlingen och CYP4A11‑nivåerna föll. Dessa experiment knöt CYP4A11 tätt till hur mycket fett som byggs upp och föreslog att AKT‑aktivitet är särskilt viktig för att driva fettlagring.
En broms på fett‑främjande gener
En annan nyckelspelare, FOXO1, är en transkriptionsfaktor — ett protein som kan gå in i cellkärnan och slå av eller på gener. FOXO1 är känd för att fungera som en broms på flera medlemmar av samma enzymfamilj som CYP4A11. Teamet fann att minskade nivåer av FOXO1 fick cellerna att hamstra mer fett och ökade CYP4A11, medan direkt överuttryck av CYP4A11 gjorde cellerna ännu fetare. I kontrast minskade tvingat överuttryck av FOXO1 både CYP4A11 och fettansamling. Ett läkemedel som blockerar CYP4A11‑aktivitet (HET0016) reducerade det extra fett som orsakades av låg FOXO1, vilket stöder idén att CYP4A11 inte bara är en åskådare utan en drivande faktor i lipidsamling. Kemiska analyser visade att HET0016 sänkte 20‑HETE, en produkt som bildas av CYP4A11 och är kopplad till oxidativ stress och inflammation, vilket ytterligare knyter denna väg till leverskada.
Hur DUSP6 avväpnar bromsen
För att förstå hur FOXO1 reglerar CYP4A11 undersökte forskarna DNA‑regionen framför CYP4A11‑genen och fann sekvenser där FOXO1 kan binda. Med en kromatinimmunutfällningsanalys visade de att FOXO1 — särskilt dess icke‑fosforylerade form — binder direkt till CYP4A11:s promotor, vilket stämmer med en repressiv, bromsande roll för denna gen. Co‑immunoprecipitationsförsök visade att DUSP6 fysiskt interagerar med FOXO1 men inte med dess fosforylerade form. Fraktionerings‑ och mikroskopistudier visade att DUSP6 finns i cellens cytoplasma och, när det är närvarande, håller mer FOXO1 utanför kärnan. När DUSP6 nedreglerades flyttade mer FOXO1 in i kärnan, där det kunde binda DNA och undertrycka CYP4A11. I praktiken fungerar DUSP6 som ett ankare som sequestrar FOXO1 i cytoplasman och hindrar det från att utföra sin bromsande funktion på CYP4A11. 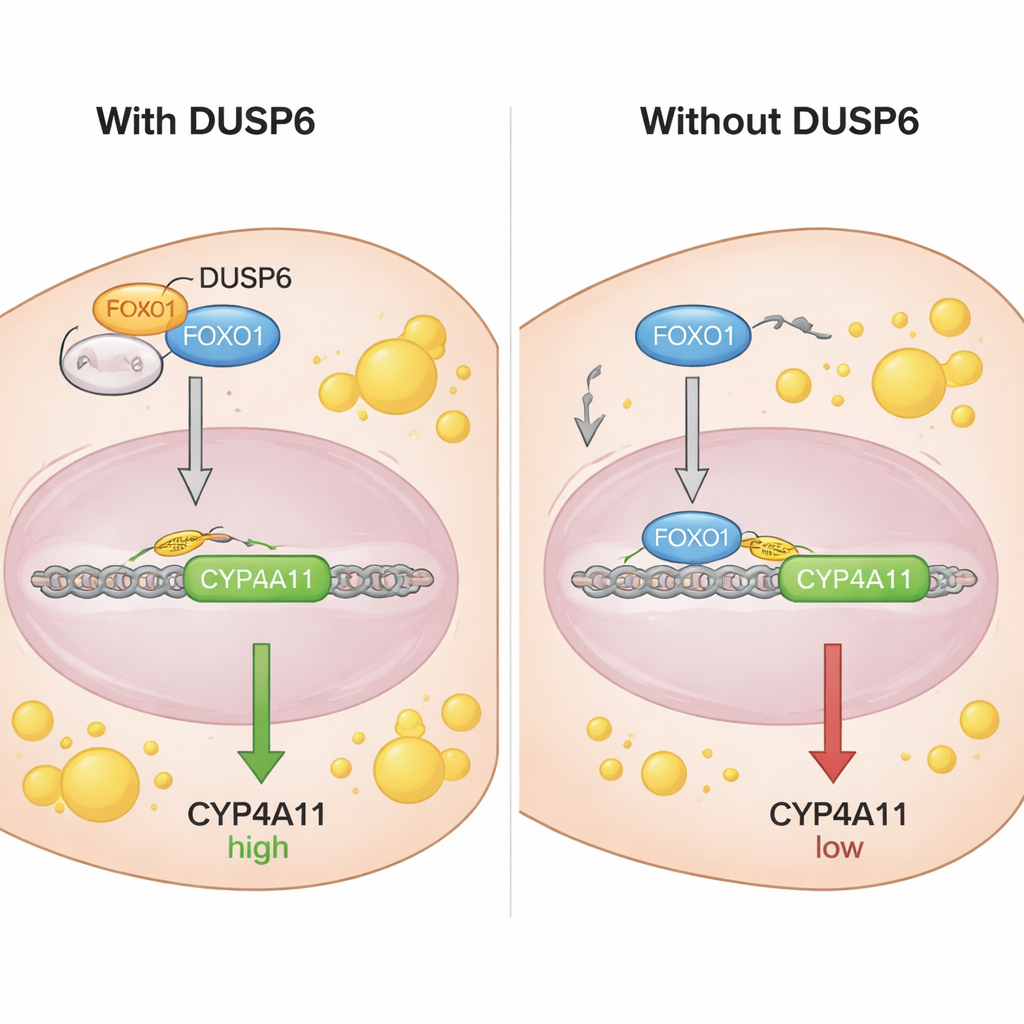
Vad detta betyder för fettlevern och vidare
Enkelt uttryckt kartlägger arbetet en händelsekedja inne i leverceller: DUSP6 håller FOXO1 i cytoplasman, vilket försvagar FOXO1:s förmåga att stänga av CYP4A11‑genen. Med FOXO1 ur spel blir CYP4A11 mer aktivt, vilket bidrar till att driva cellen mot ökad fettlagring och produktion av molekyler som 20‑HETE som kan främja oxidativ stress och inflammation. Även om dessa fynd kommer från odlade lever‑deriverade celler och inte från frisk mänsklig levervävnad, lyfter de fram DUSP6 och CYP4A11 som potentiella nya mål för behandling av metabolisk dysfunktionsassocierad steatotisk leversjukdom. Terapier som minskar DUSP6‑aktivitet eller dämpar CYP4A11:s effekter skulle i teorin kunna återställa FOXO1:s bromsande funktion och hjälpa till att hålla leverfettet under kontroll.
Citering: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Nyckelord: fettleversjukdom, DUSP6, FOXO1, CYP4A11, levermetabolism