Clear Sky Science · sv
Gruvdrift i DrugBank med maskininlärning avslöjar nya kandidater för BCL‑2‑hämning
Varför det är viktigt att hitta smartare cancerläkemedel
Cancerceller vägrar ofta att dö när de borde. Många tumörer överlever genom att överanvända en familj av ”bodyguard”-proteiner kallade BCL‑2 som blockerar cellens inbyggda självmordsprogram. Det finns redan läkemedel som riktar sig mot BCL‑2, men de kan ge biverkningar och fungerar inte för alla patienter. Denna studie undersöker hur modern maskininlärning kan sålla bland tusentals befintliga läkemedel för att hitta nya, säkrare kandidater som kan desarmera BCL‑2 och hjälpa cancerceller att gå i apoptos.
Hur celler väljer mellan liv och död
Friska vävnader avlägsnar ständigt skadade eller onödiga celler genom en kontrollerad självdestruktionsprocess känd som apoptos, eller programmerad celldöd. En grupp proteiner kallad BCL‑2‑familjen fungerar som en central omkopplare för detta beslut. Vissa medlemmar driver celler mot överlevnad, medan andra driver dem mot död. I många cancerformer produceras de överlevnadsfrämjande medlemmarna, inklusive BCL‑2 och dess nära släkting BCL‑XL, i överskott. Detta extra skydd gör att cancerceller kan ignorera dödssignaler och motstå kemoterapi. Därför har blokkering av BCL‑2 blivit en attraktiv strategi i cancerbehandling, men nuvarande läkemedel träffar ofta besläktade proteiner också, vilket leder till biverkningar som farliga sänkningar av blodplättsantalet.
Att lära datorer känna igen lovande molekyler
I stället för att söka efter nya föreningar från grunden vände forskarna sig till databaser över molekyler som redan studerats eller används som läkemedel. De började med en stor offentlig resurs kallad ChEMBL, som innehåller experimentella mätningar av hur starkt olika kemikalier binder till BCL‑2. Efter noggrann rensning av denna information — borttagning av dubbletter, osäkra mätningar och alltför stora eller ovanliga molekyler — hamnade de på 601 välkarakteriserade föreningar. Varje molekyl översattes till en sorts digitalt fingeravtryck som fångar dess strukturella egenskaper. Dessa fingeravtryck användes för att träna och jämföra sju olika maskininlärningsmodeller i uppgiften att avgöra om en ny molekyl sannolikt är en stark BCL‑2‑hämmare eller i praktiken inaktiv. 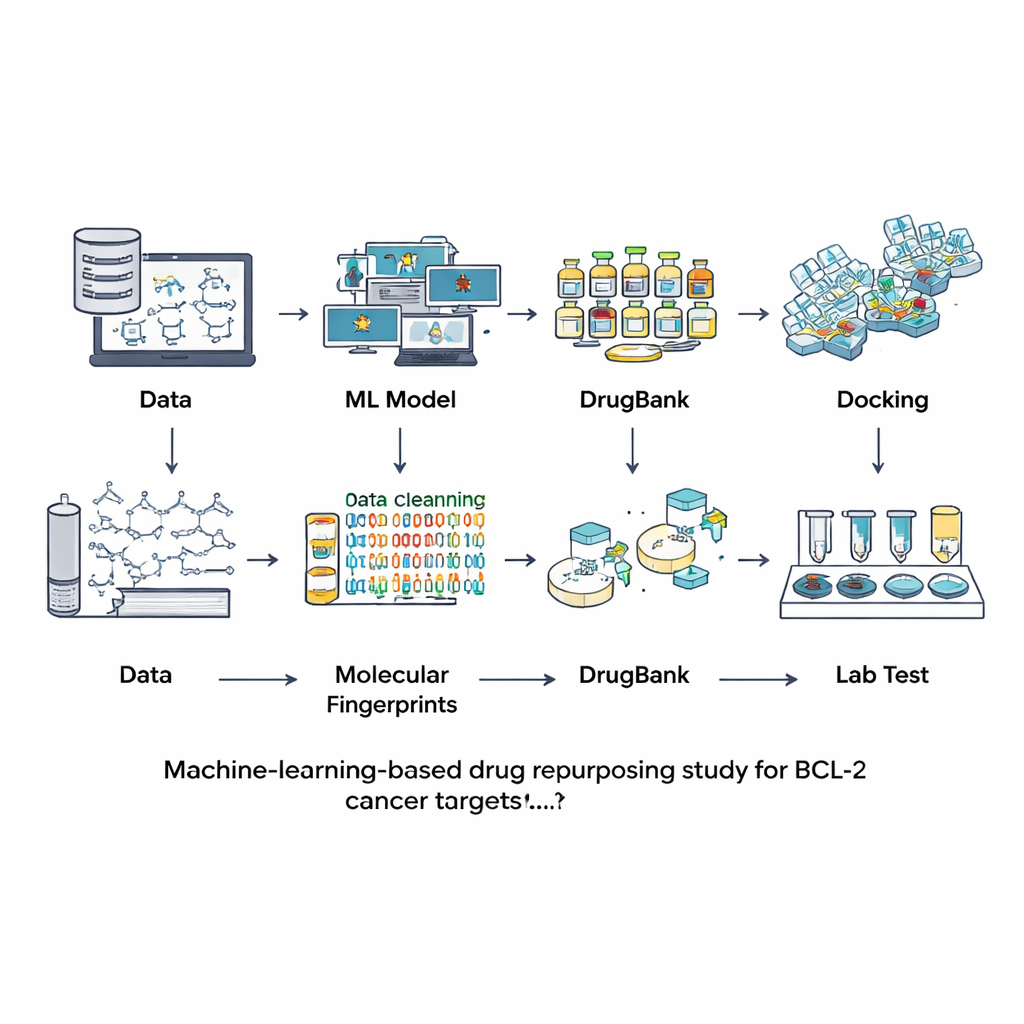
Välja bästa modellen och skanna ett läkemedelsbibliotek
Teamet utvärderade modellerna med ett separat testset som inte användes under träningen, och kontrollerade inte bara hur ofta varje modell hade rätt utan också hur väl den skiljde aktiva från inaktiva och hur balanserade förutsägelserna var. En modell kallad LightGBM — en modern, träd‑baserad boostingmetod — presterade bäst över flest mått, inklusive total noggrannhet och dess förmåga att tilldela pålitliga sannolikheter. Med denna finjusterade modell i handen vände forskarna sig till DrugBank, en kurerad samling av mer än 12 000 godkända, experimentella och indragna läkemedel. Efter att ha beräknat samma typ av fingeravtryck frågade de LightGBM vilka av dessa molekyler som såg ut som potentiella BCL‑2‑hämmare. Endast nio föreningar fick höga poäng, ungefär den översta tiondelen av en procent av hela biblioteket, vilket visar att den virtuella screeningen var mycket selektiv. Fyra av de nio var redan kända BCL‑2‑hämmare, vilket försäkrade teamet om att tillvägagångssättet var rimligt.
Från datorträffar till molekylära interaktioner
Bland de återstående högt rankade molekylerna fokuserade forskarna på tre som tidigare inte kopplats till BCL‑2: Dersalazine, Opelconazole och Zongertinib. För att se om dessa kandidater rimligen kunde passa in i BCL‑2:s bindningsficka använde de molekylär dockning, en teknik som förutspår hur en liten molekyl kan lägga sig i proteinets yta. Simulationerna antydde att Opelconazole och Zongertinib, i synnerhet, bildar nätverk av gynnsamma kontakter med samma nyckelaminosyror som håller ett välstuderat referensläkemedel, ABT‑737. Deras förutsagda bindningsstyrkor låg nära dem hos etablerade hämmare, vilket antyder att maskininlärningsmodellen faktiskt hade upptäckt molekyler kapabla att desarmera BCL‑2. 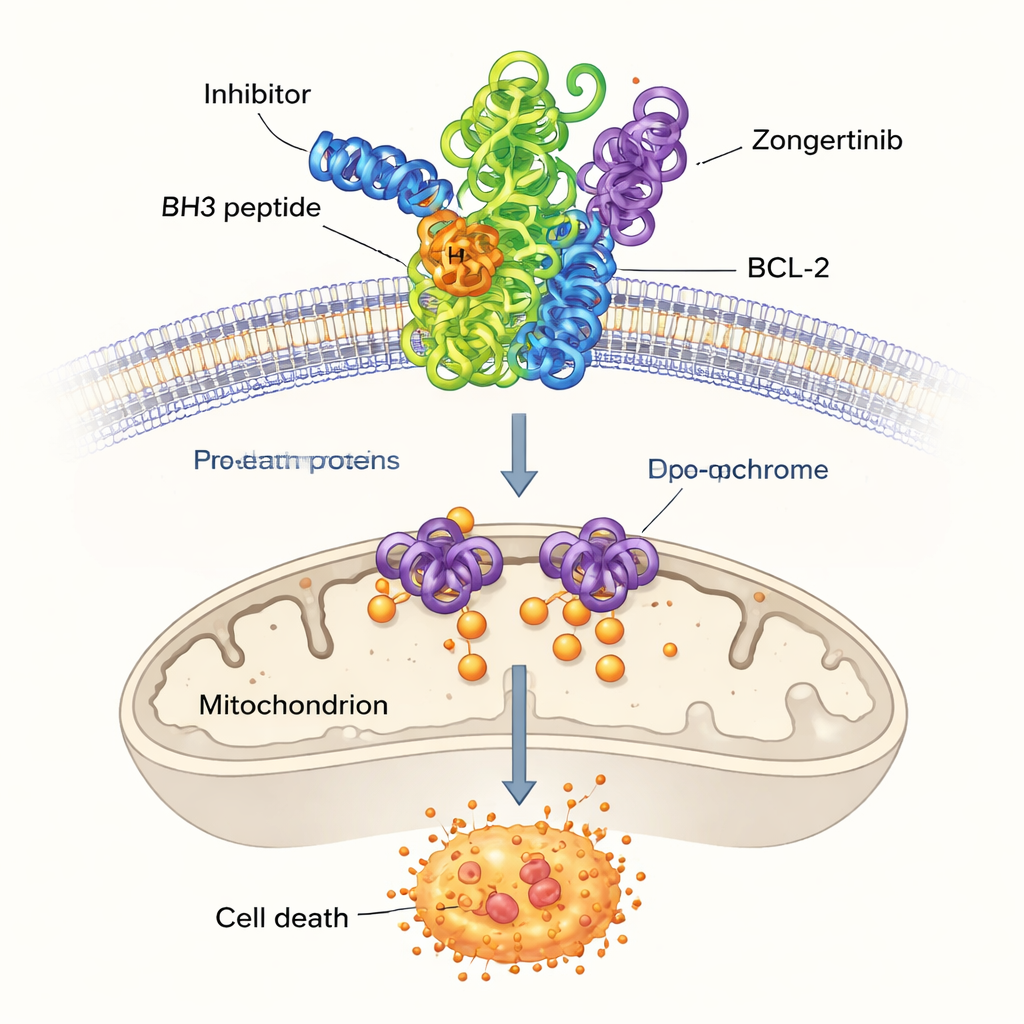
Sätta förutsägelserna på prov i labbet
Beräkningsmässiga ledtrådar är endast användbara om de håller under verkliga förhållanden. Teamet testade därför de tre kandidaterna i ett biokemiskt assay som mäter hur väl en förening kan förhindra att BCL‑2 binder till en av sina naturliga partners. Vid en rad koncentrationer visade Dersalazine liten effekt. Opelconazole och Zongertinib minskade däremot båda BCL‑2‑aktiviteten vid höga doser, med Opelconazole som nästan stängde ner signalen. Även om dessa koncentrationer är högre än vad som vore idealiskt för ett kliniskt färdigt läkemedel, visar de att kandidaterna verkligen interagerar med BCL‑2 och validerar den övergripande upptäcktsprocessen.
Vad detta betyder för framtida cancerterapier
För en icke‑specialist är huvudbudskapet att forskarna framgångsrikt tränade ett datorsystem att känna igen hur en BCL‑2‑blockerande molekyl ”ser ut”, och sedan använde det för att gräva igenom ett stort bibliotek av befintliga läkemedel och läkemedelslika föreningar. Tillvägagångssättet återupptäckte kända BCL‑2‑läkemedel och framhävde nya kandidater, varav två visade verklig hämmande aktivitet i laboratorietester. Även om mycket arbete återstår — förbättra potens, förstå säkerhet och testa i celler och djur — visar denna studie hur maskininlärning och smart datarensning kan påskynda jakten på bättre cancerläkemedel genom att återanvända och omvärdera föreningar vi redan känner till.
Citering: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Nyckelord: BCL‑2‑hämmare, maskininlärning, läkemedelsomdirigering, apoptos, cancerterapi