Clear Sky Science · sv
Kristallstruktur för Echinococcus multilocularis cystatin B avslöjar en ny egenskap hos klassiska stefiner
Varför en leverparasits hemliga vapen spelar roll
Alveolär echinokockinfektion är ett långt namn för en liten bandmaskinfektion som beter sig mycket som en långsamt växande cancer i levern. Den är ofta dödlig, och dagens läkemedel fungerar dåligt och kan ge allvarliga biverkningar. Denna studie undersöker en särskild molekyl som parasiten tillverkar, ett protein kallat EmCystatin-B, för att förstå hur det kan hjälpa masken att undkomma våra försvar — och hur det en dag skulle kunna bli ett mål för nya behandlingar.
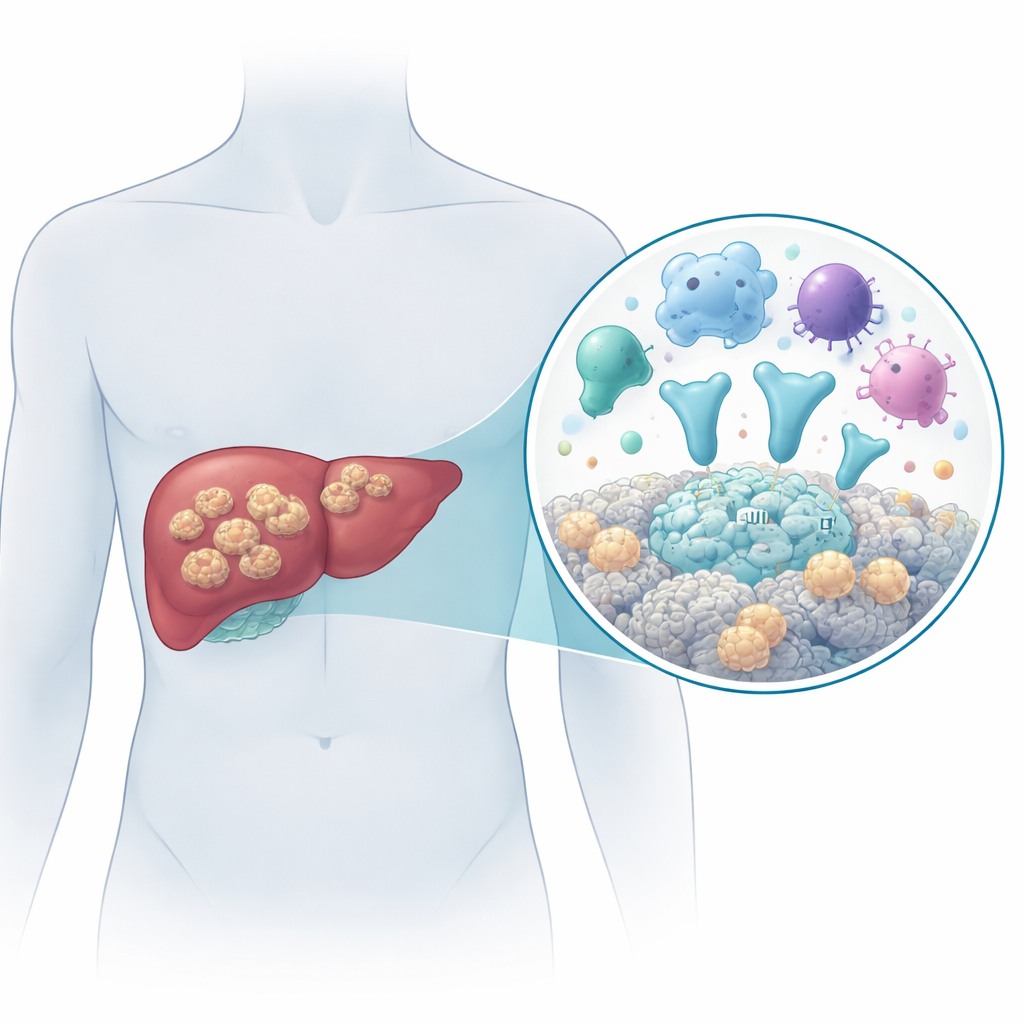
En farlig bandmask som växer som en tumör
Sjukdomen orsakas av larvstadiet av bandmasken Echinococcus multilocularis. Människor blir smittade genom att av misstag svälja parasitägg, till exempel via förorenad mat eller vatten. När äggen hamnar i kroppen etablerar larverna sig främst i levern och växer som många små vätskefyllda blåsor som infiltrerar omgivande vävnad, sprider sig till intilliggande organ som mjälten och ibland når avlägsna platser som lungor eller hjärna. Utan effektiv behandling dör mer än 9 av 10 patienter inom 10–15 år. Kirurgi i kombination med långvarig antiparasitisk medicin är för närvarande det bästa alternativet, men tidig diagnos är svår och läkemedlen botar inte alltid infektionen. Det gör det avgörande att förstå hur parasiten interagerar med människokroppen på molekylär nivå.
Ett parasitprotein som avväpnar klippande enzymer
Många djur, inklusive människor, producerar en familj proteiner som kallas cystatiner som fungerar som säkerhetslås på kraftfulla matsmältningsenzymer kända som cysteinproteaser. Dessa enzymer kan klippa sönder andra proteiner och är viktiga för processer som att bryta ner utslitna cellkomponenter och aktivera immunsvar. Parasiter har lärt sig att tillverka sina egna cystatinlika proteiner för att störa värdens enzymer och immunsystem. I detta arbete identifierade forskarna ett cystatinlikt protein från E. multilocularis och kallade det EmCystatin-B. De fann att genen för EmCystatin-B är mycket mer aktiv i parasitens mogna larvhövdningar (protoscolex) än i den omgivande cystvävnaden, och att proteinet finns i cytoplasman och kärnan i parasitens celler, särskilt i delande "stamliknande" germinativa celler. Laboratorietester visade att EmCystatin-B starkt kan blockera aktiviteten hos mänsklig cathepsin B, en viktig cysteinproteas involverad i immunitet och vävnadsombyggnad.
En bekant form med en oväntad twist
För att se exakt hur EmCystatin-B är uppbyggt kristalliserade teamet det renade proteinet och använde röntgenkristallografi för att lösa dess tredimensionella struktur på nästintill atomisk upplösning. Liksom andra medlemmar i cystatinfamiljen har varje EmCystatin-B-enhet en karaktäristisk form: ett centralt helixsegment stöds av flera platta, bandliknande strängar och bildar en kil som normalt passar in i ett proteas aktivt centrum. Baserat på dess sekvens och avsaknad av en tydlig signalpeptid för sekretion tillhör EmCystatin-B "stefin"-undergruppen av cystatiner, som vanligtvis är små, intracellulära proteiner utan stabiliserande disulfidbindningar. Överraskande visade strukturen att även om varje EmCystatin-B-enhet har den förväntade folden, är sättet dessa enheter associerar med varandra ovanligt och artspecifikt jämfört med den mänskliga motsvarigheten, cystatin B.
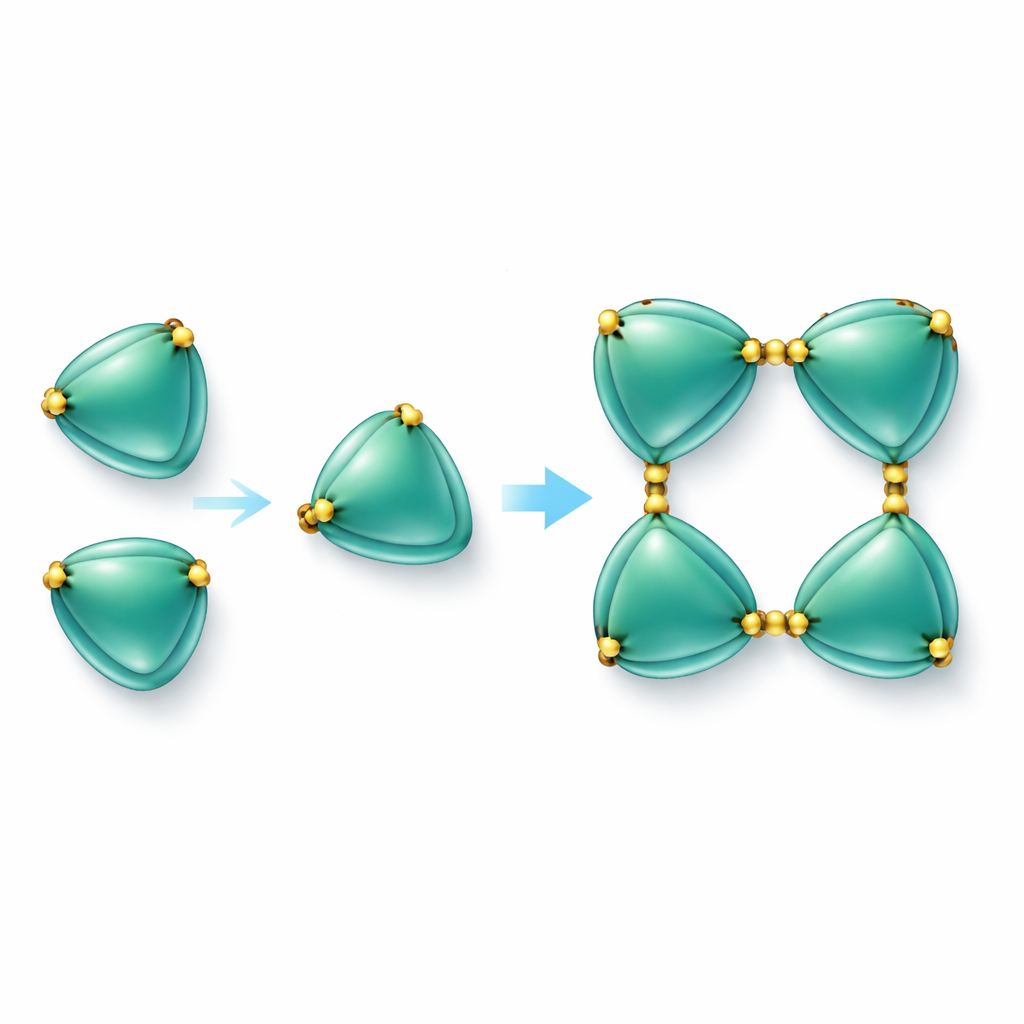
Bygga proteinkedjor med svavelbindningar
Det mest anmärkningsvärda fyndet var att EmCystatin-B-molekyler inte enbart existerar som enskilda enheter. Istället kan de förena sig stegvis för att bilda dimerer (par) och sedan tetramerer (grupper om fyra). Två olika mekanismer hjälper till att bilda de initiala dimererna. I den ena svänger en del av en molekyl över och fullbordar grannens struktur, ett fenomen som kallas domänväxling. I den andra binds par av molekyler ihop av disulfidbryggor — starka kemiska länkar mellan svavelinnehållande aminosyror (cystein). I EmCystatin-B binder cystein vid position 4 i en molekyl till cystein vid position 76 i en partner. Fyra sådana korslänkar stabiliserar sedan tetrameren. Denna användning av flera intermolekylära disulfidbryggor är helt ny för klassiska stefiner, som vanligtvis saknar sådana bindningar. När forskarna bytte ut dessa nyckelcystein mot en annan aminosyra kunde proteinet inte längre sätta ihop sig effektivt till högre ordningskomplex och dess förmåga att hämma cathepsin B minskade kraftigt.
Vad detta betyder för att bekämpa infektion
För en icke-specialist är budskapet att parasiten utvecklat en särskilt konstruerad variant av en vanlig proteinfamilj, som använder extra kemiska "nit" för att låsa flera inhibitorenheter tillsammans. Denna oligomeriska form verkar viktig för att stänga av ett värdenzym som annars skulle hjälpa till att kontrollera infektionen. Genom att avslöja EmCystatin-B:s precisa arkitektur och dess unika disulfidbundna sammankopplingar utvidgar studien vår förståelse för hur cystatinproteiner kan skräddarsys mellan arter. På lång sikt kan dessa insikter vägleda designen av läkemedel som antingen blockerar EmCystatin-B:s skyddande effekt för parasiten eller efterliknar dess immundämpande egenskaper för att behandla inflammatoriska sjukdomar.
Citering: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Nyckelord: alveolär echinokockinfektion, Echinococcus multilocularis, cystatin B, proteinstruktur, immunmodulering