Clear Sky Science · sv
Störning av NLRP3-inflammasomets montering genom ligandinducerad ombyggnad av pyrindomänsgränssnitt
Varför det är viktigt att dämpa okontrollerad inflammation
Många kroniska sjukdomar — från artrit och gikt till hjärtsjukdom och neurodegeneration — drivs av ett överaktivt immunlarm inuti våra celler. En nyckelkomponent i detta larm, kallad NLRP3-inflammasomet, hjälper oss att bekämpa infektioner men kan också orsaka skadlig inflammation när det går fel. Denna studie beskriver en ny liten molekyl, benämnd E9, som riktar in sig på ett tidigt steg i NLRP3-aktivering och erbjuder en ny infallsvinkel för att utveckla läkemedel som kyler ner skadlig inflammation utan att helt stänga av immunsystemet.
En cellulär brandvarnare med en mörk sida
När vår kropp känner fara monterar immunceller ihop NLRP3-inflammasomet, ett stort proteinkomplex som fungerar som en molekylär brandvarnare. När det väl bildats aktiverar strukturen ett enzym kallat kaspas-1, vilket i sin tur aktiverar potenta inflammatoriska budbärare, inklusive cytokinerna IL-1β och IL-18. Dessa signaler är viktiga för att bekämpa infektioner och rensa bort skadad vävnad. Men om inflammasomet förblir aktivt för länge eller slås på vid fel tidpunkt bidrar det till kroniska inflammatoriska tillstånd som påverkar leder, blodkärl, hjärna och andra organ. Därför söker forskare världen över efter precisa sätt att kontrollera NLRP3 utan att brett undertrycka immuniteten.
Bortom de vanliga läkemedelsmålen
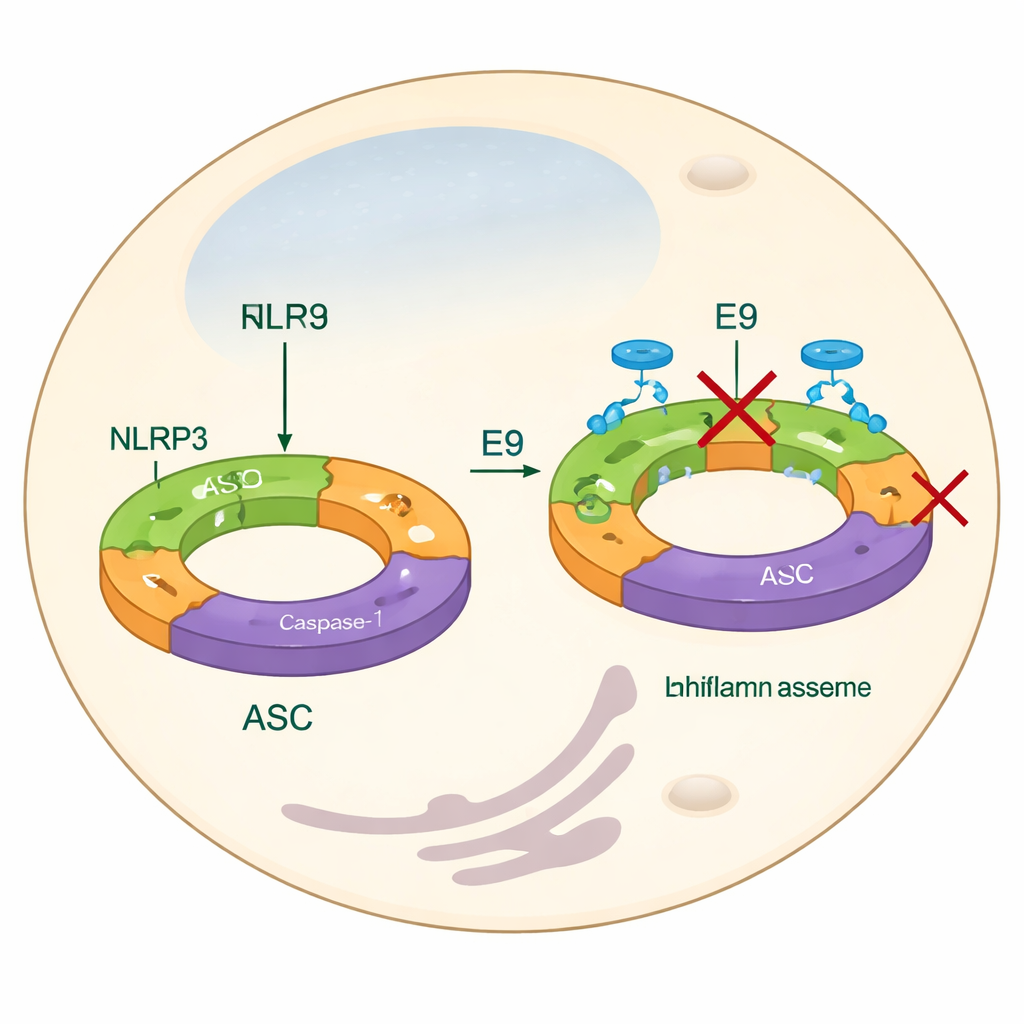
De flesta nuvarande strategier för att tygla NLRP3 fokuserar på att blockera dess slutprodukter — som IL-1β — eller på att störa en central, motorliknande domän som använder energimolekyler som ATP. Medan dessa angreppssätt kan fungera kan de missa de tidigaste monteringsstegen och adresserar inte fullt ut hur NLRP3-proteiner går ihop för att bilda en funktionell maskin. I detta arbete riktar författarna istället in sig på pyrindomänen, en del av NLRP3 som hjälper individuella enheter att haka i varandra till långa filament. Dessa filament rekryterar sedan en annan adaptorprotein, ASC, som klumpar ihop sig i ljusstarka ”specks” inuti celler — ett visuellt kännetecken för inflammasomaktivering. Genom att hitta kemikalier som förhindrar att pyrindomäner passar ihop ordentligt syftar teamet till att stoppa inflammasomets bildning från början.
Att hitta en molekyl som bryter kedjan
Forskarna screenade ett bibliotek med 1500 nyligen syntetiserade små molekyler med hjälp av ett smart ljusbaserat test. De fäste delade fragment av ett luciferasenzym vid NLRP3:s pyrindomän; när två pyrindomäner möttes, satte enzymfragmenten ihop sig igen och gav ifrån sig ljus. Föreningar som blockerade pyrin–pyrin-kontakt gjorde att ljussignalen sjönk. Ur denna screening identifierade man fyra lovande kandidater, där en — E9 — stack ut för sin starka och konsekventa hämning. Uppföljande mätningar med en teknik kallad mikroskopisk termofores visade att E9 band hårt till pyrindomänen vid mycket låga (submikromolära) koncentrationer, vilket bekräftar att dess effekt inte var ett slumpmässigt artefakt utan resultatet av en specifik interaktion.
Att se effekten inne i levande celler
För att testa om E9 också fungerade i ett levande system använde teamet humana immuncelliga celler som var konstruerade att producera en fluorescerande version av ASC. När dessa celler stimuleras med bakteriella komponenter och en andra trigger slås NLRP3 på och ASC-proteiner klustras i ljusstarka specks som kan räknas under mikroskopet. I närvaro av E9 minskade antalet specks markant, jämförbart med eller bättre än några kända NLRP3-hämmare. Detta visade att störning av pyrindomänkontakter räcker för att reducera inflammasommontering och de tidiga stegen av inflammatorisk celldöd, åtminstone under laboratorieförhållanden.
Hur E9 omformar inflammasomets ställning
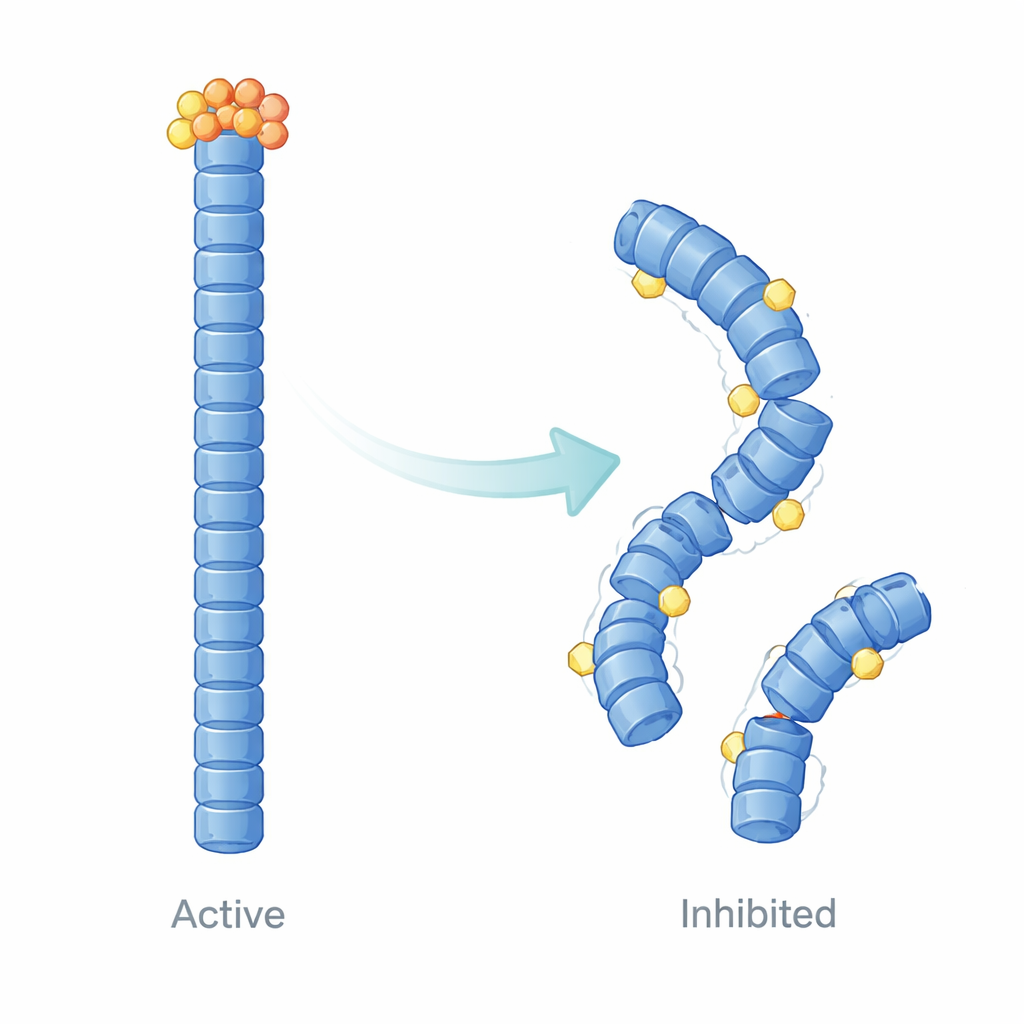
Utöver bindningsmätningar använde författarna datorbaserad strukturell modellering och molekyldynamiksimuleringar för att visualisera hur E9 förändrar beteendet hos NLRP3-filament över tid. Deras beräkningar tyder på att E9 lägger sig vid specifika kontaktytor där pyrindomäner möts och subtilt luckrar upp och omformar filamentet. Istället för en enhetligt stabil, kooperativ struktur blir filamentet ojämnt: regioner nära bundet E9 blir mer flexibla och förlorar sin precisa inriktning, medan andra delar blir dynamiskt isolerade. Dessa förändringar dämpar storskaliga rörelser och tät kommunikation som behövs för effektiv ASC-rekrytering, vilket ger en fysikalisk förklaring till den minskade speckbildningen som observerats i celler.
Vad detta kan innebära för framtida terapier
Sammantaget positionerar fynden E9 som en prototyp för en ny klass av inflammasomriktade läkemedel som verkar genom att störa gränssnitten mellan NLRP3-byggstenarna snarare än genom att blockera dess energianvändning eller slutprodukter. Även om det nuvarande arbetet är begränsat till provrörsassayer, datorbaserade simuleringar och odlade celler — och att ytterligare studier i djur och människor behövs — visar det att noggrant designade små molekyler kan omforma själva inflammasomets stomme. För patienter med sjukdomar drivna av okontrollerad inflammation skulle sådana gränssnitts‑fokuserade läkemedel kanske en dag erbjuda mer precis kontroll, genom att minska skadlig immunaktivering samtidigt som viktiga försvar i stor utsträckning bevaras.
Citering: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Nyckelord: NLRP3-inflammasom, pyrindomän, liten molekylhämmare, medfödd immunitet, pyroptos