Clear Sky Science · sv
Hepatitvirusassocierad B‑cells-non‑Hodgkins-lymfom involverar störd epigenetisk och RNA‑medierad reglering av genuttryck samt förändrad snoRNA‑transkription
Varför levervirus är viktiga för immunsystemet
Hepatit B‑ och D‑virus är mest kända för att skada levern, men växande bevis tyder på att de också kan bidra till att utlösa vissa blodcancerformer. Denna studie undersöker hur kronisk infektion med dessa virus kan förändra B‑cellernas beteende — viktiga försvarsceller i vårt immunsystem — på sätt som ökar risken för B‑cells-non‑Hodgkins-lymfom, en grupp cancerformer som uppstår från just dessa celler.
Följer patienter där infektioner är vanliga
För att undersöka dessa samband studerade forskarna patienter i Mongoliet, ett land med några av världens högsta förekomster av kronisk hepatit B och D. De samlade blodprover från fem grupper: personer med enbart hepatit B, personer med både hepatit B och D, patienter som hade både infektion och B‑cellslymfom, patienter med lymfom men utan virusinfektion, samt friska frivilliga. Från dessa prover isolerade de perifera B‑celler — de cirkulerande B‑cellerna som patrullerar blodomloppet — och använde RNA‑sekvensering för att läsa vilka gener som var aktiva eller tysta i varje grupp.
Immunceller som verkar nedreglerade
När teamet jämförde mönster av genaktivitet fann de att B‑celler från kroniskt infekterade patienter bar en signatur av bred immunnedsättning. Jämfört med B‑celler från friska personer och från lymfompatienter utan infektion visade infekterade patienters B‑celler minskad aktivitet i gennätverk kopplade till immunaktivering och svar på inflammatoriska signaler. Analyser av uppströmsregulatorer föreslog att viktiga immunstimulerande faktorer, såsom nyckelcytokiner och B‑cellsreceptorvägar, i praktiken hölls tillbaka, medan flera molekyler som hämmar dessa signalvägar var mer aktiva. Sammantaget målar data upp bilden av B‑celler som är mindre responsiva och mer dämpade vid långvarig hepatitinfektion.
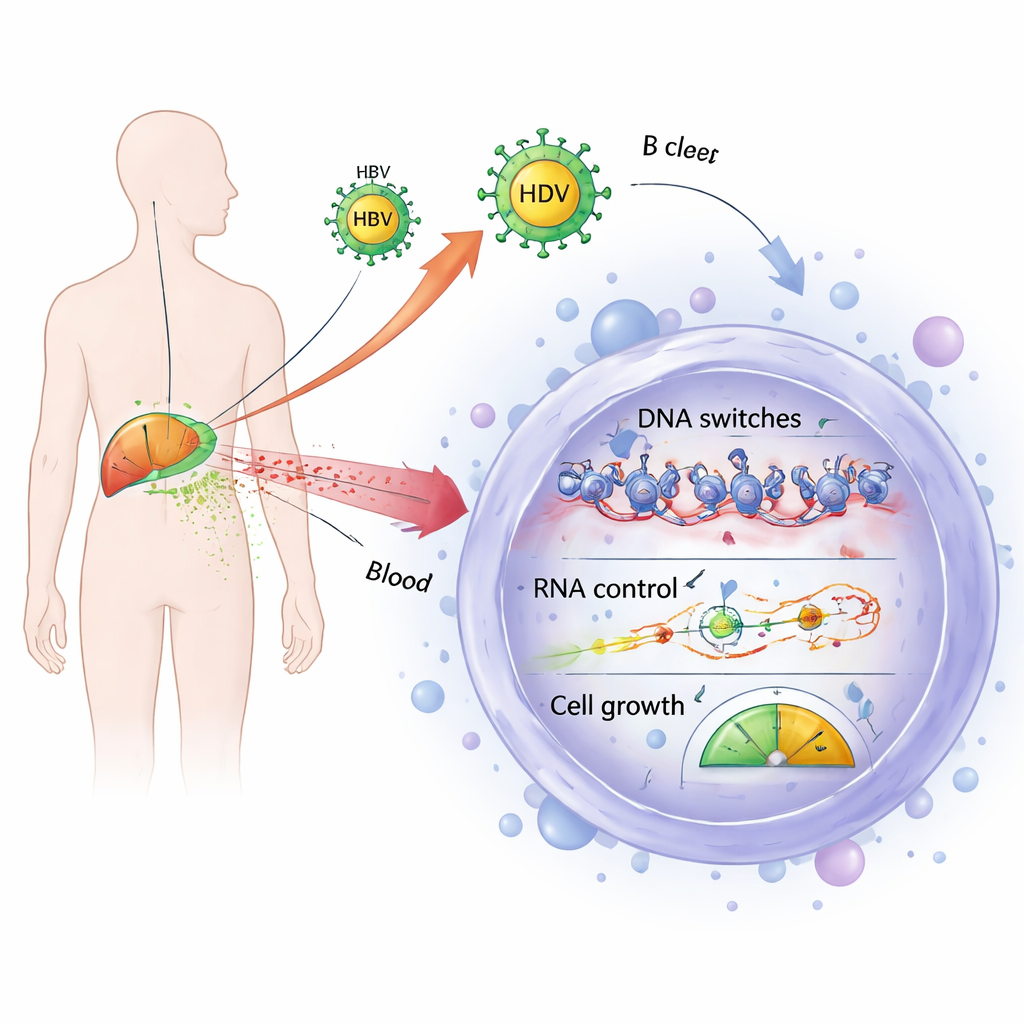
Delade problem i genreglering hos infekterade och cancerösa B‑celler
Forskarna koncentrerade sig sedan på gener som konsekvent var mer aktiva i alla sjukdomsgrupper — både i infekterade patienter och i lymfompatienter — jämfört med friska givare. De identifierade 185 sådana gener och fann att många är involverade i att kontrollera hur DNA paketeras och läses (epigenetisk reglering) samt hur RNA‑budskap bearbetas och tystas. Detta inkluderade flera komponenter i kromatinombyggande komplex och enzymer som lägger till eller tar bort kemiska markörer på histonproteiner, vilka påverkar åtkomsten till gener. Det inkluderade också nyckelkomponenter i maskineriet som microRNA använder för att slå ner målbudskap. Eftersom normal B‑cellsutveckling är beroende av noggrann kontroll av dessa system, tyder deras överaktivering i både virusassocierade och icke‑relaterade lymfom på en gemensam väg genom vilken B‑celler kan skjutas mot malign transformation.
Ovanliga ökningar av små RNA i infekterade B‑celler
En av de mest påfallande fynden var specifik för virusinfekterade patienter: en bred ökning av små nukleolära RNA, så kallade snoRNA, i deras B‑celler. Dessa små RNA‑molekyler finns normalt i cellens nukleol där de hjälper till att modifiera ribosomalt RNA och bygga ribosomer, fabrikerna som tillverkar proteiner. Vid hepatit B‑ och D‑infektion är det känt att virusen utnyttjar nukleolära funktioner för att stödja sin egen replikation. Här fann teamet 69 distinkta snoRNA vars aktivitet förändrades, mestadels ökade i infekterade B‑celler, särskilt i dem med endast hepatit B. Många av dessa snoRNA har redan kopplats till cancer i andra organ, ibland beteende sig som onkogener eller tumörsuppressorer, och vissa kan direkt förändra stabiliteten eller översättningen av specifika budbärar‑mRNA.
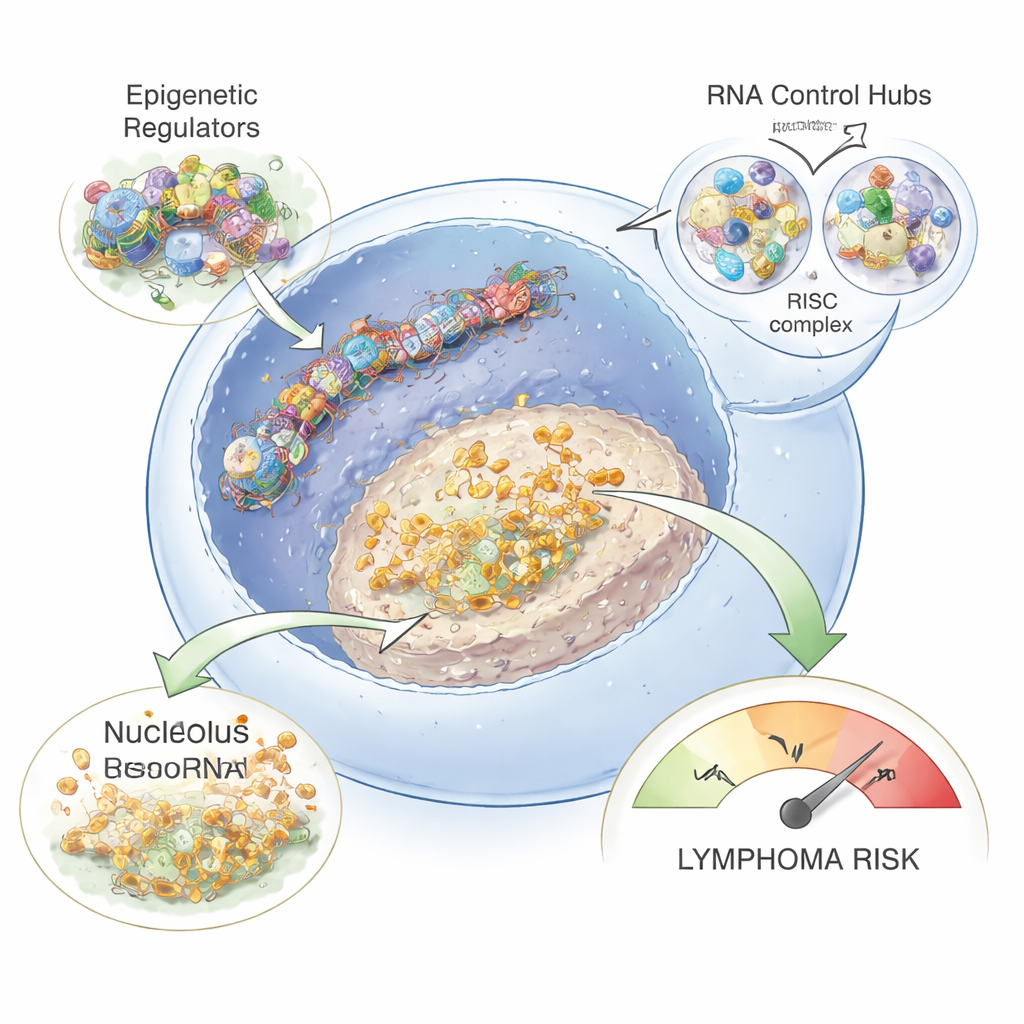
Hur dessa förändringar kan leda till lymfom
Genom att korrelera snoRNA‑nivåer med andra gener visade studien att uppreglerade snoRNA ofta rörde sig i takt med gener involverade i ribosomproduktion och ribonukleoproteinkomplex. Detta tyder på att kronisk hepatitinfektion kan finjustera hur B‑celler bygger ribosomer och bearbetar RNA, vilket potentiellt ändrar vilka proteiner som produceras och i vilka mängder. Tillsammans med överaktiva epigenetiska och microRNA‑styrda system kan dessa skiften skapa en gynnsam miljö för mutationer och felreglerade tillväxtsignaler som slutligen kan driva B‑celler mot lymfom. Även om arbetet ännu inte bevisar direkt infektion av varje enskild B‑cell, detekterade författarna hepatit B‑genetiskt material i åtminstone en patients B‑celler, vilket stöder idén att virusen kan infektera dessa celler och direkt driva några av de observerade förändringarna.
Vad detta betyder för patienter och framtida behandlingar
För icke‑specialister är huvudbudskapet att levervirus kan påverka cancerrisk långt utöver levern genom att subtilt omforma hur immunceller läser sitt DNA och bygger sin interna maskinpark. Studien lyfter fram tre sammanflätade misstänkta — epigenetiska regulatorer, RNA‑tystnadscomplex och snoRNA — som verkar rubbade både i infekterade och cancerösa B‑celler. Dessa vägar kan så småningom ge nya biomarkörer för att identifiera patienter med högre lymfomrisk och nya läkemedelsmål som fungerar både i virusrelaterade och icke‑virusrelaterade former av sjukdomen. För nu stärker fynden argumentet för att förebygga och behandla kronisk hepatit B och D inte bara för att skydda levern, utan också för att värna immunsystemet mot långsiktiga förändringar som kan främja cancer.
Citering: Henning, A.N., Budeebazar, M., Boldbaatar, D. et al. Hepatitis virus-associated B cell non-Hodgkin’s lymphoma involves dysregulated epigenetic and RNA-mediated regulatory gene expression and altered snoRNA transcription. Sci Rep 16, 5003 (2026). https://doi.org/10.1038/s41598-026-35041-3
Nyckelord: hepatit B, hepatit D, B‑cellslymfom, epigenetisk reglering, snoRNA