Clear Sky Science · sv
Strukturell grund för diosgenin som en invers agonist av retinoinsyrareceptor-relaterade föräldralösa receptor γ
Varför en växtförening och en immunomkopplare spelar roll
Många kroniska tillstånd — från autoimmuna sjukdomar som multipel skleros och psoriasis till fetma och typ 2-diabetes — drivs av överaktiva immunsignaler och felaktiga metabola signaler. Forskare har länge sökt säkrare läkemedel som kan vrida upp eller ner dessa signaler med precision. Denna studie undersöker hur diosgenin, ett naturligt molekyl funnet i vissa medicinalväxter och jams, hakar fast vid ett immunreglerande protein kallat RORγ och vänder det till ett mindre aktivt tillstånd. Att förstå denna interaktion på atomnivå kan öppna dörren för mildare, mer riktade terapier byggda på en välkänd växtbaserad stomme.
En huvudregulator för immunitet och ämnesomsättning
RORγ är en del av en stor familj av ”nukleära receptorer” — proteiner inne i celler som slår på eller av gener som svar på små molekyler. Detta särskilda protein är en viktig kontrollpunkt för en grupp immunceller som kallas Th17-celler, vilka producerar den inflammatoriska signalen IL-17A och har kopplats till autoimmuna sjukdomar såsom multipel skleros, psoriasis, reumatoid artrit och Crohns sjukdom. RORγ påverkar också hur fettceller utvecklas och hur kroppen svarar på insulin, vilket knyter det till fetma och diabetes. På grund av detta breda inflytande har RORγ blivit ett attraktivt läkemedelsmål, men många syntetiska molekyler som binder det har stött på problem med säkerhet, selektivitet eller effekt i människa.
En traditionell bot ger ett lovande led
Diosgenin är en steroidliknande molekyl som utvinns från växter, inklusive arter av Dioscorea (vild jams) och flera traditionella medicinalväxter. Den har studerats för antiinflammatoriska, antitumör-, antidiabetiska och kardiovaskulära effekter i cell- och djurmodeller. Tidigare arbete antydde att diosgenin kunde påverka RORα/γ-vägen och dämpa skadliga Th17-responser, men det var oklart om den berörde RORγ direkt eller hur den kunde forma proteinets beteende. För att besvara det screenade författarna ett bibliotek av naturliga föreningar med ett känsligt bindningsprov och identifierade diosgenin som en stark bindare till RORγ:s ligandbindande region.
Hur diosgenin pressar RORγ i motsatt riktning
Forskarna undersökte hur diosgenin påverkar RORγ:s förmåga att rekrytera hjälpproteiner som antingen förstärker (koaktivatorer) eller dämpar (korepressorer) genaktivitet. Överraskande nog uppmuntrade diosgenin RORγ att binda båda typer av partner, ett mönster som skiljde sig från en känd naturlig antagonist kallad ursolsyra. I cellbaserade reporter‑tester som följer genreglering sänkte diosgenin konsekvent RORγ‑driven aktivitet på ett dosberoende sätt, med potens i sub‑mikromolär nivå. Detta beteende stämmer med profilen för en ”invers agonist”: en förening som inte bara blockerar baslinjeaktivitet utan aktivt driver receptorn mot ett avstängt tillstånd, även när den annars skulle vara påslagen.
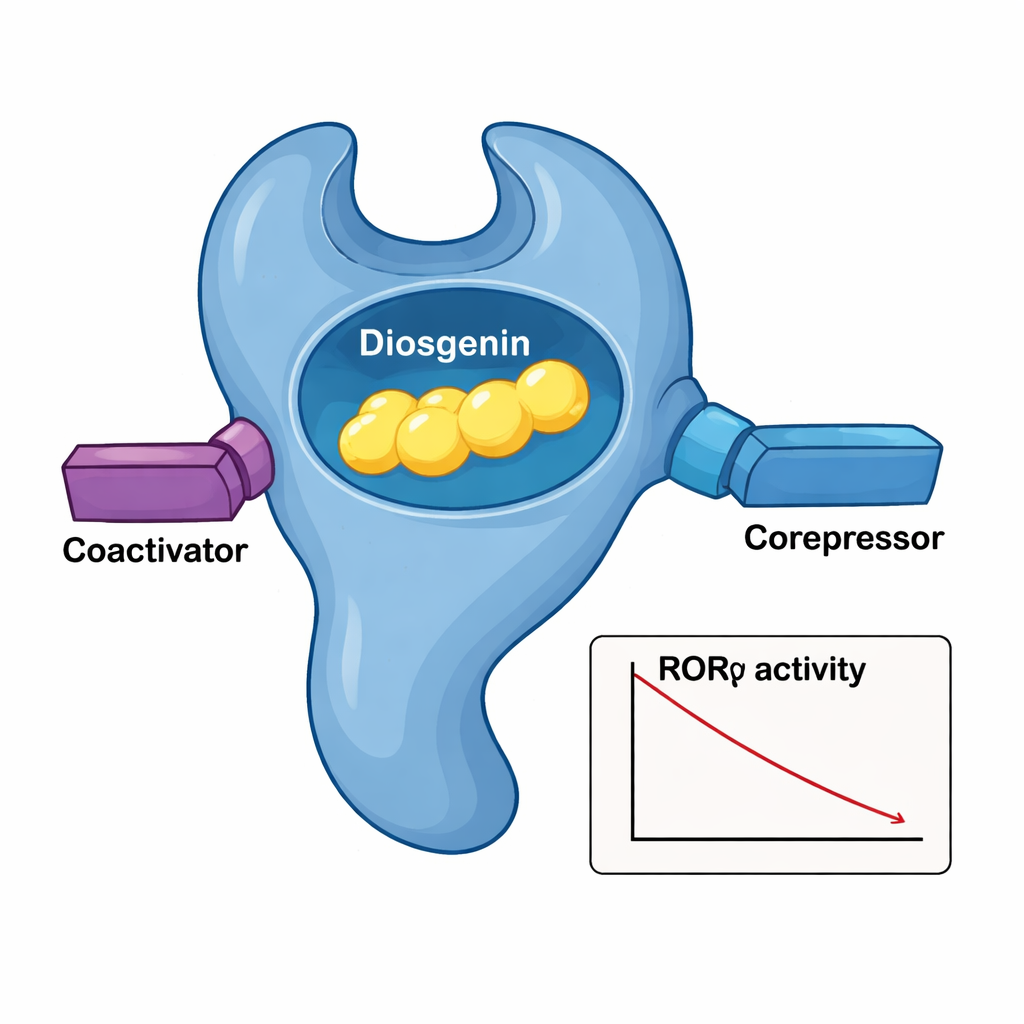
En närbild av det molekylära handslaget
För att se exakt hur diosgenin passar in i RORγ löste teamet den tredimensionella kristallstrukturen av proteinets ligandbindande domän med diosgenin inlagrad. Receptorn veckar sig till ett lager av helixar som bildar en ficka som vaggar diosgenins steroidlika kropp. Ett nätverk av täta hydrofoba kontakter från flera aminosyror fungerar som en skräddarsydd handske runt molekylens ryggrad, medan en kritisk hydroxylgrupp på diosgenin bildar vattenmedierade vätebindningar med två argininrester. När dessa fickresiduer förändrades en efter en minskade diosgenins förmåga att tysta RORγ, vilket bekräftade deras betydelse. Strukturella jämförelser med RORγ–ursolsyra‑komplexet visade att diosgenin håller en nyckelhelix i svansen (AF‑2) i en ”aktiv‑lik” position samtidigt som det fortfarande driver den övergripande transkriptionen nedåt, vilket förklarar varför det samtidigt kan dra till sig både koaktivatorer och korepressorer.
Från kristallstruktur till framtida läkemedel
Den detaljerade bilden av diosgenin–RORγ‑interaktionen framhäver två anmärkningsvärda fördelar för läkemedelsdesign. För det första visar receptorfickan tillräcklig flexibilitet för att känna igen olika ligandskador, vilket innebär att kemister kan finslipa diosgenins stomme för att förbättra selektiviteten för RORγ och minska oönskad bindning till andra nukleära receptorer. För det andra gör diosgenins naturliga ursprung och kända låga inneboende toxicitet i prekliniska modeller det till en attraktiv utgångspunkt jämfört med några helt syntetiska föreningar som stannat av i kliniska prövningar. Enkelt uttryckt visar detta arbete hur en växt‑härledd molekyl kan haka fast vid en central immunologisk och metabolisk omkopplare och trycka den i motsatt läge, vilket erbjuder en strukturell mall för att utveckla säkrare, mer effektiva behandlingar för RORγ‑relaterade sjukdomar.
Citering: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Nyckelord: ROR gamma, diosgenin, autoimmun sjukdom, nukleär receptor, invers agonist