Clear Sky Science · sv
Transkriptomisk karaktärisering av aberrant alternativ splitsning i skelettmuskler hos patienter med sarkopeni
Varför åldrande muskler förlorar sin styrka
Sarkopeni — den gradvisa förlusten av muskelmassa och styrka med åldern — är en av huvudorsakerna till att äldre får svårare med vardagliga sysslor, från att gå i trappor till att bära matkassar. Denna studie gräver in i åldrande muskel på RNA‑nivå, de budskap som talar om för cellerna vilka proteiner de ska tillverka. Författarna visar att vid sarkopeni klipps och sys många av dessa RNA‑budskap ihop på onormala sätt, vilket potentiellt stör energiproduktionen i muskeln och pekar på nya behandlingsmål.
Muskelförlust och kroppens gen‑”redigerings”system
Våra gener är skrivna i DNA, men cellerna arbetar utifrån RNA‑kopior av dessa gener. Innan ett RNA‑budskap används trimmar och splicar cellerna det normalt — ungefär som att redigera en film — så att en gen kan producera flera varianter av ett protein. Denna process, kallad alternativ splitsning, är särskilt aktiv i muskel, som behöver finstämda proteiner för att kontrahera, reparera och anpassa sig vid träning. När splitsningen går fel kan fel proteinvarianter produceras eller viktiga varianter gå förlorade, vilket bidrar till sjukdomar såsom muskeldystrofi och vissa hjärnsjukdomar. Författarna misstänkte att ett liknande dolt lager av RNA‑felredigering kan driva sarkopeni.
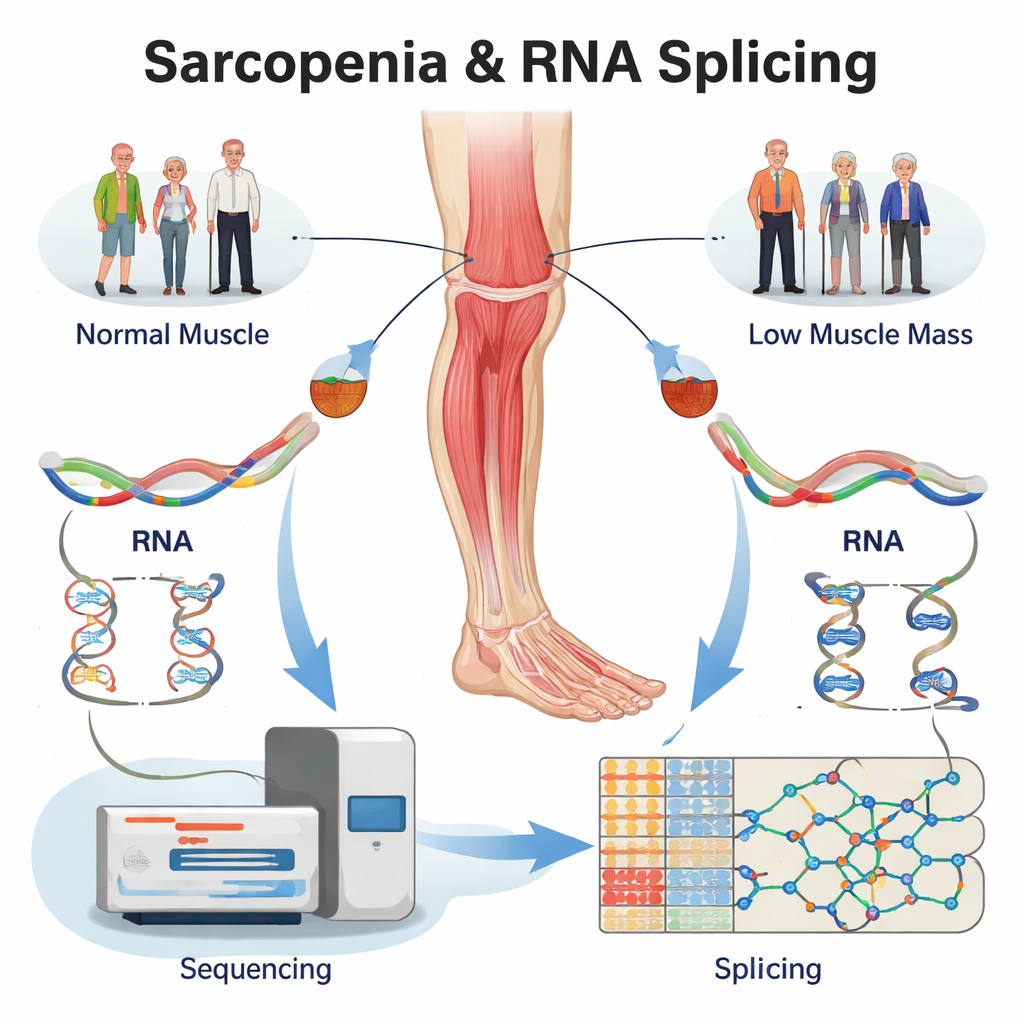
Omläsning av befintliga data för att hitta dolda RNA‑fel
I stället för att rekrytera nya försökspersoner gjorde teamet en ny analys av en befintlig stor RNA‑sekvenseringsdatamängd från mänskliga biopsier av lårmuskulatur. Proverna kom från fyra grupper: äldre vuxna med fullt utvecklad sarkopeni, personer med endast låg muskelmassa, personer med endast nedsatt muskelstyrka och åldersmatchade friska kontroller. Med specialiserad programvara bekräftade de först att hundratals gener var upp- eller nedreglerade i de sjuka musklerna. Viktigare var att de sedan undersökte hur varje gens RNA splicades och katalogiserade mer än 5 000 förändringar i splitsningen i de tre problemgrupperna jämfört med frisk muskel. Dessa förändringar koncentrerades till några grundläggande typer — som att hoppa över en exon eller välja en alternativ klippningsplats — mönster som är kända för att starkt påverka proteinstruktur.
Energifabriker och cellernas ”bränslemätare” rubbas
De upptäckta splitsningsförändringarna återfanns i gener som ligger i hjärtat av muskelfysiologin. Många påverkade gener bygger delar av mitokondrierna, de små energifabriker som driver muskelkontraktion. I sarkopenisk muskel visade 16 gener involverade i oxidativ fosforylering — processen som omvandlar näringsämnen till användbar energi — förändrad splitsning, särskilt komponenter i mitokondriella komplex som hanterar elektrontransport och protonpumpning. Andra förändringar syntes i gener som tillverkar eller använder NAD⁺, en nyckelmolekyl för cellulär energi och reparation. Istället för att bara vara mer eller mindre rikliga producerade viktiga enzymer såsom CD38, PARP2 och flera sirtuiner olika RNA‑varianter, vilket tyder på att balansen mellan NAD⁺‑produktion och konsumtion är störd på splitsningsnivå. De påverkade generna samlades också i välkända muskel‑signalvägar, inklusive AMPK‑ och FoxO‑vägarna, som fungerar som cellulära bränslemätare och stressresponser.
Delade mönster i olika skeden — och hos olika arter
Slående nog visade många av samma gener förändrad splitsning inte bara hos personer med full sarkopeni, utan också hos dem som endast hade låg muskelmassa eller endast nedsatt styrka. Det tyder på att onormal splitsning börjar tidigt och genomsyrar de olika kliniska ansiktena av sjukdomen. För att testa om dessa förändringar kunde reproduceras i en djurmodell inducerade forskarna muskelförtvining hos möss med steroiden dexametason, en standardmetod för att efterlikna vissa drag av sarkopeni. Mössen utvecklade svagare greppstyrka och sämre prestation i löp‑ och balansprov. När teamet sekvenserade muskel‑RNA från mössen fann de återigen hundratals gener med förändrad splitsning. Ungefär en femtedel av dessa överlappade med de mänskliga sarkopenigenerna, och många var involverade i kontroll av transkription, kromatinstruktur och själva splitsningen — högre nivåns strömbrytare som kan omforma cellens hela proteinutbud.
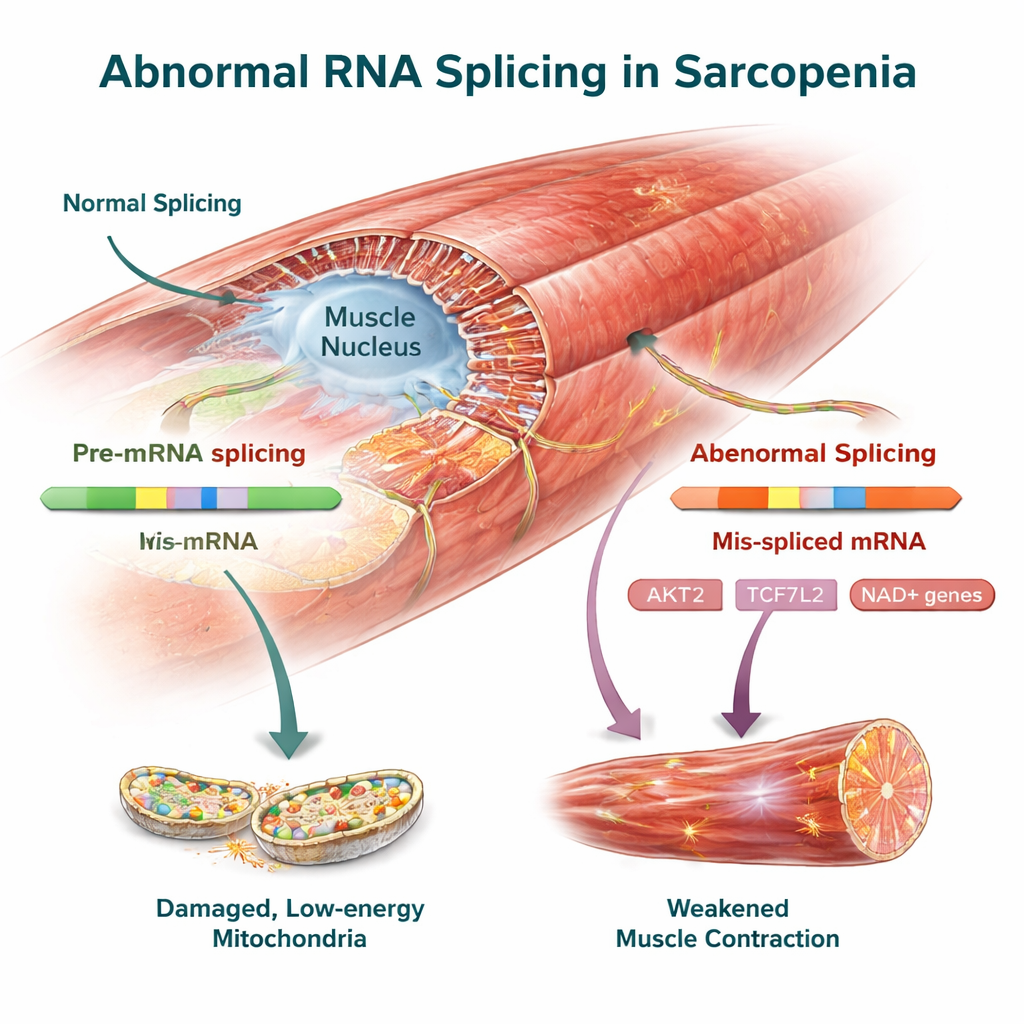
Nyckelgener för muskelkontroll som potentiella behandlingsmål
Bland de över artgränserna förändrade generna fanns flera som redan kopplats till muskelhälsa. AKT2, en central regulator för tillväxt och proteinsyntes i muskel, visade tydliga förändringar i splitsning både hos människor och möss som kan dämpa dess förmåga att upprätthålla muskelmassa. TCF7L2, en del av Wnt‑signaleringen, tillsammans med FMNL2 och USP40, som hjälper till att organisera muskels inre stomme och protein‑kvalitetskontroll, hade också förändrade RNA‑varianter. Teamet bekräftade dessa splitsningsförändringar experimentellt i muskel från möss, vilket stärker fallet att de är verkliga kännetecken för sjukdomen snarare än artefakter från dataanalysen.
Vad detta innebär för att förebygga skörhet
För icke‑specialister är budskapet att sarkopeni inte bara handlar om att muskler ”slits ut” eller att gener slås på eller av. Det innebär också en utbredd felredigering av RNA‑budskap som styr hur muskelceller bygger och underhåller sina maskiner, särskilt systemen som genererar energi och känner av stress. Eftersom splitsning i princip kan korrigeras med noggrant designade RNA‑baserade läkemedel, erbjuder de bevarade splitsningsfelen som upptäckts här — särskilt i gener som AKT2 och TCF7L2 — en ny uppsättning spår för terapier som kan hjälpa åldrande muskler att förbli starkare längre.
Citering: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Nyckelord: sarkopeni, muskelåldrande, RNA‑splitsning, mitokondrier, AKT2