Clear Sky Science · sv
Fenomenologisk modell för stabilisering av transthyretin
Varför detta är viktigt för patienter och familjer
Transthyretin-amyloidos är ett allvarligt tillstånd där ett normalt blodprotein, transthyretin (TTR), faller isär och dess delar kan klumpa ihop sig till skadliga avlagringar i hjärtat och nerverna. Nya läkemedel som tafamidis och acoramidis är utformade för att hålla detta protein i dess säkra, fyrdelade form, och de har redan förbättrat utfallen för många människor. Ändå ser läkare en förbryllande effekt hos behandlade patienter: blodnivåerna av TTR stiger med mer än 30 %, och det är inte uppenbart varför. Denna artikel använder en avskalad, matematiskt baserad modell för att utforska vad som kan hända i kroppen och vad det innebär för hur dessa läkemedel verkligen verkar. 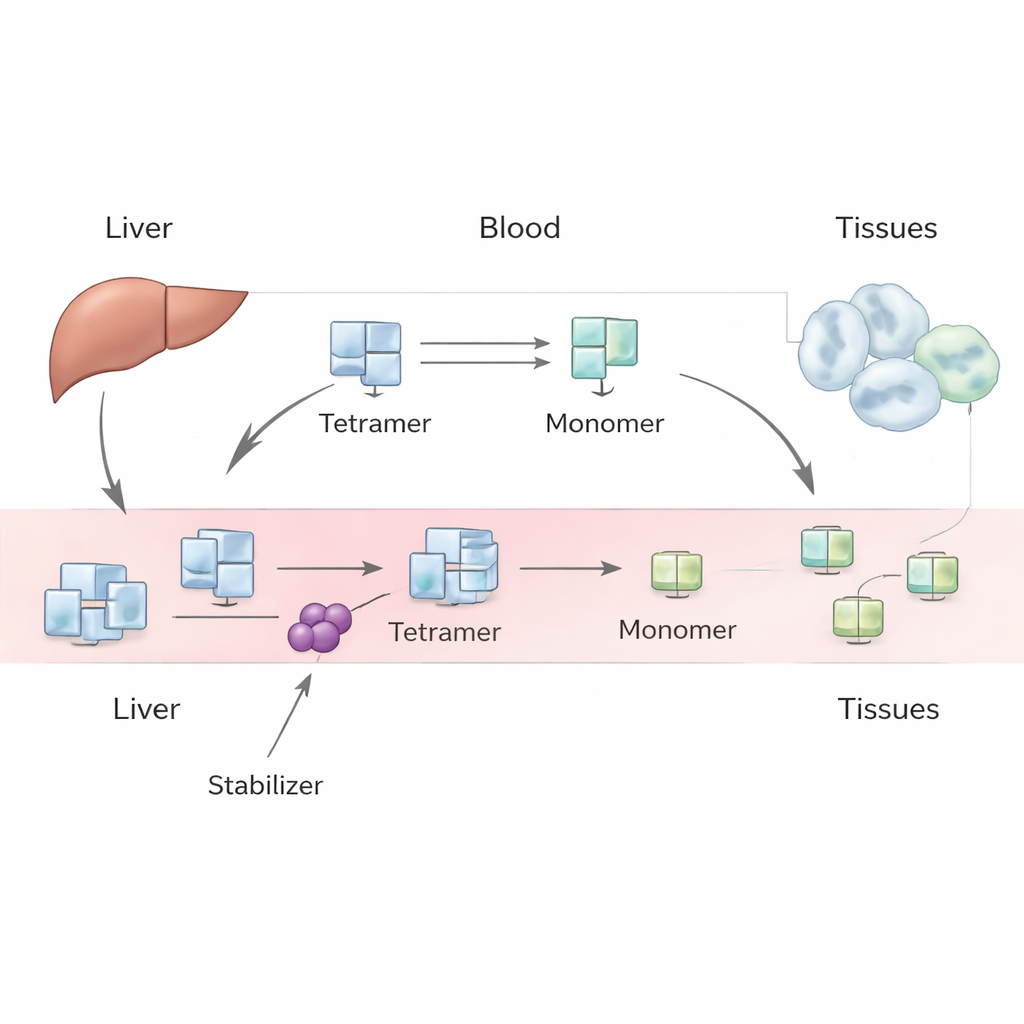
Ett protein som kan hjälpa eller skada
TTR bildas huvudsakligen i levern och cirkulerar normalt i blodet som en stabil bunt av fyra identiska subenheter, känd som en tetramer. Det transporterar sköldkörtelhormon och vitamin A. Under vissa förhållanden, inklusive åldrande eller ärftliga genvarianter, kan denna tetramer falla isär till enskilda subenheter, eller monomerer. Dessa monomerer kan felveckas och fastna ihop som amyloidfibriller, vilket skadar vävnader och leder till transthyretin-amyloidos i hjärtat (kardiomyopati) eller nerverna (neuropati). Läkemedel som tafamidis och acoramidis är utformade för att binda tetrameren och göra det svårare för den att gå sönder, vilket bromsar sjukdomsprogressionen. Trots detta stiger de uppmätta TTR-nivåerna i blodet hos patienter som påbörjar dessa läkemedel på ett tillförlitligt sätt, och denna ökning är större än vad enkla laboratorieexperiment skulle förvänta sig.
Att bygga en enkel bild av ett komplext system
Författarna angriper detta pussel med en fenomenologisk modell—en som fokuserar på övergripande observerbart beteende snarare än varje mikroskopiskt detalj. I deras ramverk producerar levern TTR-tetramerer i en jämn takt, som sedan går ut i blodomloppet. Väl i cirkulationen kan tetramerer dissociera till monomerer och återmonteras, och både tetramerer och monomerer kan tas bort från blodet genom upptag i vävnader och nedbrytning. Genom att skriva ner ett par massbalans-ekvationer för tetramerer och monomerer utforskar teamet olika scenarier: ett där monomerer mestadels återförenas till tetramerer, ett där de snabbt avlägsnas, och ett mellanläge där båda processerna spelar roll. De använder historiska mänskliga tracer-studier och moderna laboratoriedata för att uppskatta nyckelkvantiteter, såsom hur snabbt tetramerer rensas, hur snabbt de faller isär och hur starkt läkemedel bromsar denna sönderdelning.
Varför stabilisering av tetrameren ensam inte räcker
Försedda med dessa uppskattningar ställer forskarna en riktad fråga: om ett läkemedel skulle kunna helt förhindra att tetramerer går sönder, hur mycket skulle blodnivån av TTR då öka? Över alla rimliga regimer är svaret måttligt—i storleksordningen högst cirka 15 % för typiska parametervärden, och ofta mindre beroende på hur monomerer hanteras. Detta ligger långt ifrån den >30 % ökning som observerats hos behandlade patienter. Avvikelsen kvarstår även om man tillåter generösa osäkerheter i de kända parametrarna. Modellen antyder därför att enbart att bromsa tetramer-sönderdelning inte kan förklara den fulla kliniska effekten. Andra processer som styr hur snabbt TTR produceras, tas upp av celler eller bryts ner måste också förändras när stabiliserande läkemedel är närvarande. 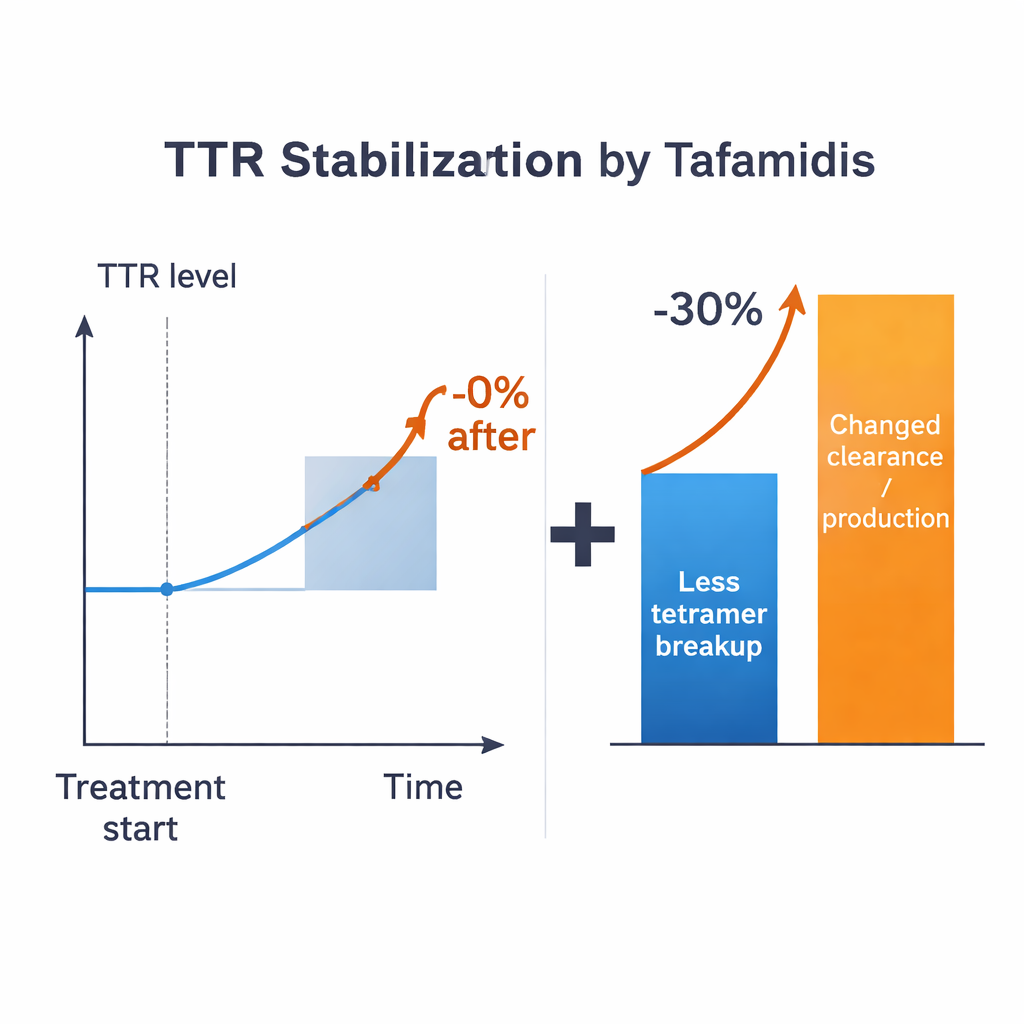
Ledtrådar från läkemedelsnivåer och smarta experiment
För att koppla läkemedelsexponering till TTR-beteende kombinerar författarna en grundläggande farmakokinetisk modell för tafamidis (hur läkemedlet rör sig i kroppen över tid) med specialiserade ”subenhetsutbytes”-assay. I dessa experiment blandas märkta och omärkta TTR-tetramerer i humant plasma, och den gradvisa utbytet av subenheter avslöjar hur ofta tetramerer faller isär. Att mäta denna process vid olika läkemedelskoncentrationer ger en direkt, datadriven länk mellan tafamidisnivå och effektiv tetramerstabilitet, utan att behöva veta hur mycket läkemedel som är bundet till albumin eller sköldkörtelhormon. Denna fenomenologiska koppling matar in i modellen och kringgår många biokemiska okända faktorer på ett elegant sätt. Ändå, även med denna fördel, begränsar beräkningarna fortfarande den förväntade ökningen av TTR till ungefär hälften av den kliniskt observerade ökningen, vilket förstärker idén att förändringar i clearance, internalisering, nedbrytning eller även syntes måste vara en del av förklaringen.
Vad detta betyder framöver
För icke-specialister är huvudbudskapet att dessa stabiliserande läkemedel sannolikt gör mer än att bara ”limma” ihop TTR-tetramerer. De påverkar troligen också hur kroppen producerar, avlägsnar eller återvinner proteinet. Författarna menar att enkla, transparenta modeller som deras är kraftfulla eftersom de blottlägger sådana kunskapsluckor och pekar på konkreta experiment—for exempel att direkt mäta hur snabbt monomerer rensas, hur snabbt olika TTR-former tas upp av celler, eller om läkemedelsbundet TTR hanteras annorlunda än obundet protein. Bättre svar på dessa frågor skulle inte bara förfina behandlingen av transthyretin-amyloidos utan kan också avslöja generella principer om andra sjukdomar där normala proteiner förvandlas till skadliga aggregat.
Citering: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Nyckelord: transthyretin-amyloidos, proteinstabilisering, tafamidis, farmakokinetisk modellering, amyloidsjukdomar