Clear Sky Science · sv
Målinriktad stabilisering av hypoxiinducerbart faktor 1-alfa (HIF1A) under in vitro-mognad av bovina kumulus-oocytkomplex ökar blastocystfrekvenser
Varför justering av syresensing i ägg spelar roll
Modern nötkreatursavel förlitar sig i hög grad på laboratorieframställda embryon, men framgången är långt ifrån säker: endast ungefär en tredjedel av äggcellerna når den avgörande blastocyststadiet, då de är redo att överföras till en ko. Denna studie ställer en förrädiskt enkel fråga med bred betydelse för djuravel och assisterad reproduktion: om vi efterliknar de låga syrgasförhållanden som ägg naturligt upplever i äggstocken mer noggrant — genom att varsamt öka en nyckelprotein för syrgassensing — kan vi då få fler embryon att utvecklas framgångsrikt?
Livet börjar i ett lågt syrgasnisch
Inne i äggstocken är varje utvecklande ägg omslutet av en stödjande cellklunga känd som kumulus, tillsammans bildande ett kumulus–oocytkomplex. Även om äggstocken får rikligare blodtillförsel när folliklar växer, når blodkärlen inte ända fram till äggets omedelbara omgivning. Syre måste diffundera in och skapar en svagt låg-syre, eller hypoxisk, ficka runt det mognande ägget. I denna nisch hjälper en intracellulär sensor kallad HIF1A cellerna att anpassa sig genom att justera ämnesomsättning och hormonproduktion. Tidigare arbete visade att blockering av HIF1A skadar äggmognaden och drastiskt minskar embryobildning, vilket lyfter fram detta protein som en central samordnare av äggets kompetens — förmågan hos ett ägg att bli befruktat och utvecklas till ett friskt embryo.
Använda ett läkemedel för att finjustera äggets syrgassensor
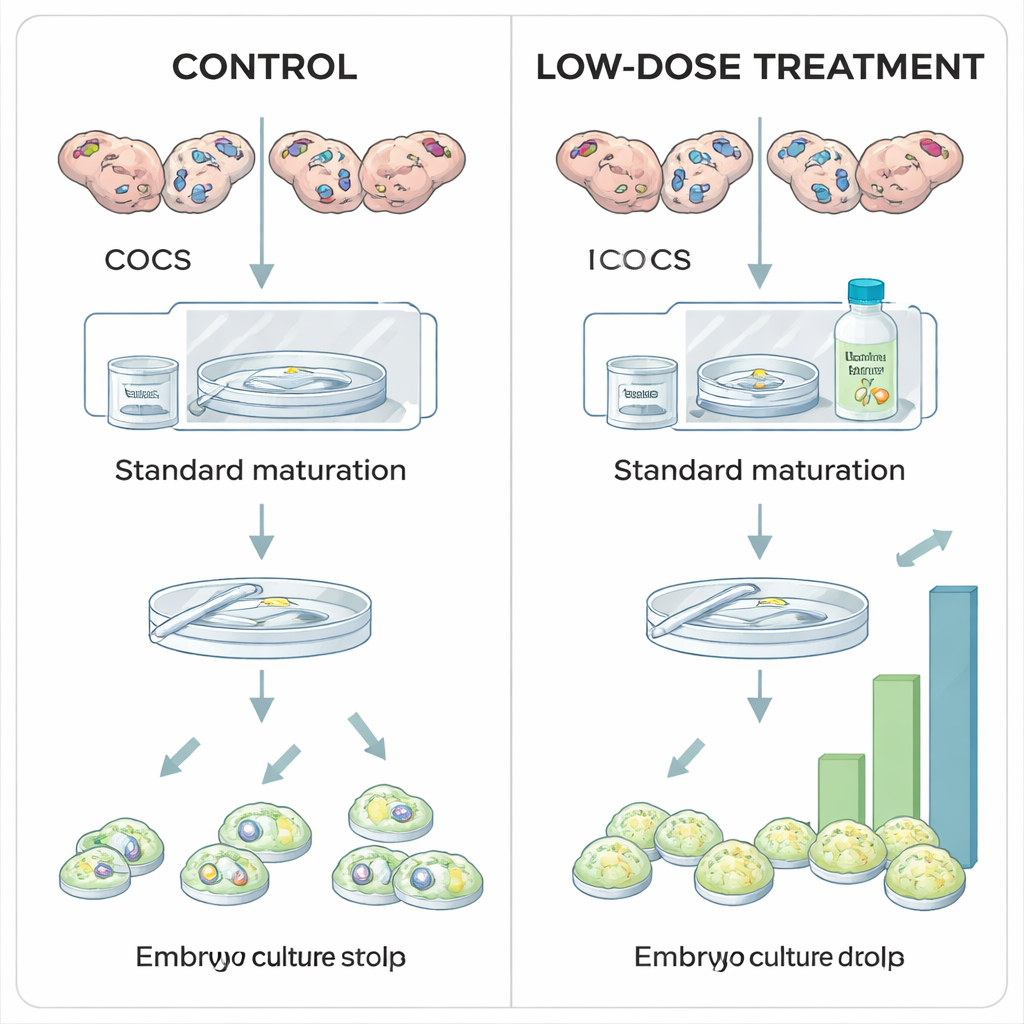
Forskarna undersökte om måttlig stabilisering av HIF1A under laboratoriemognad av bovina ägg kunde öka embryoutbytet. I standardprotokoll för in vitro-mognad utsätts kumulus–oocytkomplex för normala luftsyrenivåer, i stor utsträckning av praktiska skäl snarare än biologiska. Här delades ägg insamlade från slaktade djurs äggstockar in i grupper och exponerades under sin 24-timmarsmognadsperiod för olika doser av Roxadustat, ett läkemedel som redan används i humanmedicin för behandling av anemi. Roxadustat fungerar genom att blockera en familj enzymer som kallas prolyl-hydroxylaser (PHDs) som normalt märker HIF1A för nedbrytning när syre är rikligt. Genom att hämma PHDs tillåter Roxadustat att HIF1A-protein ackumuleras även vid högre syrgashalt, vilket delvis återskapar den hypoxiska signal ägget skulle uppfatta in vivo.
Fler blastocyster vid rätt dos, skada vid högre nivåer
När teamet undersökte hur ägg och embryon klarade sig efter behandling framträdde ett tydligt mönster. En låg dos Roxadustat (25 mikromolar) förändrade inte hur många ägg som slutförde mognaden eller hur många befruktade ägg som började dela sig, men den ökade signifikant andelen som nådde blastocyststadiet. Med andra ord påverkades inte de tidiga stegen, ändå lyckades fler embryon fullfölja den krävande resan till blastocyststadiet — vilket tyder på att måttlig HIF1A-stabilisering förbättrar äggets inneboende kvalitet. Däremot minskade den högsta dosen (100 mikromolar) andelen ägg som överhuvudtaget mognade, och när samma hämmare applicerades senare, under den åtta dagar långa embryokulturen, sänkte höga doser kraftigt blastocystbildningen utan att påverka tidig celldelning. Dessa fynd indikerar att "lagom" HIF1A-aktivitet under mognaden är fördelaktigt, medan för mycket eller för långvarig aktivering är skadligt.
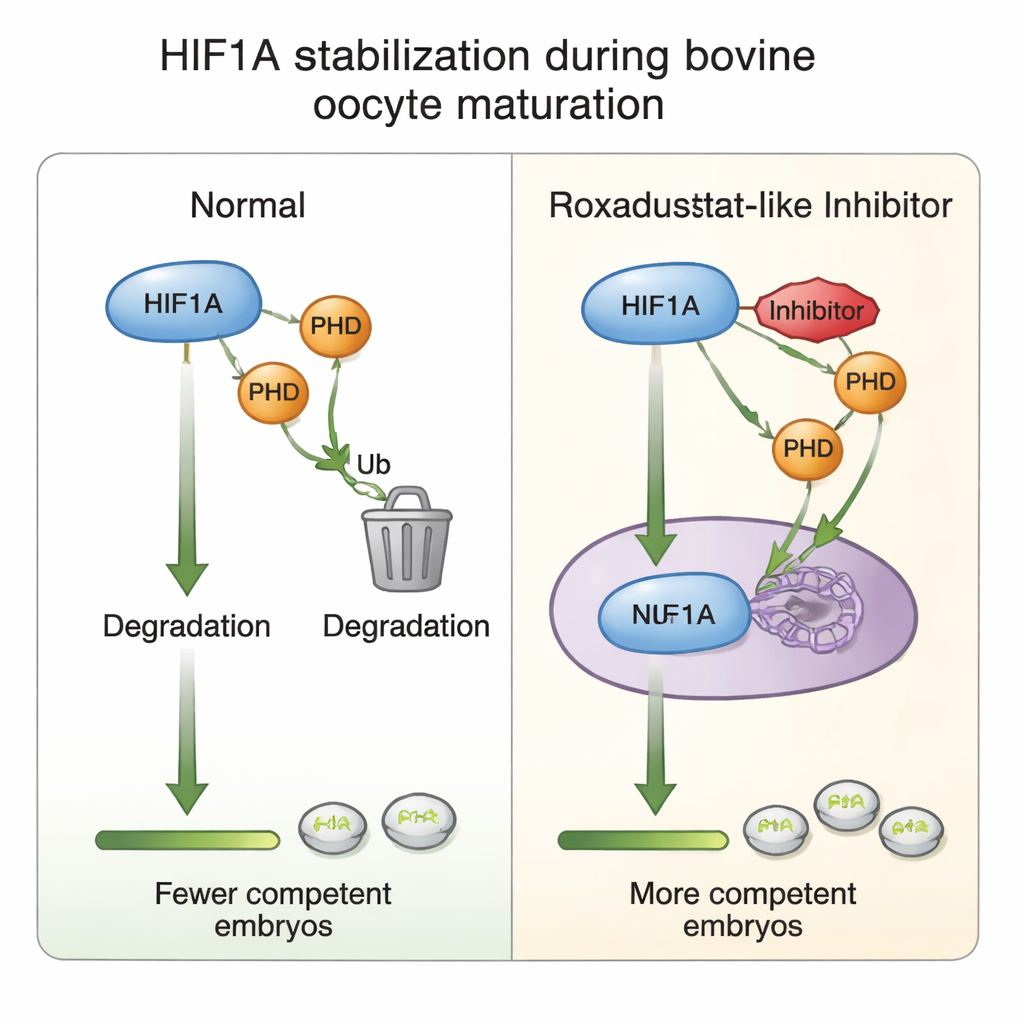
Vad som sker inne i äggets stödjeceller
För att förstå hur denna kemiska fininställning fungerar undersökte författarna kumuluscellerna som omsluter varje ägg. De fann att mognad i allmänhet ökar HIF1A-gens aktivitet, men att tillsats av Roxadustat paradoxalt nog sänkte HIF1A-messenger-RNA samtidigt som HIF1A-proteinnivåerna förblev stabila — en ledtråd att cellerna kan dämpa genuttrycket när proteinet är tillräckligt stabiliserat, en slags inbyggd broms mot överaktivering. Nivåerna av PHD2, det mest syrekänsliga av PHD-enzymerna, ökade som svar på läkemedlet, vilket förstärker dess roll som en del av syresensorns återkopplingsslinga. Vid högre läkemedelsdoser minskade markörer för cellproliferation och för den klibbiga matris som hjälper kumulusceller att expandera runt ägget, i linje med den observerade nedgången i mognad och embryobildning. Allt detta stödjer idén att noggrant balanserad HIF1A-aktivitet finjusterar dialogen mellan ägg och kumulusceller som ligger till grund för senare utvecklingsframgång.
Konsekvenser för djuravel och bortom
Detta arbete visar att en varsam stabilisering av äggets syrgassensor under det korta fönstret av in vitro-mognad kan avsevärt öka och stabilisera blastocystutfallet hos nötkreatur, utan att förändra befruktning eller tidig klyvning. I praktiska termer kan det översättas till mer pålitlig embryoproduktion för avelsprogram, med ett målinriktat läkemedel snarare än grova förändringar i syrgashalt eller mer giftiga kemikalier. Studien understryker också en bredare lärdom relevant för mänskliga fertilitetsbehandlingar: att efterlikna den nyanserade, lågsyriga miljön i äggstocken handlar inte bara om att höja eller sänka syre, utan om att respektera den känsliga balansen av signalsubstanser som HIF1A. Att finjustera den balansen, snarare än att driva den till ytterligheter, kan vara en nyckelväg till friskare embryon.
Citering: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Nyckelord: in vitro-embryoproduktion, oocytmognad, hypoxisignalering, HIF1A-stabilisering, nötkreatursreproduktion