Clear Sky Science · sv
In vivo-visualisering av extracellulära adenosindynamiker i hjärtat och dess farmakologiska modulering i zebrafiskmodeller för hjärtsvikt
Varför den här historien om ett fiskhjärta är viktig
Hjärtsvikt är fortfarande en av de ledande dödsorsakerna i världen och många patienter försämras trots dagens bästa läkemedel. Forskare vet att stressade hjärtceller utsöndrar kemiska "nöd-signaler" i sin omgivning, men det har varit svårt att iaktta dessa signaler i aktion inne i ett slagande hjärta. Denna studie använder transparenta zebrafiskar, vars små hjärtan efterliknar viktiga drag hos mänskliga hjärtan, för att observera dessa farosignaler i realtid och pröva ett nytt sätt att dämpa dem.
Signaler från ett kämpande hjärta
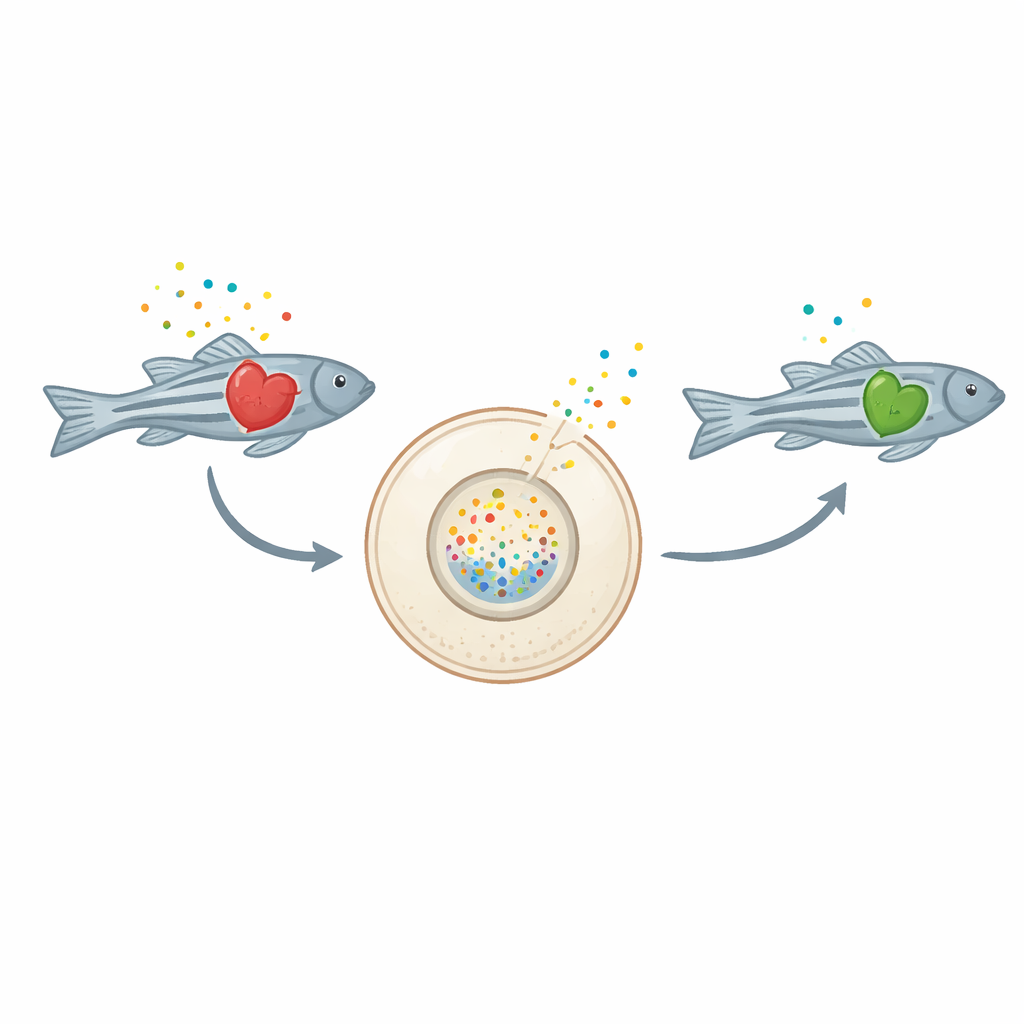
När hjärtceller skadas släpper de ut energibärande molekyler som ATP och dess nedbrytningsprodukt adenosin ut i det extracellulära rummet. Utanför cellen slutar dessa molekyler att fungera som bränsle och beter sig istället som angelägna budskap som kan elda på inflammationen. Vid kronisk hjärtsvikt kan den inflammatoriska responsen bli överaktiv och skada hjärtat ytterligare. Fram till nu har forskare saknat direkt, in vivo-bevis för hur dessa molekyler beter sig över tid i ett sviktande hjärta.
Att göra zebrafiskar till levande kemiska kameror
Forskargruppen konstruerade zebrafiskar vars hjärtceller uttrycker ett speciellt fluorescerande sensorprotein kallat GRABAdo på sin yta. När adenosin ansamlas utanför cellerna lyser sensorn starkare grönt och förvandlar varje litet hjärta till en egen levande kemisk kamera. Forskarna framkallade sedan hjärtsvikt i zebrafiskar med terfenadin, ett läkemedel känt för att störa hjärtrytmen och försvaga pumpfunktionen. När fiskarna utvecklade tydliga tecken på hjärtsvikt — långsammare hjärtslag, förstorade och svagare kammare, svullnad runt hjärtat och sämre simförmåga — tändes hjärtsensorerna och avslöjade en markant ökning av extracellulärt adenosin. Kemiska mätningar av hela larver bekräftade att de totala adenosinnivåerna var högre i de sviktande hjärtana.
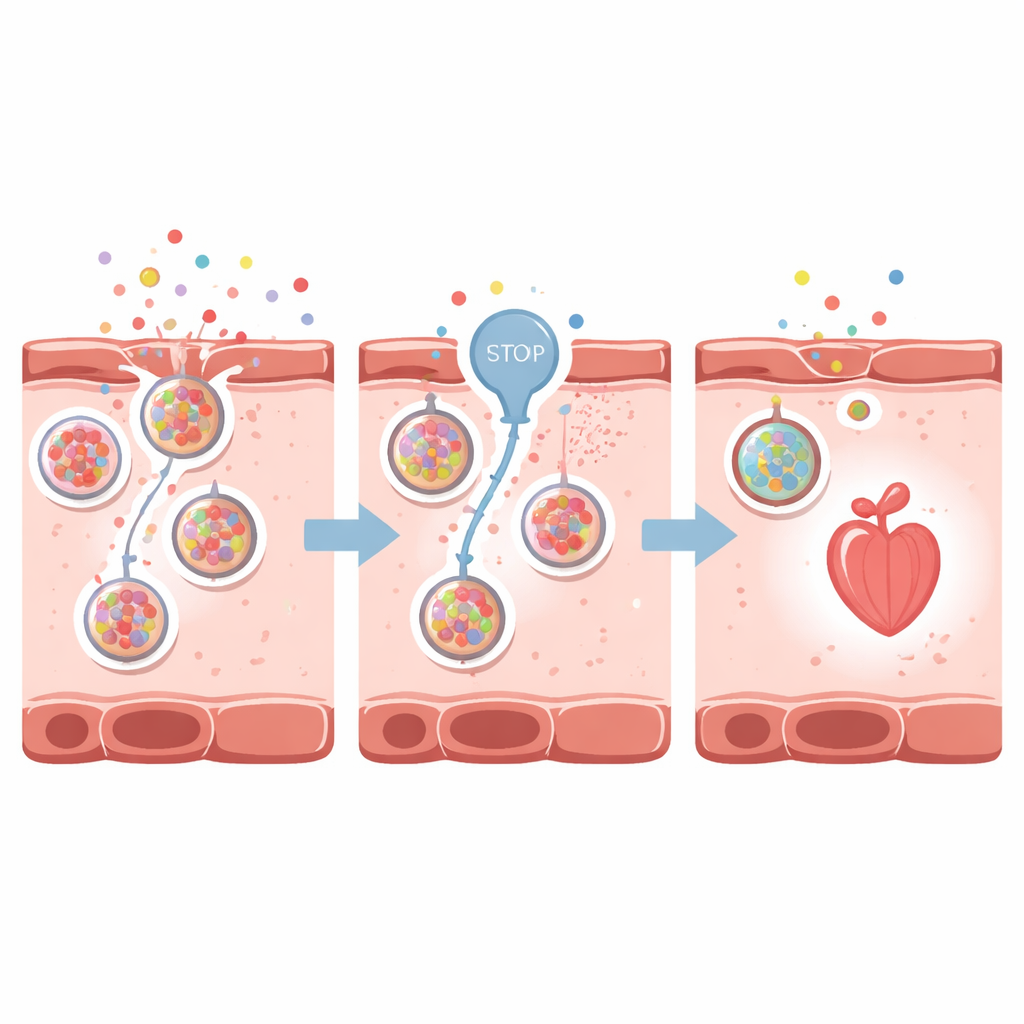
Blockera utlösningsventilen
Forskarna frågade sedan om dämpning av dessa farosignaler kunde skydda hjärtat. De fokuserade på VNUT, en transportör som fyller ATP i små cellulära blåsor (vesiklar) för utsöndring utanför cellen. Med hjälp av klodronat, ett läkemedel som blockerar VNUT, minskade de ATP-utsöndringen och därigenom indirekt adenosinansamlingen runt hjärtcellerna. Hos zebrafiskar med läkemedelsinducerad hjärtsvikt bevarade VNUT-hämning hjärtats form, minskade kammarvidgning, förbättrade hjärtfrekvens och pumpkraft samt bibehöll bättre blodflöde. Den fluorescerande adenosinsensorn bleknade, vilket visade att mindre av nödsignalen fanns utanför cellerna. Liknande skyddande effekter observerades i adulta zebrafiskar med en akut, snabbt utvecklande form av hjärtsvikt.
Flera skyddande spakar som samverkar
Hjärtsvikt involverar mer än en väg, så forskarna testade hur VNUT-blockad interagerar med andra kända aktörer. Läkemedel som blockerar vissa adenosinreceptorer och ATP-receptorer, liksom en förening som begränsar passiv ATP-läckage genom membrankanaler, hjälpte var och en zebrafiskhjärtana. När dessa behandlingar kombinerades med VNUT-hämning gav många av dem additiva fördelar, vilket antyder att dämpning av purinsignalering på flera punkter kan vara särskilt effektivt. VNUT-hämning bidrog också till att återställa kalciumbalansen i hjärtcellerna — avgörande för normalt hjärtslag — och minskade både celldöd och aktiviteten av gener kopplade till inflammation. Tillsammans målar dessa resultat upp VNUT som en central switch som länkar ATP-frisättning, inflammation, störd kalciumhantering och progressiv hjärtskada.
Från akvarier till framtida terapier
För icke-specialister är huvudbudskapet att studien direkt visualiserar en kemisk stressignal som stiger i sviktande hjärtan och visar att blockering av dess utsläpp kan skydda hjärtfunktionen i ett levande djur. Även om zebrafiskhjärtan är enklare än mänskliga hjärtan delar de tillräckligt med biologiska likheter för att fungera som ett kraftfullt testfält för nya idéer. Genom att identifiera VNUT som ett lovande mål i skärningspunkten mellan inflammation och elektrisk instabilitet antyder arbetet att framtida behandlingar av hjärtsvikt kan göra mer än att stödja blodflödet — de kan aktivt dämpa skadliga cellulära samtal som driver hjärtat mot svikt.
Citering: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Nyckelord: hjärtsvikt, adenosinsignalering, zebrafiskmodell, inflammation, hjärtskydd