Clear Sky Science · sv
Matcher helgenomsekvensering av blod (10×) och fem enskilda spermier (1×) per individ hos 53 män
Varför denna studie är viktig för familjer
För många par som har svårt att bli gravida hamnar fokus ofta på hormonnivåer eller allmän hälsa, medan de finare detaljerna inne i spermierna förblir ett mysterium. Denna studie öppnar ett nytt fönster mot de detaljerna genom att noggrant läsa hela DNA:t både från blod och från enskilda spermier hos tiotals män. Genom att kombinera denna genetiska information med precisa mätningar av spermiernas rörelse har forskarna skapat en delad resurs som kan hjälpa vetenskapsmän världen över att bättre förstå manlig infertilitet och så småningom förbättra diagnostik och behandling.
Nära granskning av rörliga och slöa spermier
Män kan vara infertila av många skäl, men ett av de vanligaste är asthenozoospermi—ett tillstånd där spermier är levande men rör sig för långsamt eller svagt för att nå och befrukta ett ägg. I det här projektet rekryterade teamet 53 han-kinesiska män: 37 med typisk spermiekvalitet och bevisad fertilitet, och 16 vars spermier hade dålig rörlighet men normalt antal. Alla deltagare screenades noggrant för att utesluta andra medicinska problem och nylig COVID-19-infektion, så att skillnader i spermierörelse inte skulle förväxlas med orelaterade sjukdomar. För varje man registrerades en rik uppsättning hälsouppgifter, inklusive ålder, kroppsstorlek, rök- och alkoholvanor, reproduktionshistoria, hormonnivåer och ett brett spektrum av spermieparametrar såsom total rörlighet, simhastighet och rörelsemönster.
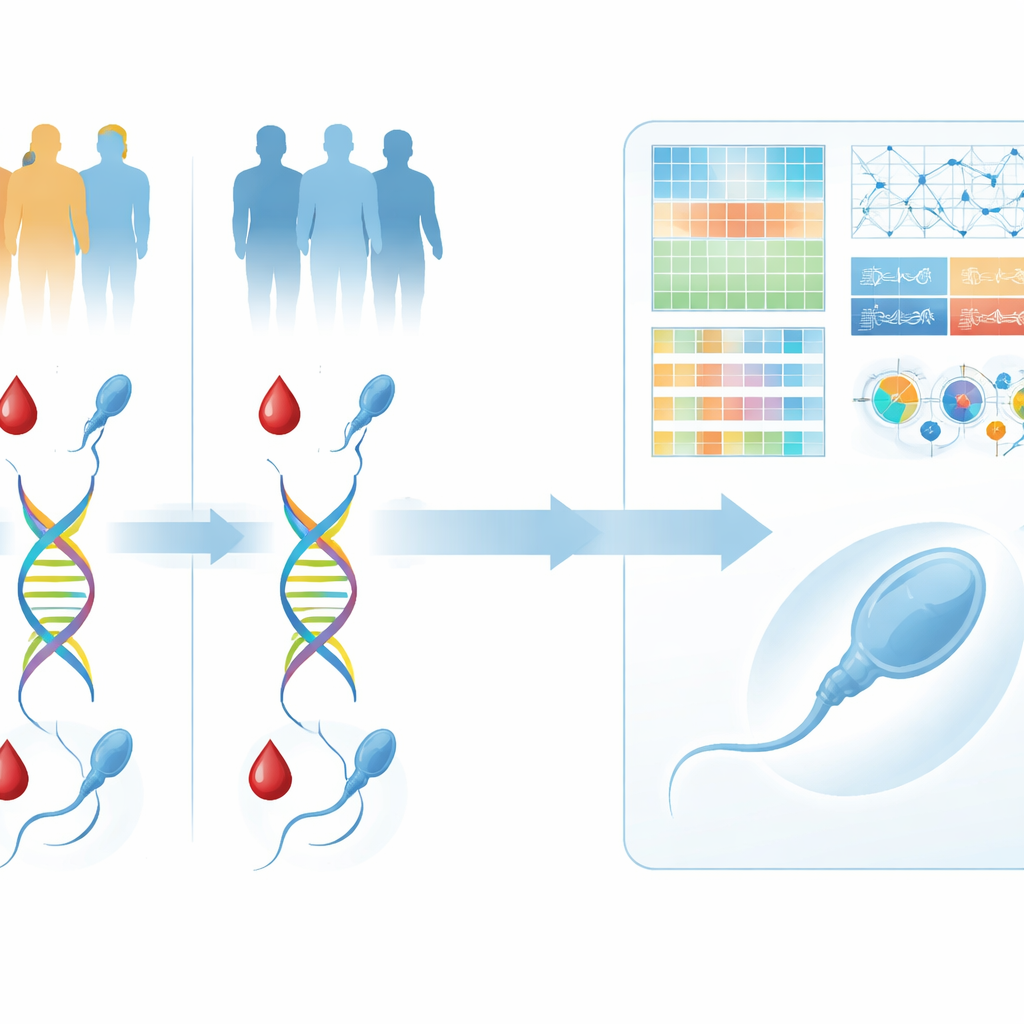
Bygga en DNA-karta från blod och enskilda spermier
Det som särskiljer detta arbete är dess dubbla fokus: forskarna tittade inte bara på sperma i mikroskop, de samlade också komplett DNA-information från både blod och enskilda spermier. Blodprover gav en bild av varje mans övergripande genetiska blåtryck med ungefär tiodubbel täckning, vilket innebär att de flesta positioner i genomet lästes flera gånger för tillförlitlighet. Från varje deltagare isolerade tekniker därefter noggrant flera enskilda spermier en och en under mikroskop, och undvek de som såg uppenbart abnorma ut. Dessa enskilda celler bearbetades med en specialiserad metod som kan kopiera och sekvensera nästan allt deras DNA, vilket ger en låg men användbar ögonblicksbild av varje sperms genom.
Förvandla råa läsningar till en högkvalitativ dataresurs
Eftersom detta är en datafokuserad studie snarare än ett typiskt experiment med en specifik hypotes, är det viktigaste resultatet kvaliteten och strukturen i datasättet självt. Teamet kontrollerade DNA‑koncentration och integritet, rensade bort tekniskt brus och verifierade att både blod‑ och spermsekvenser uppfyllde vanliga standarder som används inom human genetik. I genomsnitt lästes blod‑DNA med en djup på strax över tio gånger, medan sperm‑DNA nådde cirka 1,7 gånger täckning per cell, en nivå lämpad för storskalig mönsterupptäckt över många celler. Viktigt var att de bekräftade att hormonnivåer såsom testosteron och östrogen var likartade mellan män med slöa spermier och de med typisk fertilitet. De verkliga skillnaderna låg i hur väl spermierna rörde sig: män i den fertila gruppen hade ungefär dubbelt så hög total rörlighet och högre mått på simväg och vändningsbeteende, vilket understryker att de två grupperna är meningsfullt olika i funktion även när deras hormonprofiler ser lika ut.
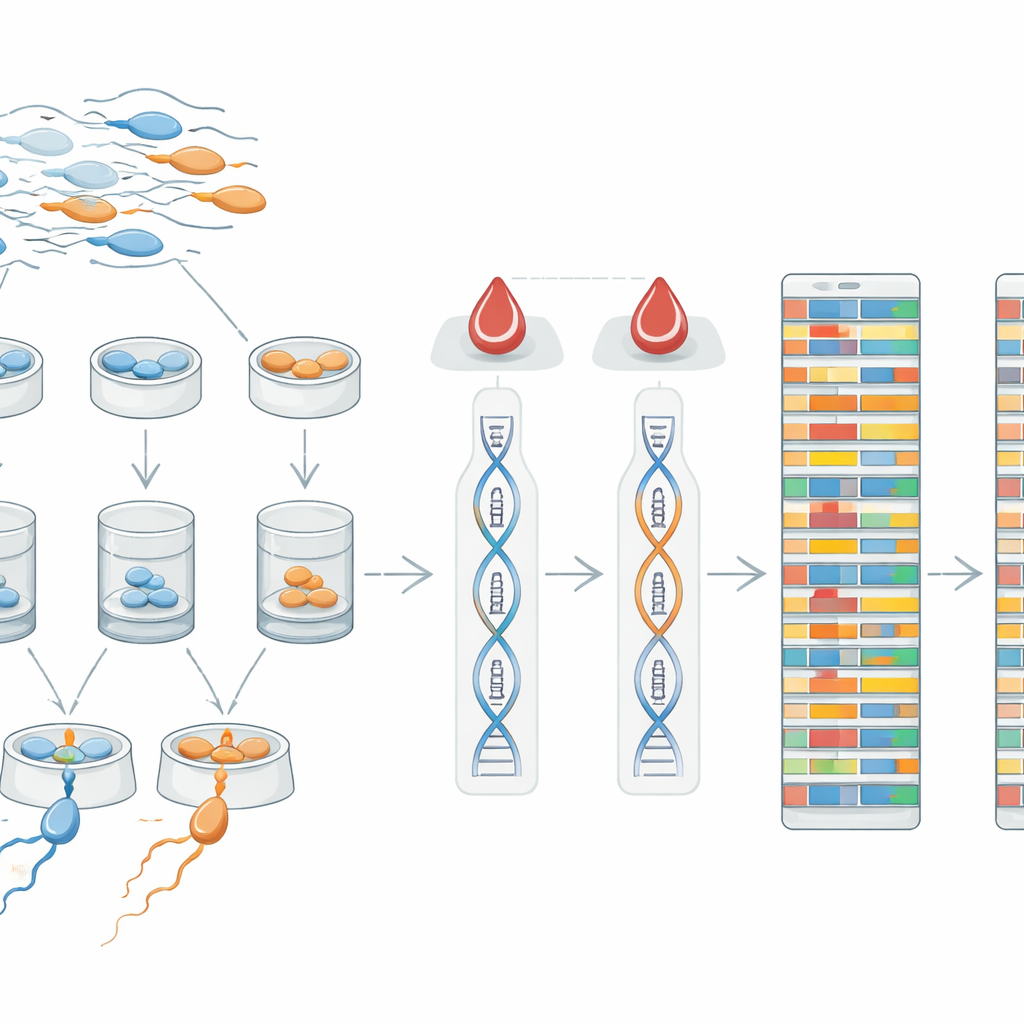
En ny testbänk för fertilitetsalgoritmer
Genom att göra alla dessa data offentligt tillgängliga vill författarna påskynda metodutveckling inom flera spetsområden. Eftersom spermier bara bär en kopia av varje kromosom erbjuder deras genom ett rent sätt att spåra hur DNA blandas under spermieutvecklingen och hur specifika kombinationer av genetiska varianter kan relatera till spermiefunktion. De parade blod‑ och spermsekvenserna ger också en referens för att testa nya beräkningsverktyg som försöker fylla i saknad information i låg‑täckningsdata eller som återskapar långa segment av ärvt DNA från spridda ledtrådar. Forskare kan använda detta datasätt för att förfina metoder för att upptäcka sällsynta mutationer, spåra överkorsningsevent där föräldrakromosomer byter segment, och jämföra genetiska mönster mellan män med och utan rörlighetsproblem.
Vad detta betyder för framtida patienter
För patienter i dag leder detta datasätt ännu inte till ett nytt kliniskt test, och det pekar inte ut en enda ”infertilitetgen”. Istället erbjuder det en noggrant kurerad grund som många framtida studier kan bygga på. Genom att kombinera detaljerade mått på hur spermier beter sig med matchat DNA från både kroppsceller och enskilda spermier ger resursen forskare en kraftfull plattform för att utforska hur subtila genetiska skillnader kan forma manlig fertilitet. Med tiden, när fler grupper analyserar dessa data och adderar sina egna, kan detta arbete bidra till att omvandla vaga etiketter som ”oförklarad manlig infertilitet” till klarare, DNA‑informerade diagnoser och i slutändan vägleda mer personligt anpassade val inom reproduktiv vård.
Citering: Chen, W., Yu, L., Li, R. et al. Matched whole-genome sequencing of blood (10×) and five single sperm cells (1×) per individual in 53 men. Sci Data 13, 405 (2026). https://doi.org/10.1038/s41597-026-06808-0
Nyckelord: manlig infertilitet, spermierörelse, helgenomsekvensering, single-cell–genomik, reproduktiv hälsa