Clear Sky Science · sv
En enda cell-transkriptomisk datamängd som kartlägger traumatisk hjärnskada och NeuroD1-baserad genterapi hos möss
Varför hjärnskador berör oss alla
Varje år drabbas miljontals människor av slag mot huvudet vid fall, kollisioner, idrott eller strid. Dessa traumatiska hjärnskador kan ge bestående problem med minne, rörelse och humör, och dagens behandlingar hanterar mest symtom snarare än att verkligen reparera hjärnan. Denna studie undersöker en lovande genbaserad metod i möss som syftar till att inte bara begränsa skadan utan att hjälpa hjärnan att bygga om sig själv inifrån, och kartlägger dessa förändringar cell för cell för att skapa en offentlig resurs för framtida terapier.
En inblick i den skadade hjärnan
När hjärnan skadas fungerar den inte som en muskel som bara får ett blåmärke. En komplex kedjereaktion tar vid: nervceller dör, blodflödet störs och stödjeceller som astrocyter och immunceller strömmar till. Astrocyter hjälper normalt till att försörja neuroner och hålla nervsignaler i balans, men efter trauma kan de bilda en tät ärrvävnad och driva långvarig inflammation. Författarna använde ett kontrollerat stickskadeprov i cortex hos möss för att efterlikna vissa former av penetrerande hjärnskada och undersökte hur varje större celltyp i den drabbade vävnaden svarade över tid. De använde en teknik kallad single-cell RNA-sekvensering, som läser av vilka gener som är aktiva i tiotusentals individuella celler, vilket möjliggör en detaljerad folkräkning av hur hjärnans cellulära gemenskap förändras efter skadan.
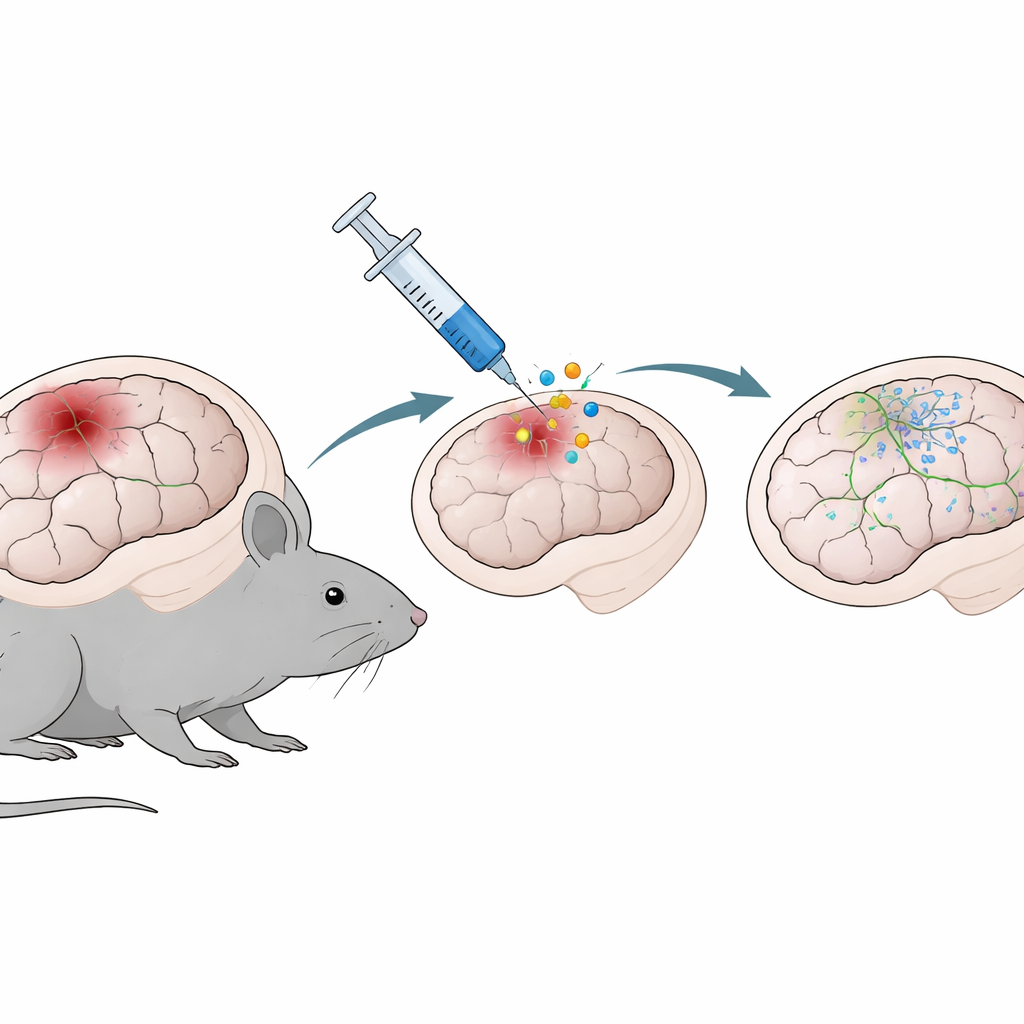
En genterapi som rekryterar hjärnans stödjeceller
Eftersom astrocyter är vanliga och finns direkt vid skadans plats är de attraktiva mål för reparationsstrategier. Teamet testade en genterapi baserad på NeuroD1, en gen som är känd för att driva celler mot ett neuronlikt tillstånd. Med hjälp av ett ofarligt virus som injicerades i det skadade kortikala området tre dagar efter skadan levererade de antingen en neutral markör (GFP) eller NeuroD1 till astrocyterna. När hjärnorna undersöktes en och två veckor senare visade mössen som fått NeuroD1 mindre vävnadshåligheter där skadan uppstått och färre aktiverade immunceller kallade mikroglia runt lesionen. Med andra ord minskade terapin inte bara synlig strukturell skada utan lugnade också den lokala inflammatoriska responsen.
Spåra celltyper en efter en
För att förstå vad som låg bakom dessa förbättringar jämförde forskarna tre grupper kortikala prover: friska möss, skadade möss som fått kontrollvirus och skadade möss som fått NeuroD1-virus. De sekvenserade mer än 97 000 individuella celler totalt och grupperade dem efter sina genaktivitetsmönster i välkända hjärnbosättare, inklusive neuroner, astrocyter, oligodendrocyter (som isolerar nervfibrer), mikroglia och celler som bekläder blodkärl och hjärnans hålrum. Själva skadan försköt denna balans mot fler astrocyter och mikroglia och färre neuroner och myelbildande celler, vilket speglar ärrbildning och inflammation. Med NeuroD1-behandling började denna snedvridning att vända: andelen neuroner, oligodendrocyter och epitelceller i plexus choroideus ökade, medan astrocyter och mikroglia blev mindre dominerande i det skadade området.
Astrocytundertypernas dolda arbete
Det visade sig att astrocyter inte är en enhetlig population. Genom att analysera dem separat identifierade teamet sju distinkta astrocytsubkluster, var och en med sin egen gensuskrift och beteende över de tre förhållandena. Vissa subkluster var vanliga i frisk vävnad men försvann nästan efter skadan, medan andra dök upp först efter trauma. I skadade hjärnor som behandlats med kontrollvirus slog flera astrocytgrupper på program involverade i att bygga och omforma synapser—de förbindelser där neuroner kommunicerar—samtidigt som de nedreglerade gener kopplade till energiproduktion i mitokondrierna. Detta mönster antyder att astrocyter efter skada främjar onormala omkopplingsförändringar samtidigt som de arbetar med minskad metabolisk kapacitet.
Hur NeuroD1 återbalanserar cellernas energi och kopplingar
NeuroD1-behandlingen formade dessa astrocytsubkluster i en annan riktning. I flera skadeassocierade astrocytgrupper ökades gener relaterade till mitokondrieaktivitet, cellandning och generell energimetabolism igen, medan gener kopplade till överdriven synapsbildning och myelinombyggnad dämpades. Med andra ord verkade NeuroD1 återställa energimotorerna i dessa celler och dämpa överdrivna försök till omkoppling som annars kan bidra till dysfunktion. Några astrocyttyper som expanderat kraftigt efter skada krympte i närvaro av NeuroD1, medan andra associerade med friskare funktioner ökade. Dessa detaljerade skift ger ledtrådar om vilka astrocyttillstånd som är skadliga och vilka som kan stödja reparation.
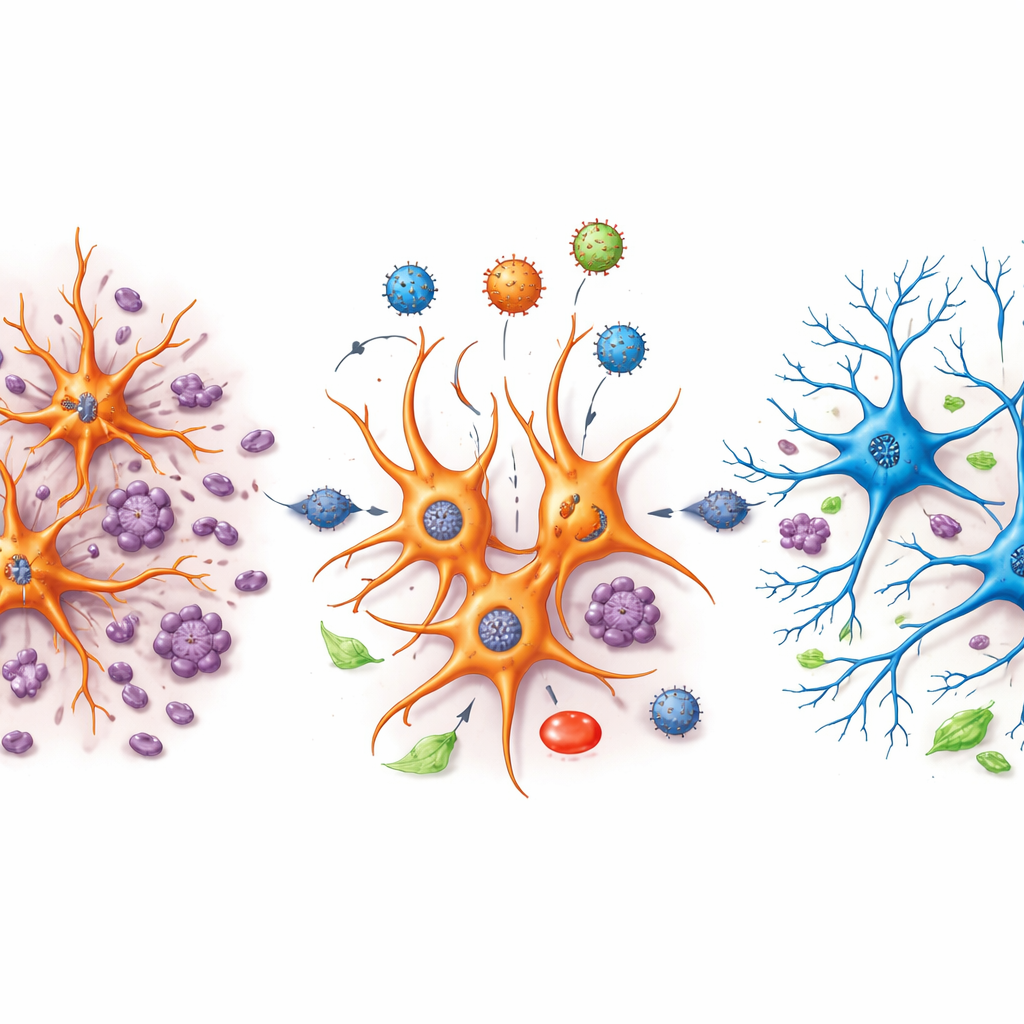
Vad detta betyder för framtida hjärnreparation
Detta arbete erbjuder ännu ingen färdig bot för mänskliga hjärnskador, men det levererar två viktiga framsteg. För det första visar det i en levande däggdjurshjärna att en riktad genterapi kan minska vävnadsförlust och inflammation samtidigt som den skjuter cellpopulationer och energianvändning tillbaka mot ett friskare tillstånd. För det andra gör det tillgängligt en rik, offentlig single-cell-datamängd som andra forskare kan gräva i för att identifiera specifika celltyper, gener och vägar som driver skada eller återhämtning efter trauma. För läsare utanför laboratoriet är huvudbudskapet att hjärnans egna stödjeceller potentiellt kan rekryteras och omprogrammeras för att hjälpa till att återbygga skadade kretsar, vilket för oss ett steg närmare behandlingar som återställer snarare än endast stabiliserar hjärnfunktionen efter ett traumatiskt slag.
Citering: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Nyckelord: traumatisk hjärnskada, genterapi, astrocyter, single-cell-sekvensering, NeuroD1