Clear Sky Science · sv
HMI-LUSC: En histologisk hyperspektralbildsdatamängd för skivepitelcancer i lungan
Att se cancer i nya färger
Lungcancer är fortfarande en av världens dödligaste sjukdomar, delvis eftersom det är svårt och tidskrävande att upptäcka varje sista cancercell på ett mikroskopglas. Patologer förlitar sig vanligen på rosa‑ och lila‑färgade färgningar som ses i mikroskop, en metod som fångar struktur men missar subtila kemiska ledtrådar. Denna artikel introducerar HMI‑LUSC, den första öppet tillgängliga samlingen av mikroskopbilder av skivepitelcancer i lungan fångade inte bara i tre färger utan i dussintals smala färgband, vilket ger datorer och kliniker en mycket rikare bild av vad som skiljer tumörceller från deras friska grannar.
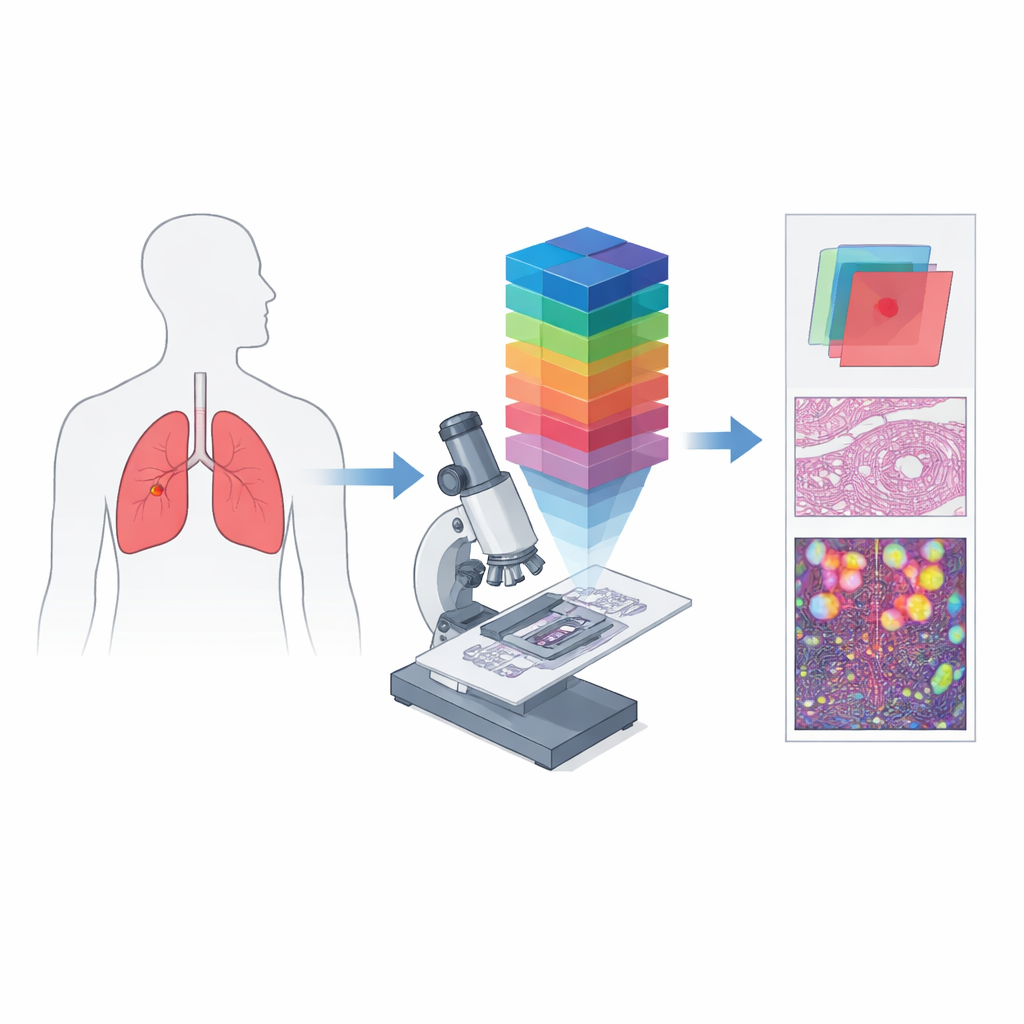
Från enkla färgbilder till spektrala fingeravtryck
Konventionell digital patologi fungerar mycket som en telefonkamera: den registrerar rött, grönt och blått för att approximera vad ögat ser. Hyperspektralavbildning tar flera steg längre genom att dela upp ljuset i många tätt liggande våglängder och producerar en tredimensionell ”datakub” där varje liten vävnadsfläck har sitt eget detaljerade färgspektrum. När denna idé kombineras med ett mikroskop blir det hyperspektral mikroskopi, som kan fånga både fin struktur och rikt spektralinformation på nivån av enskilda celler. Sådana data kan avslöja skillnader i hur vävnader absorberar och reflekterar ljus som är osynliga i standardbilder och skapa unika spektrala ”signaturer” för cancerösa respektive icke‑cancerösa områden.
Bygger ett nytt bibliotek för lungcancerforskning
Författarna skapade HMI‑LUSC för att fylla ett tydligt gap: före detta arbete fanns ingen offentlig hyperspektral datamängd för lungcancersnitt, vilket gjorde det svårt att testa och jämföra datorbaserade diagnostiska metoder. De samlade vävnad från tio patienter som genomgick lungtumörkirurgi, preparerade standardhematoxylin‑och‑eosin‑färgade snitt och skannade dem i hög upplösning. Erfaren patologer markerade tumör‑ och normalområden, och representativa regioner avbildades om med ett egenbyggt hyperspektralt mikroskop. Varje resulterande bild täcker en liten vävnadsyta men omfattar 61 våglängder mellan 450 och 750 nanometer, med en upplösning på 3088 x 2064 pixlar. För varje region inkluderar datamängden den råa spektralkuben, en konventionell RGB‑rendering och maskar som avgränsar var tumörvävnad finns.
Från grova omriss till cellnivåkartor
Medan märkningar på snittnivå är användbara kräver träning av moderna algoritmer ofta information på nivån av individuella celler. Att manuellt rita ut varje cell är opraktiskt, så teamet utformade ett semi‑automatiskt arbetsflöde. Först grupperade de pixlar i kluster baserat på deras spektrala likhet med en standard metod inom datorseende. Sedan granskade patologer dessa kluster överlagrade på vävnadsbilden och tilldelade dem till fyra kategorier: tumörceller, icke‑tumörceller, icke‑cellulär vävnad såsom stroma eller blod, och tom bakgrund. En andra patolog granskade och justerade dessa resultat, där meningsskiljaktigheter löstes genom konsensus. Resultatet är en uppsättning detaljerade pixelför‑pixel‑masker som fångar subtila blandningar av celltyper och förvirrande gränszoner, vilket ger mycket rikare undervisningsmaterial för maskininlärningssystem.
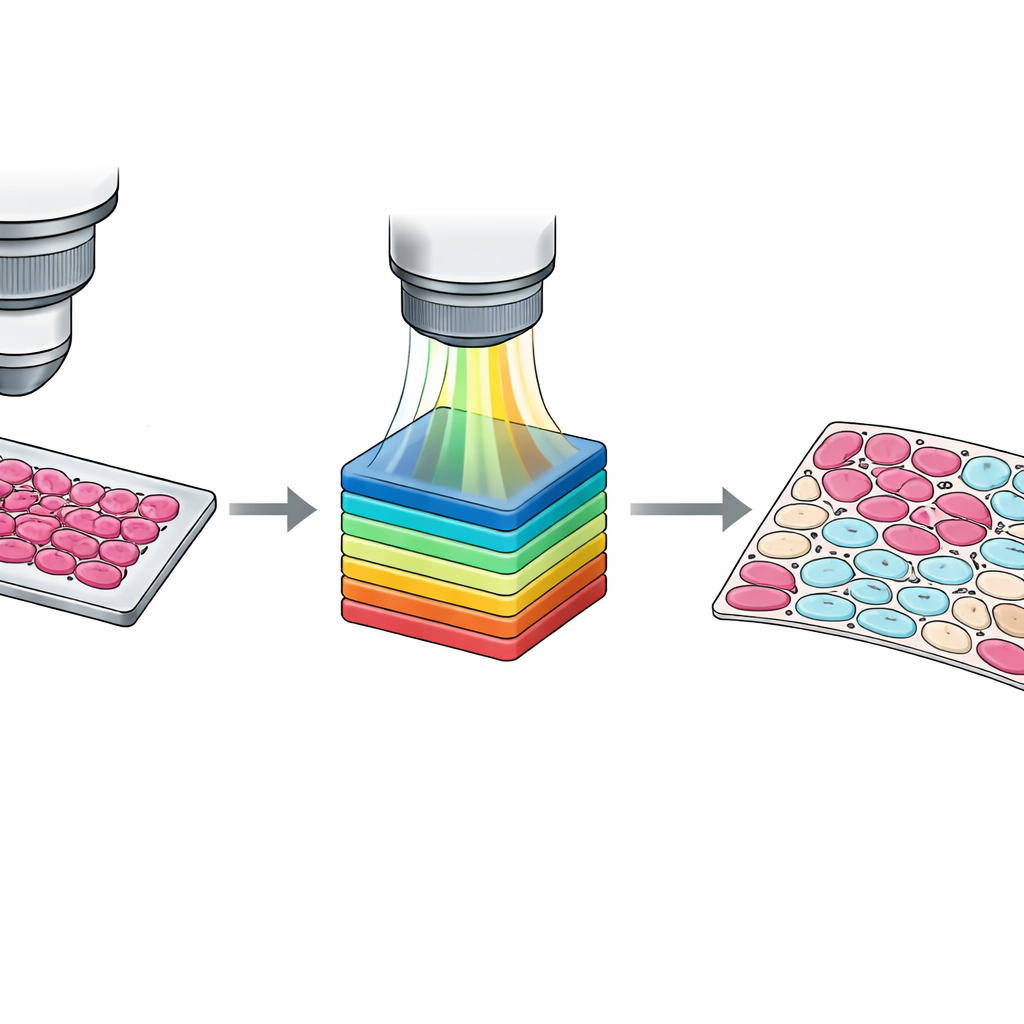
Att säkerställa skarpa och pålitliga data
För att göra datamängden trovärdig testade författarna sitt avbildningssystem noggrant. De verifierade att mikroskopet kan lösa fina mönster ned till ungefär en mikrometer—tillräckligt litet för att särskilja enskilda celler—och att bildbrus är lågt över de flesta våglängder. De jämförde också det uppmätta spektrumet för en standardljuskälla med referenskurvor och med en kommersiell hyperspektralkamera och fann utmärkt överensstämmelse. Slutligen demonstrerade de hur data kan användas genom att köra baslinjemodeller, från klassiska maskininlärningsmetoder till enkla djupa nätverk, för att segmentera tumörområden. Även utan omfattande optimering uppnådde dessa modeller god noggrannhet, vilket visar att datamängden lämpar sig väl som en referens för framtida metoder.
Vad detta betyder för framtida lungcancervård
HMI‑LUSC ersätter inte stora samlingar av standardsnitt, och det är ännu inte ett kliniskt verktyg i sig. Istället erbjuder det forskare ett noggrant kurerat fönster in i hur lungtumörceller skiljer sig från närliggande vävnad över många ljusvåglängder. Genom att göra dessa data, etiketter och kod öppet tillgängliga ger författarna en gemensam testbädd för att utveckla och jämföra algoritmer som utnyttjar spektralinformation, från enkla klassificerare till avancerade neurala nätverk. På lång sikt kan sådan forskning hjälpa datorer att bistå patologer att upptäcka tumörer mer precist och snabbare, och kan avslöja spektrala mönster kopplade till tumörtyp eller behandlingssvar som vanliga bilder inte kan visa.
Citering: Yan, Z., Huang, H., Guo, Y. et al. HMI-LUSC: A Histological Hyperspectral Imaging Dataset for Lung Squamous Cell Carcinoma. Sci Data 13, 415 (2026). https://doi.org/10.1038/s41597-026-06766-7
Nyckelord: hyperspektralavbildning, lungcancer, digital patologi, tumörsegmentering, medicinsk bilddatamängd