Clear Sky Science · sv
Flerdimensionell transkriptomdatamängd för systematisk utvärdering av Jakyakgamcho-tang‑inducerade cellsignaturer
Varför detta forntida botemedel är relevant idag
Många vänder sig till traditionella växtbaserade läkemedel för muskelkramper, smärta eller allmänt välbefinnande, men hur dessa åldrade preparat påverkar våra celler är fortfarande till stor del ett mysterium. Denna studie fokuserar på Jakyakgamcho‑tang, en enkel två‑örtformel som länge använts i Östasien, och ställer en modern fråga: hur förändrar olika sätt att blanda och bereda örterna vad de gör med våra celler? Genom att kartlägga hur gener i mänskliga och djuriska celler svarar på många varianter av detta preparat skapade forskarna en detaljerad referens som kan hjälpa forskare att testa, jämföra och förfina växtbaserade behandlingar med samma stringens som används för konventionella läkemedel.
En enkel två‑örtformel under mikroskopet
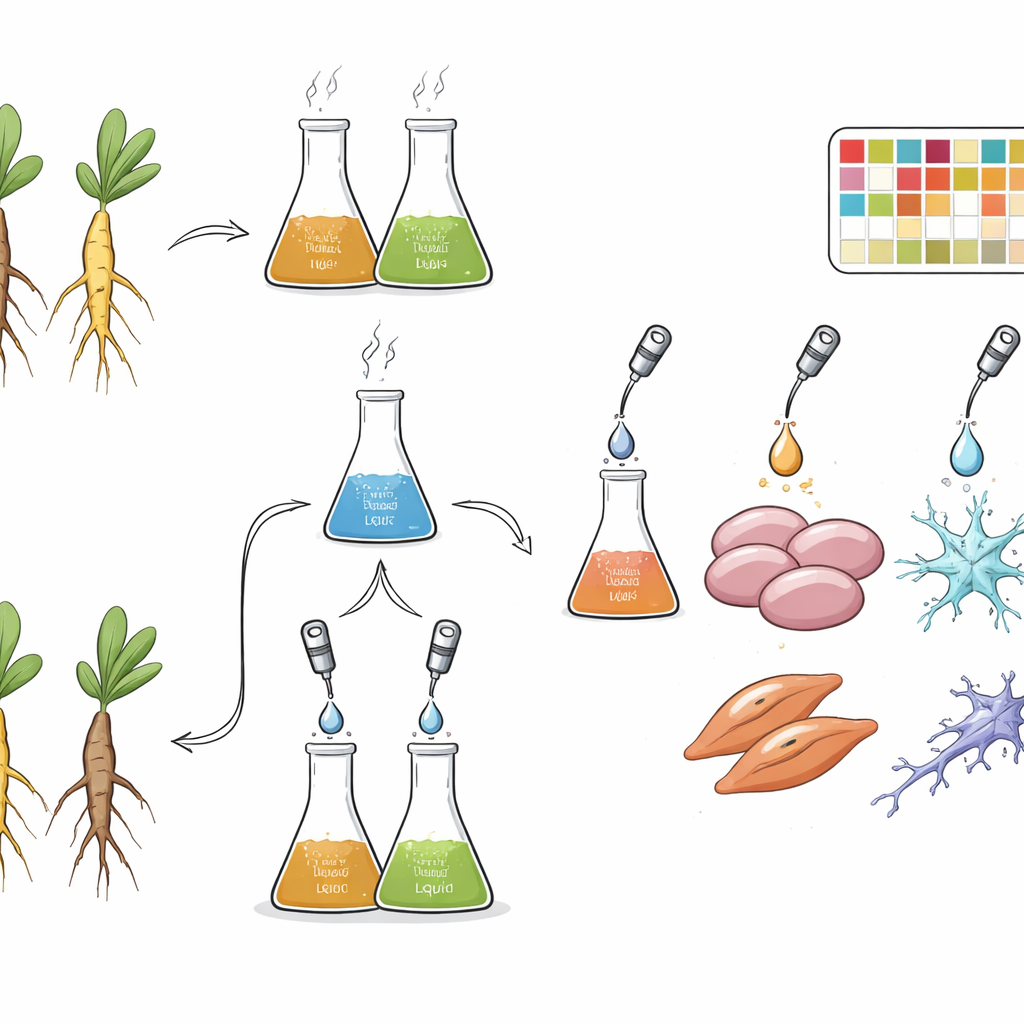
Jakyakgamcho‑tang består av bara två ingredienser: Paeoniae Radix (från pionrot) och Glycyrrhizae Radix et Rhizoma (från lakritsrot). Traditionellt ordineras den för muskelspasmer och smärta, och nyare forskning tyder på att den även kan hjälpa vid muskelförtvining, inflammation och minnesproblem. Men preparatet bereds inte alltid på samma sätt. Vårdare kan använda mer pion eller mer lakrits, koka örterna i vatten eller extrahera dem med alkohol, och antingen koka dem tillsammans eller göra separata extrakt och sedan blanda dem. Var och en av dessa val kan förändra vilka växtkemikalier som hamnar i slutligen drycken och därmed hur kroppen reagerar. Författarna satte som mål att fånga dessa skillnader på ett systematiskt och datarikt sätt.
Att utforma ett brett och noggrant testfält
För att göra detta framställde teamet många versioner av formeln. De testade tre pion‑till‑lakrits‑förhållanden (mer pion, lika delar eller mer lakrits), två lösningsmedel (vanligt varmt vatten eller 70 % etanol) och två beredningsmetoder. I den kombinerade metoden blandades örterna först och extraherades sedan tillsammans, vilket tillät deras kemikalier att interagera under kokning eller sonikering. I den individuella metoden extraherades varje ört för sig och de torkade extrakten blandades först i efterhand, vilket främjar standardisering och bevarande av känsliga föreningar. Forskarna mätte också viktiga markörkemikalier med hjälp av högpresterande vätskekromatografi och bekräftade att pionrelaterade föreningar ökade i pionrika blandningar och lakritsrelaterade föreningar i lakritsrika blandningar, samt att etanol generellt extraherade högre mängder av många ingredienser än vatten.
Att lyssna på celler i lever, muskel och nerv
Nästa steg exponerade forskarna tre väletablerade celltyper för dessa olika extrakt: leverliknande HepG2‑celler, muskelliknande C2C12‑celler och nervliknande PC12‑celler. Dessa cellinjer valdes eftersom de är nära knutna till tillstånd där formeln används, såsom muskelspasmer, smärta och bredare metabola eller nervsystemrelaterade problem. Noggrann dosbestämning säkerställde att de använda koncentrationerna störde cellaktiviteten utan att döda cellerna, så att genresponsen skulle reflektera farmakologiska effekter snarare än ren toxicitet. Varje förhållande testades i triplikat och mer än 500 RNA‑prover sekvenserades, vilket slutligen gav 513 högkvalitativa genuttrycksprofiler som registrerar hur tusentals gener i varje celltyp svarar på varje beredning av det växtbaserade preparatet.
Säkerställande av pålitliga och återanvändbara data
Eftersom detta arbete är avsett som en delad resurs lade teamet ner betydande ansträngning på kvalitetskontroller. Örterna autentiserades av experter och med DNA‑streckkodning, och deras kemiska sammansättning dokumenterades. RNA från behandlade celler undersöktes för renhet och integritet, och sekvenseringsläsningar visade höga kvalitetsvärden och god kartläggning mot lämpliga referensgenom. Replikatexperimenten var mycket konsekventa, med mycket starka korrelationer mellan upprepade prover över arter och batcher. Teamet jämförde också mönster på väg‑nivå från sina data med en oberoende läkemedels‑responsresurs kallad Connectivity Map. För tre välkända läkemedel som användes som kontroller överensstämde genaktivitetsmönstren i denna nya datamängd mycket bättre med de i den externa databasen när samma läkemedel användes, vilket stödjer mätningarnas pålitlighet och bredare relevans.
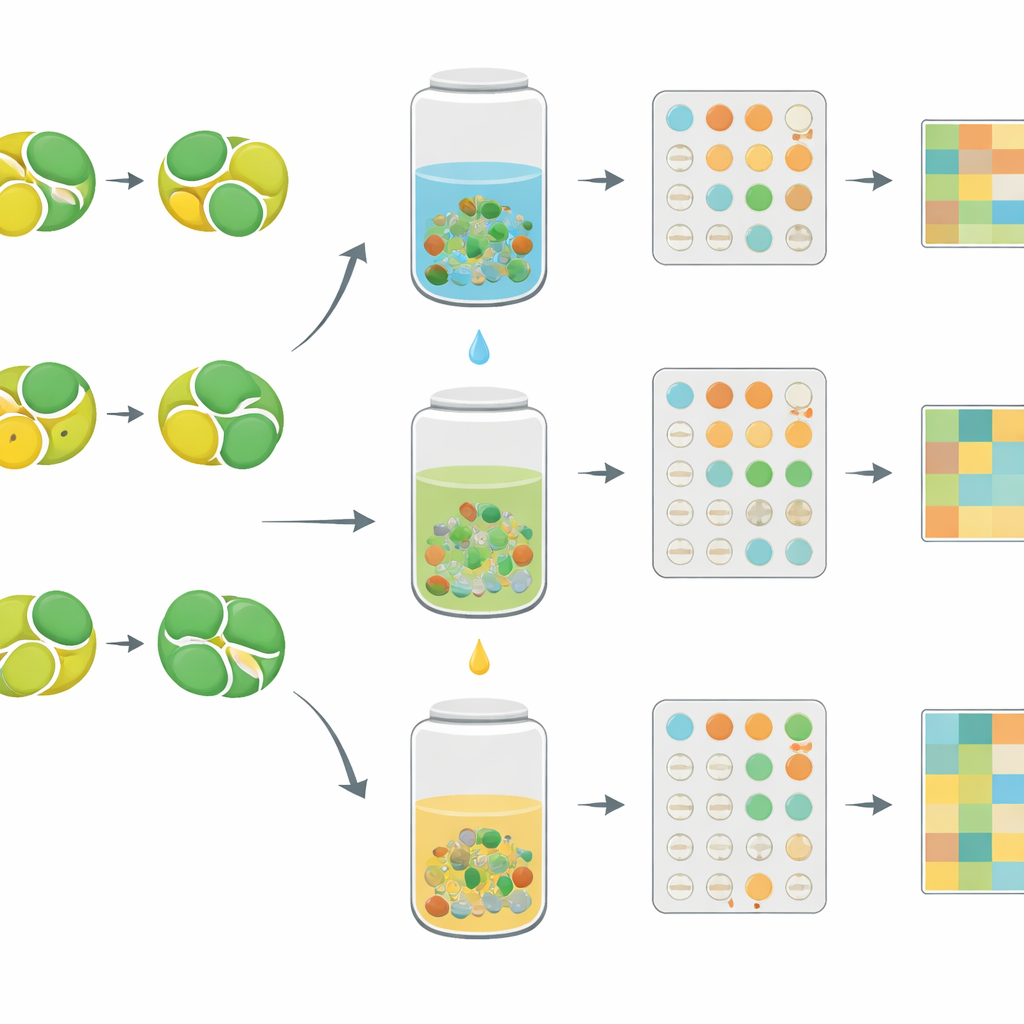
Från traditionella recept till datadriven förfining
All rå och bearbetad genuttrycksdata, tillsammans med detaljerad berednings‑ och kemisk information, har deponerats i offentliga databaser där andra forskare fritt kan utforska dem. I vardagliga termer förvandlar denna studie många små variationer av ett traditionellt två‑örts‑te till ett sökbart ”fingeravtrycks‑bibliotek” över hur celler reagerar på genetisk nivå. Detta gör det möjligt att till exempel ställa frågan vilken blandningskvot och vilket lösningsmedel som bäst stödjer muskelskyddande svar samtidigt som inflammatoriska signaler begränsas, eller vilken beredning som mest liknar verkan hos ett känt läkemedel. Genom att bygga sådana broar mellan länge använda botemedel och moderna molekylära verktyg lägger arbetet grunden för mer precis, evidensbaserad optimering av växtbaserade läkemedel.
Citering: Baek, SJ., Lee, H., Park, SM. et al. Multidimensional transcriptome dataset for systematic evaluation of Jakyakgamcho-tang-induced cell signatures. Sci Data 13, 367 (2026). https://doi.org/10.1038/s41597-026-06759-6
Nyckelord: läkemedel av växtrötter, genuttryck, RNA-sekvensering, läkemedelsresponsdata, Jakyakgamcho-tang