Clear Sky Science · sv
Storskalig histologisk bilddatabas med metadata för tjock- och ändtarmscancerens mikromiljö
Varför det spelar roll att kartlägga cancerns dolda grannskap
När läkare tittar på en tumör i tjocktarmen under mikroskopet ser de inte bara cancerceller; de ser ett livligt grannskap av fett, immunceller, bindväv och mer. Denna blandning av celltyper, som kallas tumörmikromiljön, påverkar starkt hur en patient svarar på behandling och hur lång tid de lever. Datorer som skulle kunna hjälpa läkare att tolka dessa komplexa scener har dock hindrats av ett enkelt problem: de har inte haft tillräckligt många välannoterade bilder att lära sig från. Denna studie presenterar en av de största och noggrant annoterade bildsamlingarna av vävnad från kolorektal cancer som någonsin satts ihop, speciellt utformad för att träna och testa moderna artificiella intelligenssystem.
Bygga ett massivt bildbibliotek av colon-tumörer
Forskarna skapade en resurs de kallar HMU-CRC-Hist550K, byggd från vävnadsprover från 500 patienter som behandlats för kolorektal cancer vid ett större cancercenter i Kina. Varje patients tumör bevarades, färgades på det sätt som är standard i patologiska laboratorier och skannades till en högupplöst digital bild. Från dessa skivor klippte teamet automatiskt ut små kvadratiska bildrutor, vardera ungefär i storlek med det en patolog kan se genom mikroskopet vid ett givet tillfälle. Totalt framställdes omkring 550 000 sådana rutor, vilket ger artificiella intelligensmodeller en stor och varierad uppsättning exempel för att lära sig hur olika vävnader ser ut.
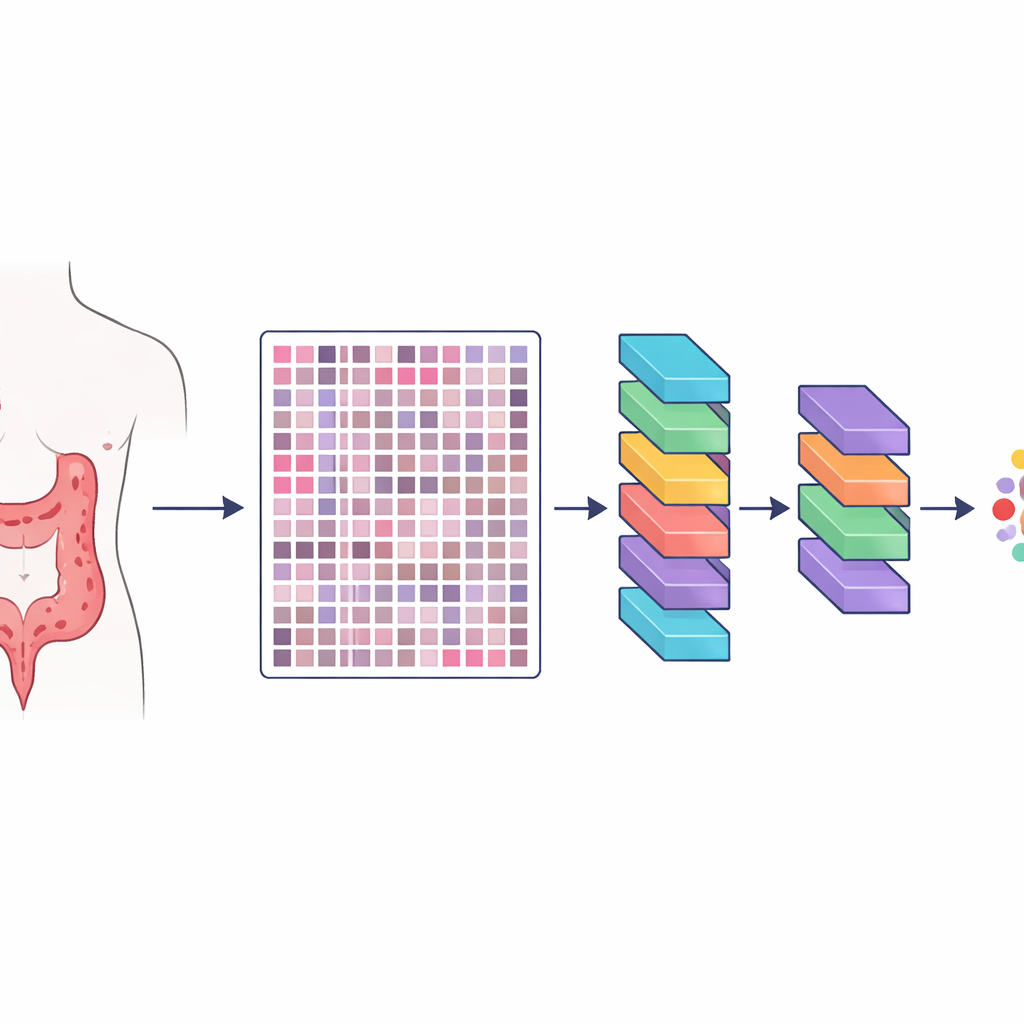
Noga mänsklig märkning av cancerlandskapet
Att skapa ett stort bildbibliotek räcker inte; bilderna måste också märkas korrekt. Tre erfarna patologer arbetade tillsammans genom en trestegsprocess för att markera åtta centrala komponenter i tumörens omgivning: fettvävnad, cellrester, immunceller kallade lymfocyter, slem, glatt muskulatur, normal tarmepitel, stödjande bindväv runt tumören och själva cancercellerna. Två patologer ritade först regioner på de stora skivorna oberoende av varandra och kontrollerade sedan varandras arbete. En senior specialist gjorde en slutlig granskning, löste meningsskiljaktigheter och uteslöt oklara områden. Denna ömsesidiga kontroll minskade i hög grad personlig bias och gav mycket konsekventa etiketter i fin detalj, så att varje ruta kopplades till en specifik vävnadstyp inom tumörens grannskap.
Koppla mikroskopbilder till patienthistoria
Det som gör denna datamängd särskilt kraftfull är att bilderna är parade med rik klinisk information för varje patient. För varje fall samlade teamet grundläggande uppgifter såsom ålder och kön, liksom tumörstadium, tumörens placering längs tjock- och ändtarmen, hur avvikande cancercellerna såg ut, om nerver eller lymfkörtlar var invaderade och hur länge patienten överlevde efter behandling. De registrerade även resultat från vanliga laboratorietester som speglar tumörens genetiska och proteinhalt. Alla personliga identifierare togs bort så att patienterna inte kan kännas igen. Genom att kombinera vävnadsmönster med dessa kliniska egenskaper kan forskare undersöka hur specifika mikromiljöupplägg relaterar till verkliga utfall, till exempel vilka patienter som klarar sig bättre eller sämre.
Sätta AI på prov med den nya datamängden
För att visa att datamängden verkligen är användbar tränade forskarna tre olika djupinlärningsmodeller—moderna mönsterigenkänningssystem som är utmärkta på bilduppgifter—för att identifiera de åtta vävnadstyperna i rutorna. De använde strikta regler för att dela upp patienter mellan tränings- och testgrupper så att modellerna bedömdes på patienter de aldrig sett tidigare. Modellerna, inkluderande både klassiska bildernätverk och en nyare ”vision transformer”-arkitektur, uppnådde alla mycket hög noggrannhet, med prestationsmått som var nära perfekta på flera testuppsättningar. Teamet jämförde också resultaten med andra avancerade bildsegmenteringsmetoder och fann liknande stark prestanda. Visuella verktyg användes för att framhäva vilka delar av vävnaden modellerna förlitade sig på, vilket bekräftade att de fokuserade på medicinskt meningsfulla regioner snarare än slumpmässiga mönster.
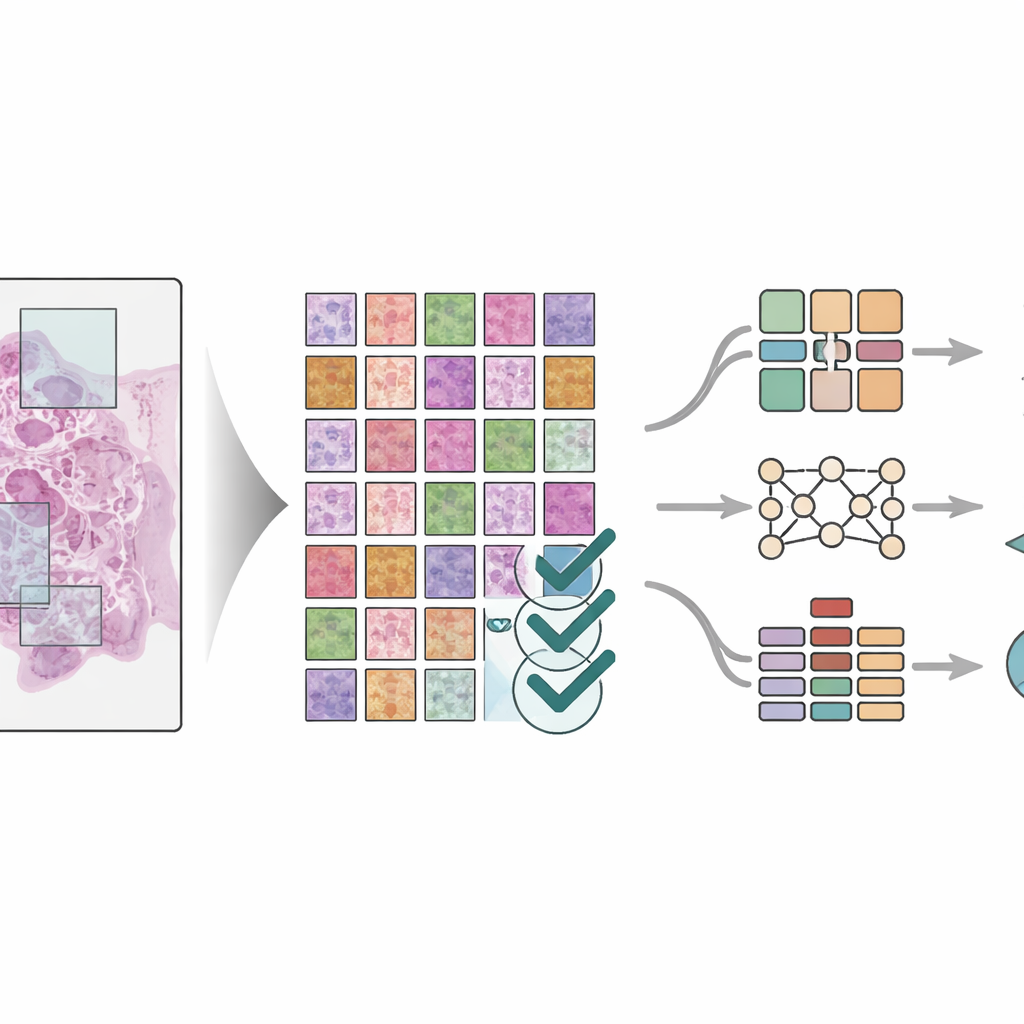
Vad detta betyder för framtida cancervård
För icke-specialister är huvudbudskapet att detta arbete inte introducerar en ny behandling, utan snarare en kraftfull grund för smartare diagnostik och prognosbedömning. Genom att dela ett stort, välorganiserat och öppet tillgängligt bildbibliotek kopplat till detaljerade patientregister möjliggör författarna för forskare världen över att bygga och jämföra artificiella intelligensverktyg på samma solida grund. Sådana verktyg skulle på sikt kunna hjälpa patologer att snabbare och mer konsekvent kartlägga tumörens grannskap, förutsäga vilka patienter som löper högre risk och föreslå mer individualiserade behandlingsstrategier. Även om de nuvarande data endast fångar enstaka tidpunkter snarare än förändringar över månader eller år, är denna resurs ett viktigt steg mot att använda digital patologi och AI för att bättre förstå och i slutändan bättre behandla kolorektal cancer.
Citering: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Nyckelord: kolorektal cancer, tumörmikromiljö, digital patologi, djupinlärning, medicinsk bilddatamängd