Clear Sky Science · sv
Vitamin B2-metabolism främjar FSP1-stabilitet för att förhindra ferroptos
Hur ett vanligt vitamin hjälper celler att avgöra mellan liv och död
Våra celler balanserar ständigt mellan överlevnad och självförstörelse. En dramatisk form av celldöd, kallad ferroptos, har fått uppmärksamhet eftersom den kan döda cancerceller selektivt som är motståndskraftiga mot andra behandlingar. Denna studie visar att ett vardagligt näringsämne — vitamin B2, eller riboflavin — tyst tippar vågskålen genom att stabilisera ett viktigt skyddande protein. Att förstå denna dolda koppling mellan kost, cellmetabolism och cancercelldöd kan hjälpa forskare att utforma klokare behandlingar och förfina framtida kostråd.
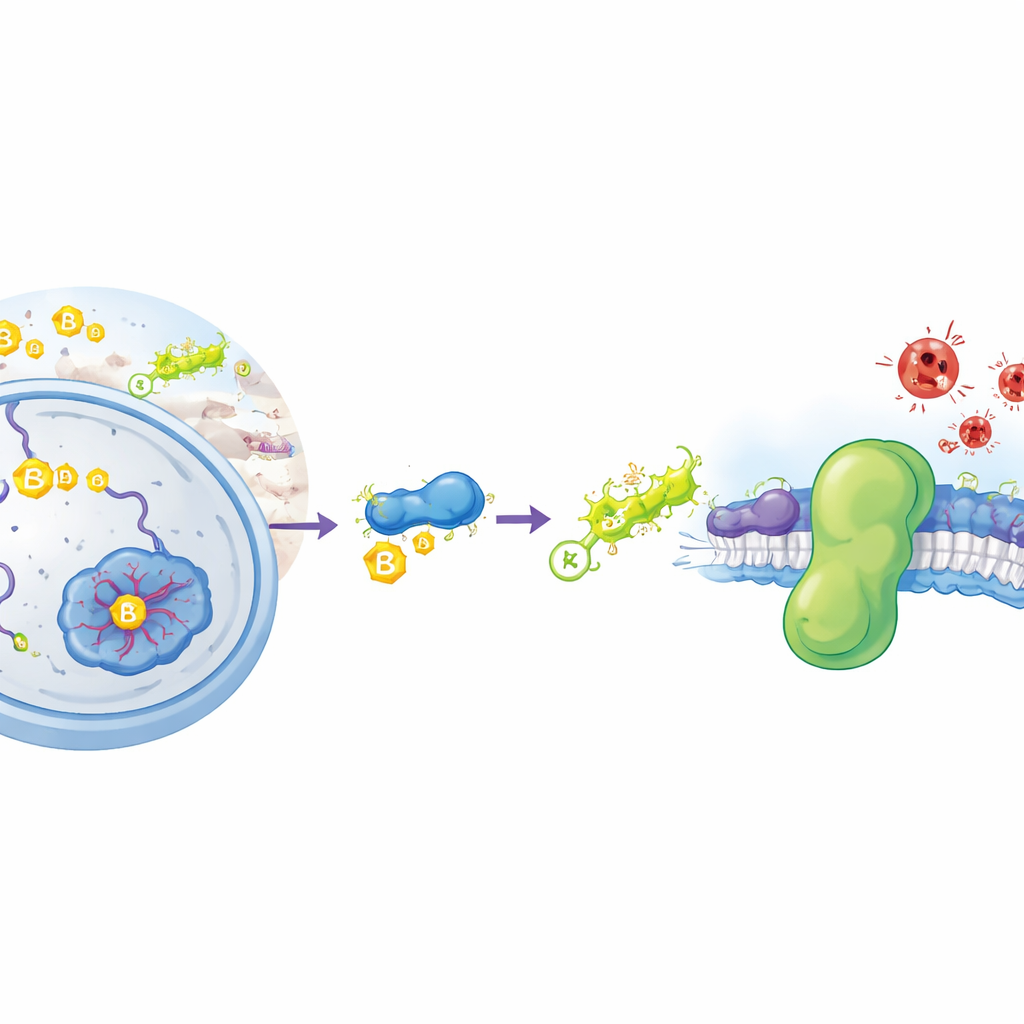
En speciell sorts rost inne i celler
Ferroptos är en typ av celldöd som drivs av en kemisk process inte olik metallrost: okontrollerad oxidation av fetter i cellmembran. När dessa fetter bryts ner förlorar membranen sin integritet och cellerna spricker. Våra celler använder normalt flera försvar för att förhindra detta. En huvudsköld är ett enzym som kallas GPX4, som använder en liten molekyl, glutation, för att avgifta skadliga lipidhydroperoxider. En andra, parallell sköld är ett protein som heter FSP1, som sitter på cellmembran och använder små fettliknande molekyler för att fånga destruktiva radikaler innan de sprider sig. Cancerceller ökar ofta FSP1 för att undvika ferroptos, vilket gör detta protein till ett huvudmål för nya cancerläkemedel. Ändå har forskare hittills inte vetat hur celler styr hur mycket FSP1 som tillverkas och hur länge det överlever.
Bygga en cellulär "bränslemätare" för en död-blockerare
För att avslöja de dolda reglerarna av FSP1 konstruerade forskarna först mänskliga bencancerceller så att de bar en fluorescerande rapportör. De märkade det naturliga FSP1-proteinet med en grön ljussignal och kopplade det till en blå signal som visar hur mycket FSP1-meddelande cellen producerar. Denna fiffiga design gjorde det möjligt att särskilja förändringar i genaktivitet (blå) från förändringar i proteinstabilitet (grön). Med detta tvåfärgssystem på plats använde de CRISPR–Cas9 för att systematiskt störa nästan varje gen i genomet och sorterade sedan celler med höga respektive låga nivåer av FSP1. Genom att jämföra vilka guide-RNA som var berikade i varje grupp kartlade de hundratals gener som antingen förstärker eller minskar FSP1, verksamma på nivåer av genkontroll eller proteinomsättning.
Vitamin B2:s dolda uppgift: skapa ett stabiliserande grepp
Bland de mest iögonfallande träffarna fanns två enzymer, riboflavinkinase (RFK) och FAD-syntas (FLAD1), som omvandlar vitamin B2 till en kofaktor kallad FAD. FSP1 är en flavoprotein som normalt binder FAD tätt för att utföra sina kemiska reaktioner. När RFK eller FLAD1 togs bort, eller när celler odlades i medium utan vitamin B2, sjönk FSP1-proteinnivåerna kraftigt trots att dess genaktivitet förblev liknande. Teamet visade att denna förlust gjorde cellerna mycket mer sårbara för ferroptos när GPX4 blockerades. Viktigt är att vitamin B2 i sig inte fungerade som en klassisk antioxidant: i ett känsligt provrörstest lyckades det inte stoppa lipidoxidation, till skillnad från vitamin E. Istället återställde tillsats av FAD (och delvis dess föregångare FMN) till bristfälliga celler både FSP1-nivåer och motståndskraft mot ferroptotisk död, medan extra vitamin B2 ensam inte hjälpte om processeringsenzymerna saknades.
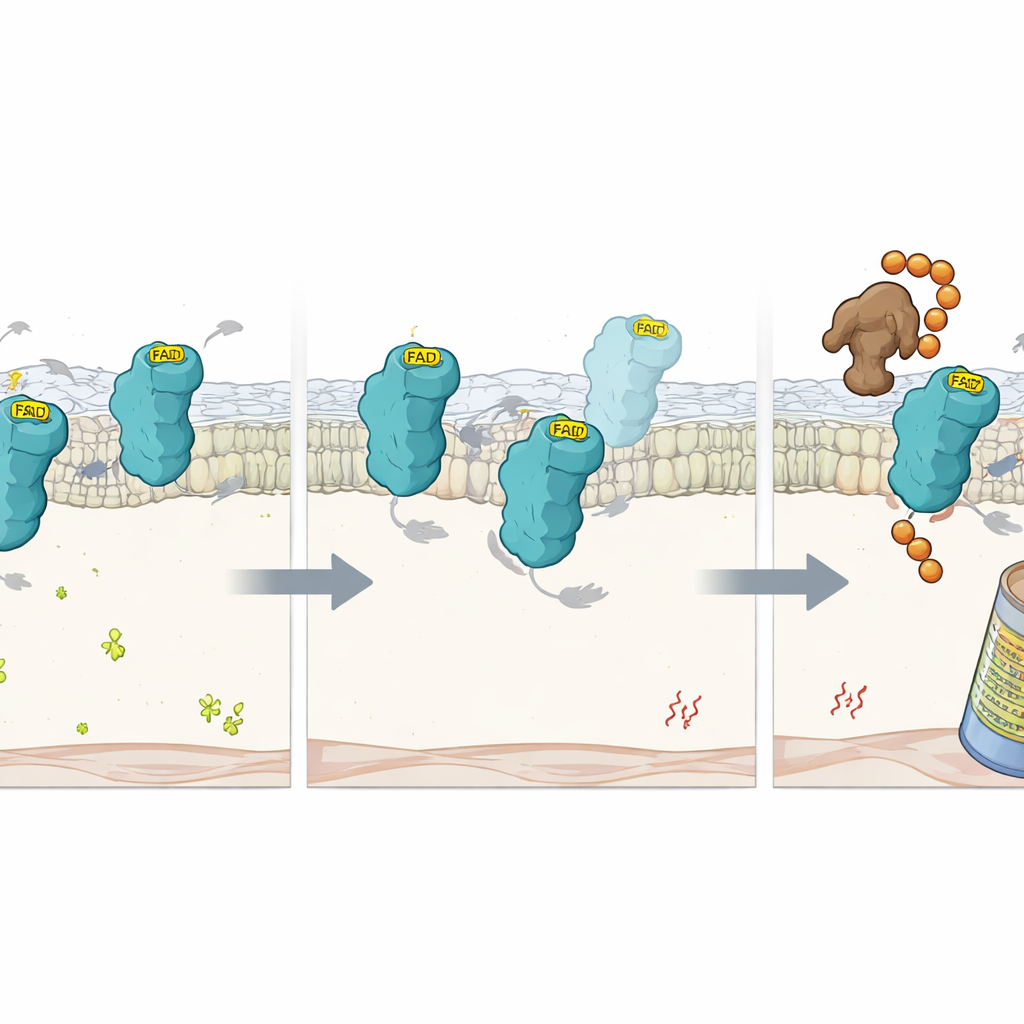
Vad som händer när kofaktorn saknas
För att zooma in ytterligare studerade forskarna precisa mutationer i FSP1 som försvagar dess förmåga att hålla FAD. Dessa mutantproteiner veckades fortfarande till i stort sett normala former men förlorade sitt FAD och sin katalytiska aktivitet. Inne i cellerna förföll de mycket snabbare än normalt FSP1, såvida inte proteasomen — cellens proteinreducerande maskineri — blockerades. Detta antyder att FAD-bindning i sig fungerar som ett stabiliserande handtag som skyddar FSP1 från att märkas som defekt. Genom att använda en annan riktad CRISPR-skärm under förhållanden med låg FAD identifierade teamet en E3-ligas som kallas RNF8 som en nyckelfaktor som känner igen FAD-fri FSP1. När RFK raderades fäste RNF8 kedjor av ubiquitinmärken på det tomma proteinet, vilket riktade det för nedbrytning av proteasomen. Att ta bort RNF8 saktade ner FSP1-omsättningen i FAD-fattiga celler, även om det inte kunde återställa dess förlorade skyddsfunktion utan kofaktorn.
Från molekylär krets till idéer för cancerterapi
Genom att sätta ihop dessa delar föreslår författarna en enkel men kraftfull modell. Vitamin B2, efter att ha omvandlats till FAD av RFK och FLAD1, binder till FSP1 och är avgörande både för dess biokemiska aktivitet och dess livslängd. När vitamin B2-försörjningen eller dess bearbetning sviktar kan nyproducerad FSP1 inte säkra FAD, märks av RNF8 och bryts snabbt ner av proteasomen, vilket lämnar cellerna mer exponerade för ferroptotisk skada. Cancerdata tyder på att tumörer med högre RFK-uttryck är mer motståndskraftiga mot ferroptosframkallande läkemedel, vilket understryker denna pathways verkliga betydelse. För icke-specialister är huvudbudskapet att ett välbekant vitamin gör mycket mer än att fungera som en enkel antioxidant: det hjälper avgöra om ett kraftfullt anti-dödsprotein står vakt eller sopas bort. Genom att justera vitamin B2-metabolismen eller stabiliteten hos FSP1 kan framtida behandlingar bättre utnyttja ferroptos för att eliminera cancerceller samtidigt som frisk vävnad skonas.
Citering: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Nyckelord: ferroptos, vitamin B2, FSP1, cancercelldöd, cellmetabolism