Clear Sky Science · sv
Kartläggning, uppkomst och roll för transposabla element–gen-kimera i att öka transkriptomets plasticitet
Dolda passagerare i vårt DNA
En stor del av vårt DNA består av forntida virala fripassagerare kallade transposabla element — genetiska kodstycken som förr hoppade runt i genomet som hitte-påparasiter. Denna studie visar att dessa gamla virala fragment inte bara är tyst skräp: de kan splicas in i våra egna gener och skapa hybrida budskap, hjälpa celler att anpassa sig till förändrade förhållanden och ibland driva sjukdom. Genom att kartlägga dessa hybrider över utveckling, åldrande och cancer visar författarna ett överraskande sätt på vilket viralt DNA fortfarande formar mänsklig biologi i dag.
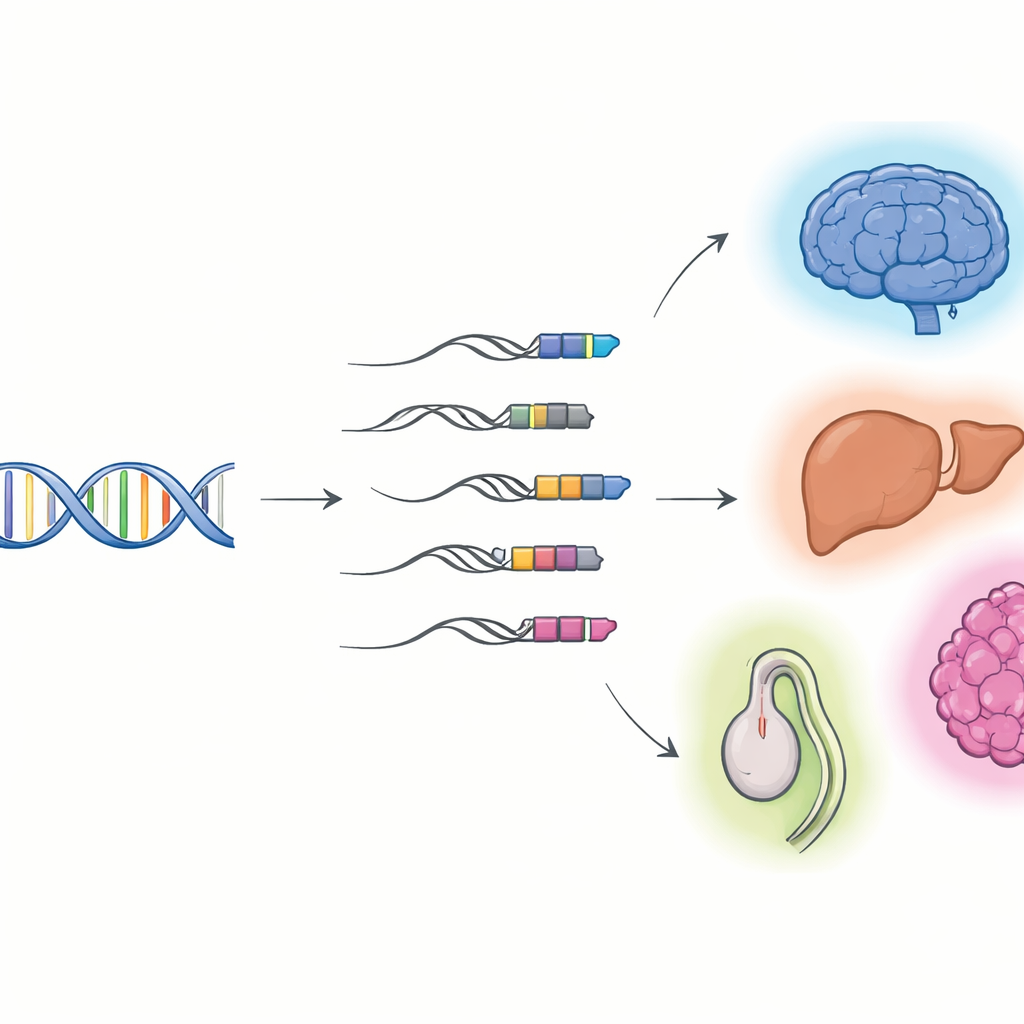
När viralt DNA blir en del av våra gener
Forskarnas fokus låg på ”TE–gen-kimera”: RNA-molekyler som börjar i ett transposabelt element och sedan fortsätter in i en värdgen. Med hjälp av långavläsningssekvensering, som kan återge hela RNA-molekyler från ände till ände, i kombination med vanlig kortavläsningssekvensering, byggde de detaljerade kataloger över dessa hybrider i mus- och människoceller och organ. De fann tusentals tidigare okända kimära transkript, de flesta av dem icke-kodande RNA snarare än proteinkartor. Många börjar i en klass av virala rester kallade long terminal repeats (LTR), som ofta ligger framför gener och kan fungera som alternativa av- och på-strömbrytare. Olika vävnader och organ använder olika uppsättningar av dessa kimera, med särskilt rik aktivitet i hjärnan, levern och testiklarna, och deras användning skiftar när vävnader utvecklas från foster- till vuxenstadier.
Kimera vid åldrande och cancer
För att se hur dessa viral–värd-hybrider beter sig i verkliga populationer grävde teamet i stora mänskliga dataset som täcker dussintals vävnader från hundratals personer, samt tumörprover. De identifierade flera hundra kimera med hög trovärdighet som återkommer mellan individer. Deras uttryck varierar inte bara mellan organ utan även med ålder: i vävnader som blod och hjärna minskar vissa LTR-drivna kimera hos äldre vuxna, medan de i vissa perifera vävnader ökar. I många cancerformer är dessa LTR-baserade hybrider generellt uppreglerade i tumörer jämfört med närliggande normalvävnad, och patienter vars tumörer uttrycker mer av dem tenderar att få sämre utfall. I dataset från personer som är resistenta mot kemoterapi eller immunterapi sitter generna som påverkas av nya LTR-drivna exoner ofta i vägar kopplade till hur dessa läkemedel fungerar, vilket tyder på att TE-kimera kan hjälpa tumörer att omkoppla sig själva under behandlingspress.
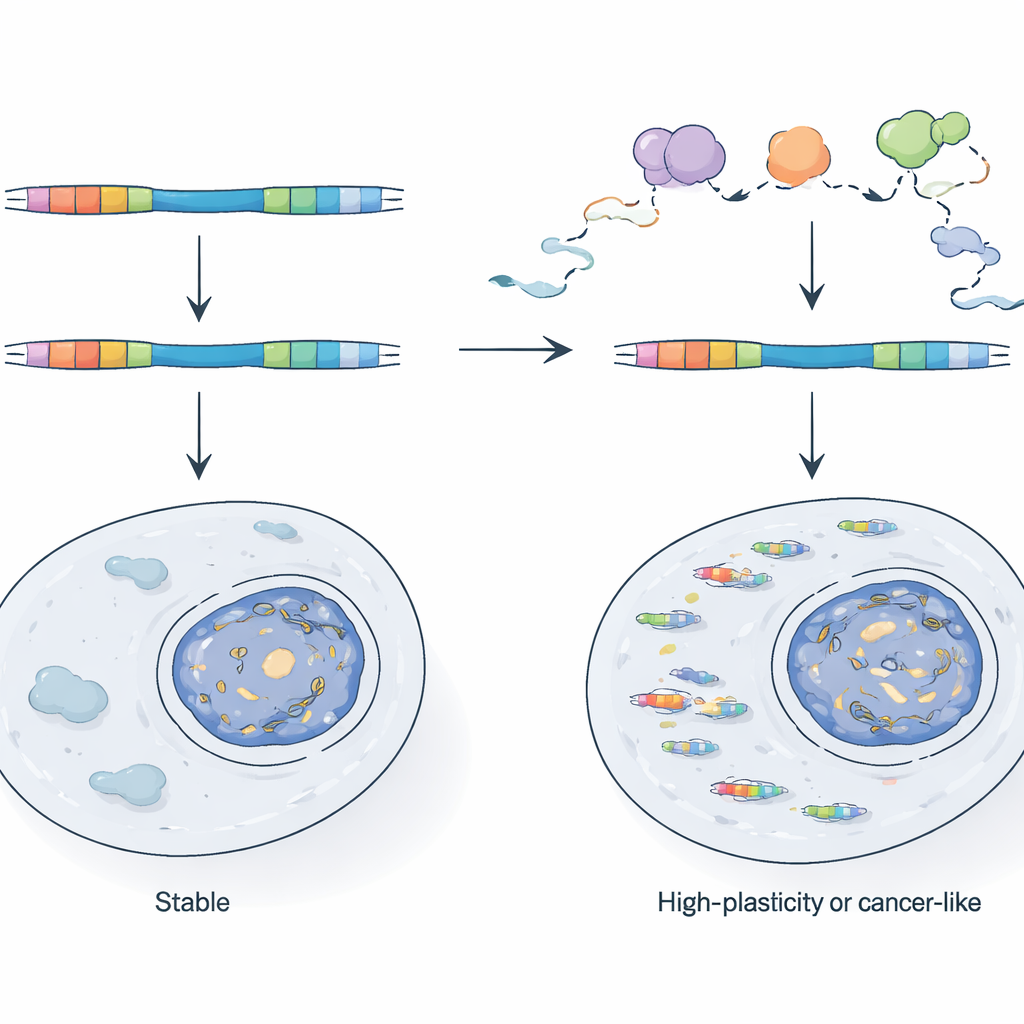
Hur celler håller virala hybrider i schack
Givet deras kraft, varför dominerar inte TE-kimera normala celler? Författarna visar att celler är beroende av ett RNA-kvalitetskontrollsystem, centrerat kring det nukleära exosomkomplexet, för att kontrollera och förstöra många av dessa transkript medan de bildas. När de genetiskt försvagar en nyckelkomponent i exosomet i musstamceller blir LTR-drivna promotorer mycket mer aktiva och kimära RNA ökar kraftigt. Genom att jämföra nybildat RNA med stabilt RNA visar de att vissa LTR vanligtvis hålls tillbaka eftersom deras transkript snabbt degraderas, medan andra kontrolleras på nivån hur ofta transkription startar. Dessa aktiva LTR tenderar att ligga i genomregioner som redan är tillgängliga och ofta transkriberade, vilket indikerar att det räcker att befinna sig nära en aktiv gen eller ett antisens-transkript för att ett viralt fragment ska undkomma traditionell epigenetisk tystnad.
Splicing, stamcellsplasticitet och en viral ”huvudströmbrytare”
Berättelsen blir mer invecklad när cellens splitsningsmaskineri störs. Författarna sänker uttrycket för flera centrala splitsningsfaktorer eller hämmar spliceosomen kemiskt och observerar ett gemensamt utfall med exosomförlust: en kraftig ökning av LTR-drivna kimera och av korta, intronfattiga gener. Bland vinnarna finns MERVL, ett endogent retrovirus aktivt i mycket tidiga musembryon. När MERVL:s interna sekvens och dess nedströms transkriptionsfaktorer uppregleras skiftar stamceller mot ett mer ”totipotent-liknande” tillstånd, vilket liknar tidiga embryonala celler som kan bilda alla vävnader. Omvänt dämpar nedbrytning av MERVL-RNA med antisens-oligonukleotider detta skifte och minskar LTR-promotoraktivitet, vilket visar att MERVL fungerar som en huvudströmbrytare som kan utlösa ett bredare nätverk av TE-kimera och celltillståndsplasticitet.
Viral innovation under evolutionen
Genom att jämföra många däggdjursgenom spårar teamet när olika TE-familjer började donera exoner till värdgener. I både människor och möss är relativt unga LTR-familjer särskilt benägna att bilda kimera i den ”sense”-orientering som kan läsas som en del av värdtranskript. Detta mönster tyder på att nya vågor av TE-insertioner upprepade gånger har försett genregulatoriska nätverk med råmaterial under evolutionär tid. Istället för att vara rent skadliga kan dessa insertioner testas av cellens transkriptions- och nedbrytningsmaskineri: de flesta tystas eller degraderas, men en minoritet hamnar på rätt plats och i rätt kontext för att bli upptagna som användbara regulatoriska element eller nya genstarter.
Varför dessa virala rester betyder något
För en icke-specialist visar detta arbete att en stor och en gång avfärdad del av vårt genom aktivt påverkar hur gener läses, hur celler ändrar identitet och hur sjukdomar utvecklas. Forntida virala sekvenser kan förvandlas till alternativa gen-”entréer”, producera hybrida RNA som normalt övervakas av cellulära städsystem. När den övervakningen eller normal splitsning sviktar kan dessa hybrider skjuta i höjden, skjuta stamceller mot mer flexibla tillstånd eller hjälpa tumörer att anpassa sig och motstå terapi. Under miljontals år har evolutionen upprepade gånger labbat med dessa virala fragment, förvandlat många från genomiska parasiter till byggstenar i regulatorisk komplexitet — och lämnat oss med ett transkriptom som är mycket mer plastiskt och dynamiskt än en enkel lista av gener skulle antyda.
Citering: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Nyckelord: transposabla element, kimära transkript, RNA-övervakning, stamcellsplasticitet, cancerevolution