Clear Sky Science · sv
Stressanpassning av mitokondriellt proteinimport genom OMA1-medierad nedbrytning av DNAJC15
Hur våra celler hanterar när deras kraftverk är under stress
Varje cell i din kropp är beroende av små strukturer kallade mitokondrier för att omvandla näring till användbar energi. Som miniatyrfabriker importerar mitokondrier ständigt nya delar—proteiner som byggts upp någon annanstans i cellen—för att hålla maskineriet igång. Denna artikel visar hur celler, när mitokondrier är stressade eller skadade, avsiktligt skruvar ned denna proteinimport. Genom att göra det skyddar de sig mot överbelastning och samordnar en bredare stressreaktion som involverar inte bara mitokondrierna utan även ett annat nyckelkompartment, det endoplasmatiska retikulumet.
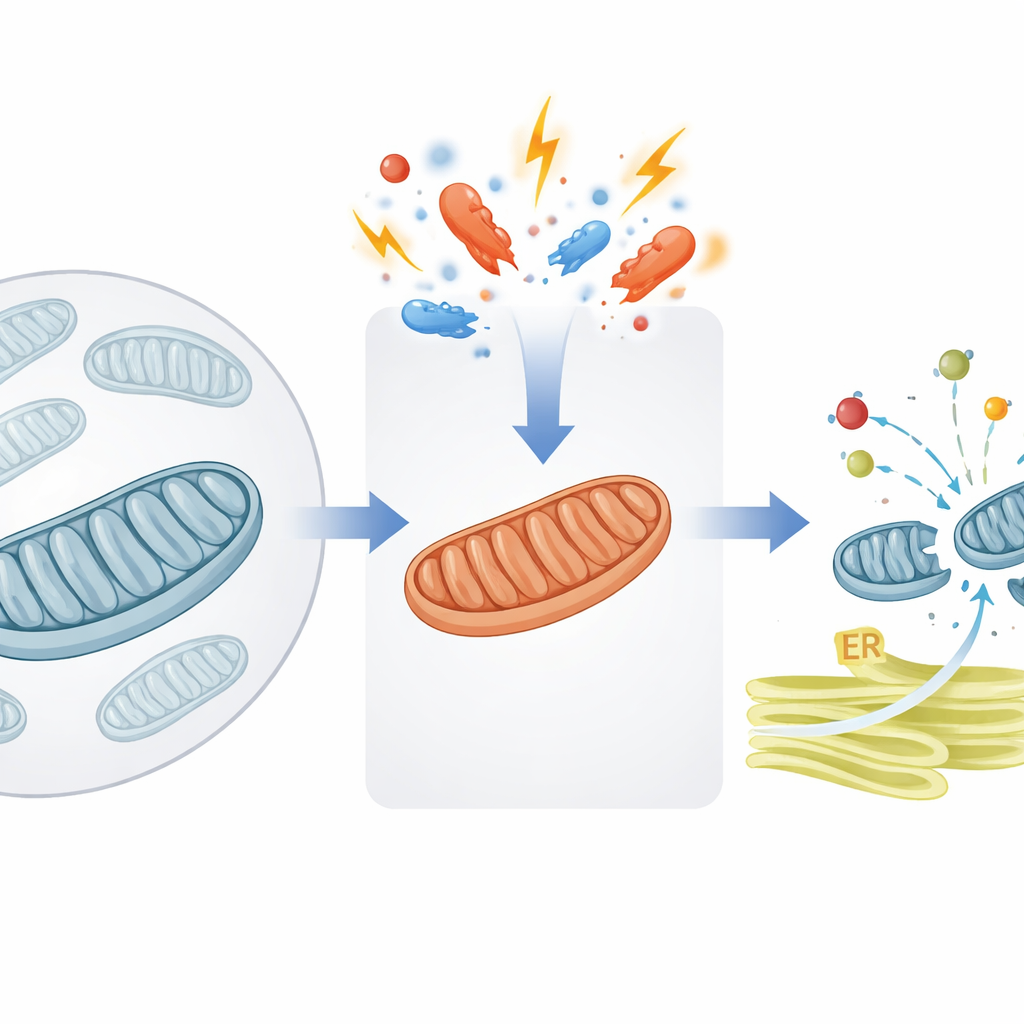
En säkerhetsventil för mitokondriell proteintrafik
Mitokondrier är beroende av tusentals proteiner som först byggs i cellens huvudkompartment och sedan skickas in. Författarna fokuserar på en avgörande port i mitokondriens inre membran, understödd av ett hjälpprotein som heter DNAJC15. Under normala förhållanden hjälper DNAJC15 till att dra nya protein"paket" genom importkanalen och in i mitokondriens inre, där många av dem blir en del av det energiproducerande maskineriet känt som oxidativ fosforylering (OXPHOS). Studien visar att när mitokondrier utsätts för stress—såsom nedsatt energiproduktion eller förändringar i membranets egenskaper—slår cellen om en molekylär brytare som ändrar hur mycket protein organellen är villig att importera.
OMA1: den stressaktiverade saxen
I centrum för denna brytare ligger ett stresskänsligt enzym kallat OMA1, inbäddat i det inre mitokondriella membranet. När mitokondrier får problem aktiveras OMA1 och klipper DNAJC15 vid en bestämd position nära dess början. Denna klyvning ger en förkortad variant av DNAJC15 som snabbt bryts ned av ett annat mitokondriellt enzymkomplex kallat m-AAA-proteaset. Som en följd försvinner den fullängds, importkompetenta formen av DNAJC15. Författarna visar att celler som saknar DNAJC15, eller där DNAJC15 snabbt förstörs efter OMA1-aktivering, har en minskad kapacitet att föra in nya proteiner i mitokondrier, särskilt sådana som behövs för att bygga och underhålla OXPHOS-komplexen.
Att bromsa energisammansättningen för att matcha mitokondriens tillstånd
Genom storskaliga proteinmätningar och importtester fann teamet att DNAJC15 är särskilt viktigt för att förse mitokondriens inre med proteiner involverade i genuttryck och montering av respirationskedjan. När DNAJC15 saknas ackumuleras dessa proteiner långsammare inne i mitokondrierna, och organellernas förmåga att förbruka syre och driva energiproduktion—as mätt i isolerade mitokondrier—minskar, särskilt för komplex I i respirationskedjan. En annan komponent i importkanalen, TIMM17A, samarbetar tätt med DNAJC15: att förlora båda ger särskilt starka brister i nivåerna av mitokondriella ribosomala proteiner och OXPHOS-komponenter. Tillsammans tyder dessa fynd på att OMA1-medierad nedbrytning av DNAJC15 är ett sätt att temporärt dämpa uppbyggnaden av nytt energimaskineri tills organellen återhämtat sig.
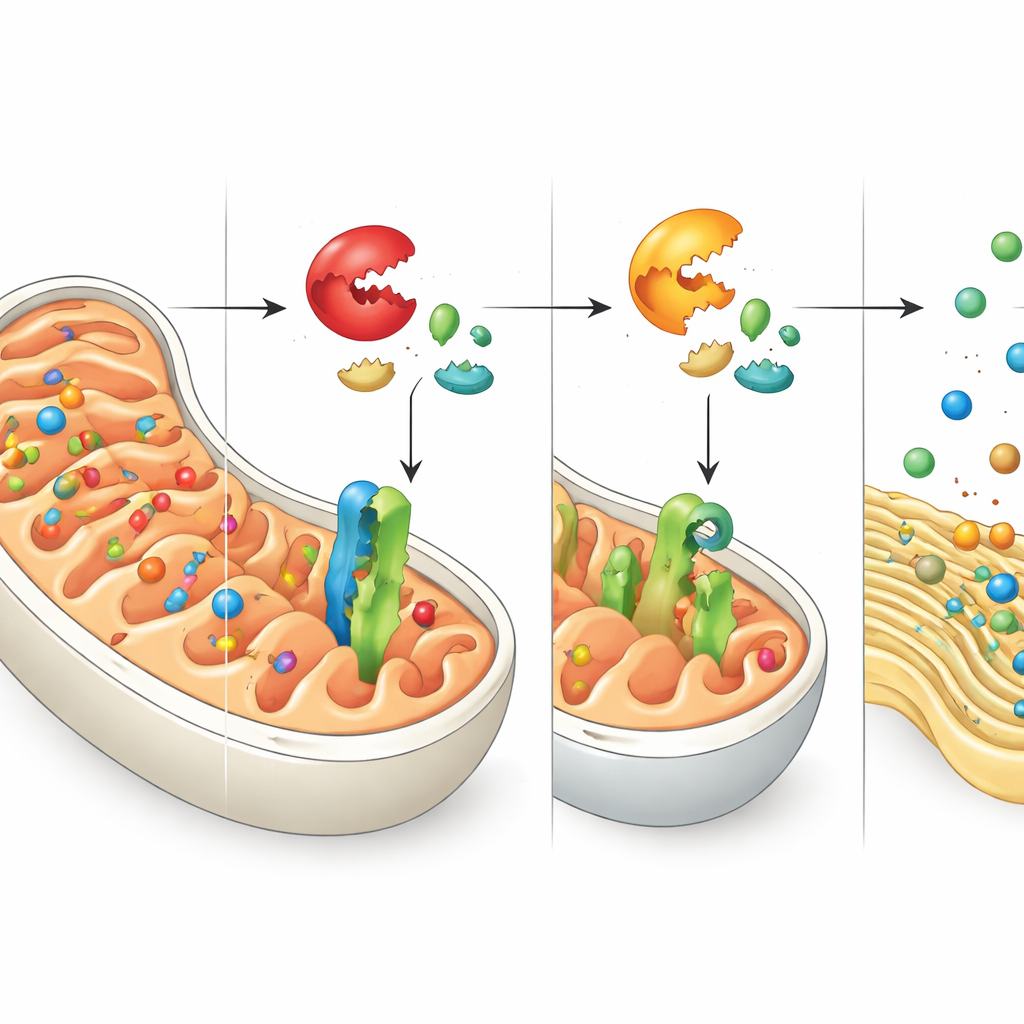
Fellevererade paket och en nödringning till ER
Att stänga av DNAJC15 stoppar inte cellen från att tillverka mitokondriella proteiner—det hindrar dem främst från att anlända till sin avsedda destination. Författarna följde var dessa strandade proteiner tar vägen och fann att många hamnar i det endoplasmatiska retikulumet (ER), ett nätverk av membran som normalt hjälper till att veckla och bearbeta andra proteinuppsättningar. Dessa felplacerade mitokondriella proteiner blir inbäddade i ER-membranen och stör ER:s egen kvalitetskontrollbalans. Som svar aktiverar cellen ett skyddsprogram känt som den ofolda proteinresponsen, specifikt genom en gren styrd av sensorn ATF6. Denna respons ökar ER:s kapacitet att hantera felveckade eller felplacerade proteiner och visar på en tät samordning mellan mitokondriell och ER-relaterad stresshantering.
En samordnad inbromsning för att skydda cellen
Sammantaget målar studien upp bilden av ett inbyggt bromssystem för mitokondriell biogenes. När mitokondrier befinner sig under stress trimmar OMA1 och indirekt förstör DNAJC15, vilket reducerar inflödet av nya, energirelevanta proteiner till komprometterade organeller. Några av dessa proteiner buffras temporärt vid ER, som i sin tur sätter igång ett eget skyddsprogram. Genom att koppla importkapaciteten till organellens hälsa, och genom att engagera ER som en reservplats för överskottsproteiner, kan celler undvika att täppa igen skadade mitokondrier och vinna tid för antingen reparation eller eliminering. För en lekmans betraktare visar detta arbete hur djupt integrerade våra cellulära kvalitetskontrollsystem är: även de minsta missstegen i ett kompartment upptäcks och balanseras av andra för att hålla energiproduktionen—och livet självt—på rätt kurs.
Citering: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Nyckelord: mitokondriell stress, proteinimport, cellulär kvalitetskontroll, oxidativ fosforylering, endoplasmatiskt retikulum