Clear Sky Science · sv
Struktur och funktion hos jästens aminosyra-kännande SEAC–EGOC-superkomplex
Hur celler bestämmer när de ska växa
Varje cell måste ständigt avgöra om den har resurser att växa eller om den bör spara. Det beslutet beror i hög grad på aminosyror, proteinerna byggstenar och en viktig kvällkälla för kväve. Denna artikel avslöjar, i anmärkningsvärd strukturell detalj, hur jästceller känner av aminosyrors tillgänglighet via en jättelik molekylär sammansättning och använder den informationen för att slå på eller av en huvudregulator för tillväxt, kallad TORC1. Eftersom samma krets är bevarad i mänskliga celler och kopplad till cancer och ämnesomsättning, ger insikter från jäst en inblick i hur våra egna celler bedömer när förhållandena är rätt för tillväxt.
En intrikat nav på cellens återvinningscentral
I jäst sitter ett centralt beslutsfattande komplex som kallas SEAC på vakuolens membran, ett organell som fungerar som cellens återvinningscentral. Där möter det ett annat komplex, EGOC, som förmedlar information om aminosyranivåer. Tillsammans förmedlar de signaler till TORC1, huvudbrytaren för tillväxt. SEAC har två funktionella halvor: SEACIT, som kan stänga av TORC1, och SEACAT, som länge antagits hålla SEACIT i schack. Författarna använde högupplöst kryo‑elektronmikroskopi för att visualisera hela SEAC bundet till EGOC och fånga en ögonblicksbild av detta molekylära nav exakt där signaleringen sker, på vakuolens yta. 
Att se den molekylära arkitekturen på nära håll
Strukturen visar SEAC som en stor kärna byggd av SEACAT‑subenheter, från vilken två flexibla ”vingar” av SEACIT sträcker sig. Varje vinge kan binda ett EGOC‑komplex, vilket innebär att en enda SEAC kan ta emot två signalinmatningar samtidigt. Slående nog fäster EGOC endast vid vingarna och inte vid kärnan, och SEAC:s övergripande form förändras knappt när EGOC är närvarande. Det visar att SEACAT inte fysiskt blockerar den aktiva ytan på SEACIT och inte hindrar EGOC från att binda. Komplexets orientering på vakuolmembranet placerar dessutom SEAC‑kärnan mot cytoplasman, där den kan interagera med ytterligare regulatorer, medan vingarna ligger nära membranet, idealiskt placerade för att kontakta EGOC och andra membranankrade partners.
Hur SEAC väljer rätt signal
Författarna zoomade in på kontakterna mellan SEAC och EGOC och fann att SEAC känner igen endast den ”aktiva” versionen av EGOC, där en av dess små GTPaser, Gtr1, bär en GTP‑liknande nukleotid, medan dess partner Gtr2 har GDP. SEACIT tillhandahåller ett katalytiskt ”finger” som når in i Gtr1:s nukleotidficka och påskyndar nedbrytningen av GTP, vilket vänder EGOC från ett aktivt tillstånd till ett inaktivt. Detaljerade kryo‑EM‑kartor och mutationsstudier visar att detta katalytiska finger och en närliggande hjälpresidua är avgörande för interaktionen och för att korrekt läsa nukleotidstatus. När författarna förändrade dessa nyckelresiduer lokaliserade SEAC inte längre korrekt till vakuolen, och EGOC kunde inte engagera sig produktivt.
Snabbt vs långsamt kontroll av tillväxtbrytaren
För att förstå vad detta betyder för den levande cellen följde forskarna TORC1‑aktiviteten över tid när aminosyror avlägsnades och sedan återinfördes. I normala celler slås TORC1 snabbt av inom några minuter efter kväve‑svält och slås sedan snabbt på igen när aminosyrorna återvänder. När det katalytiska fingret i SEACIT avaktiverades, eller när SEACIT‑subenheter togs bort, svarade TORC1 knappt i detta tidiga tidsfönster. Detsamma gällde när både Gtr1 och Gtr2 togs bort, vilket visar att SEAC–EGOC‑paret är den dominerande, snabba vägen för aminosyrakontroll av TORC1. Men vid senare tidpunkter—runt en halvtimme—justerade sig TORC1‑aktiviteten långsamt även i dessa mutanter, vilket indikerar att en separat, långsammare väg till TORC1, oberoende av detta GTPas‑system, också är verksam i cellerna.
En överraskande roll för en avlägsen subenhet
En särskilt fascinerande upptäckt rör Sea2, en SEACAT‑komponent med en flexibel ”propeller”‑domän som sticker ut från kärnan. Att ta bort Sea2, eller bara dess propeller, gav signaleringsdefekter nästan identiska med de som uppstår när SEAC:s katalytiska aktivitet förloras: TORC1 svarade trögt både vid aminosyra‑borttagning och återmatning. Ändå sitter Sea2 långt från den katalytiska platsen och rör inte direkt SEACIT‑vingen, vilket gör en enkel blockeringsmekanism osannolik. Genetiska experiment som kombinerade Sea2‑bortfall med en katalytiskt död SEAC‑variant föreslog att att låsa GAP‑aktiviteten fullt på eller fullt av båda stör det snabba svaret, medan en intermediär reglering behövs. Författarna föreslår att Sea2:s propeller fungerar som en dockningsplattform för en okänd faktor som dämpar SEACIT:s aktivitet och tillåter cellerna att finjustera TORC1 istället för att helt enkelt slå av den permanent.
Vad detta betyder för beslut om celltillväxt
Sammantaget omformulerar studien SEAC inte som två motsatta enheter utan som en enda, integrerad maskin vars katalytiska vinge (SEACIT) och strukturella kärna (SEACAT) samarbetar för att känna av aminosyror och snabbt justera tillväxtbrytaren TORC1. SEACIT:s enzymatiska verkan på EGOC ger den snabba, precisa kontrollen, medan Sea2:s propeller sannolikt rekryterar regulatorer som modulerar denna aktivitet. Samtidigt säkerställer långsammare, parallella vägar att TORC1 ändå så småningom speglar näringstillståndet även om huvudsensorn är störd. Eftersom nära besläktade komplex utför samma uppgift i mänskliga celler, belyser dessa insikter från jäst hur våra egna celler väger tillväxt mot näringstillgång, med konsekvenser för att förstå sjukdomar där TORC1‑signalering går fel.
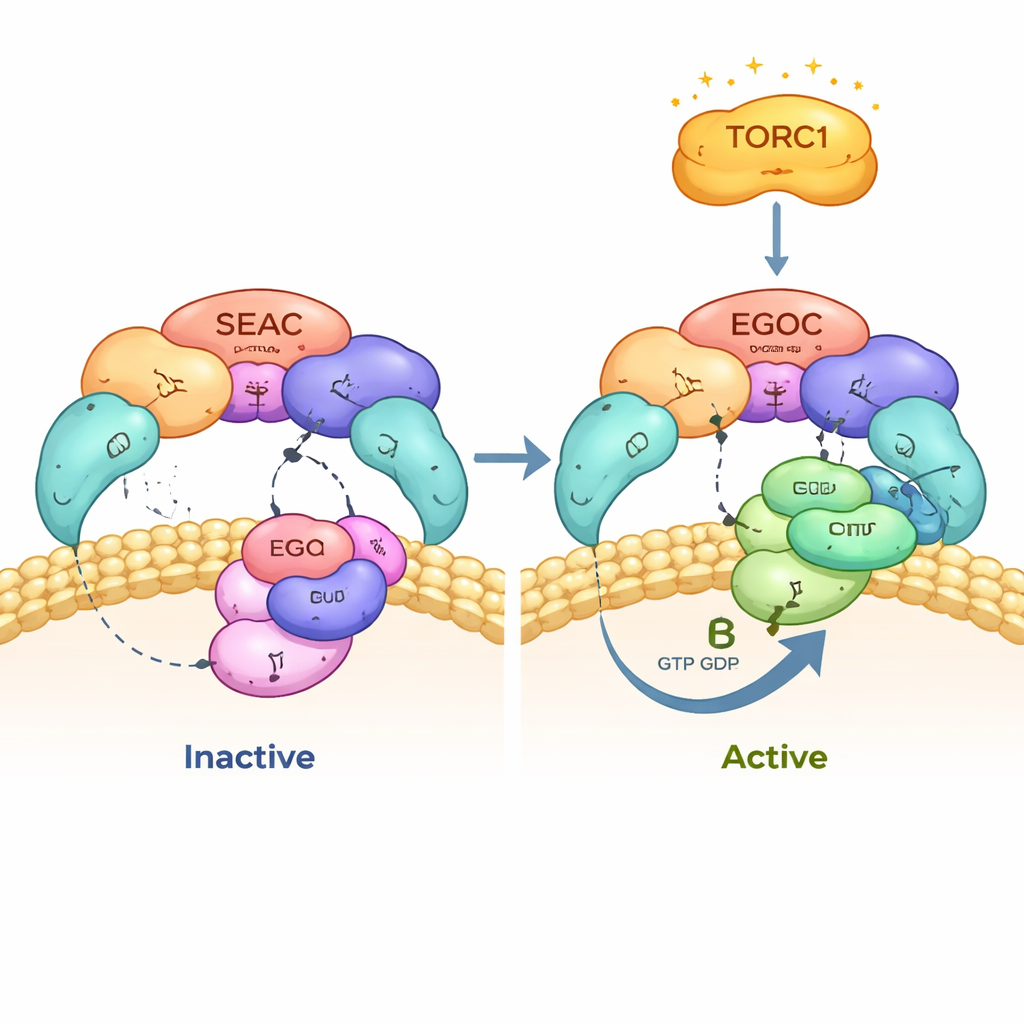
Citering: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Nyckelord: amino syroravkänning, TORC1-signalering, SEAC GATOR-komplex, kontroll av celltillväxt, kryoelektronmikroskopi