Clear Sky Science · sv
PopZ-kondensatets filamentösa ultrastruktur krävs för dess cellulära funktion
Hur celler använder mjuka droppar för att hålla ordning
Inuti varje levande cell är kemin trång och kaotisk. Ändå lyckas celler placera avgörande molekyler på rätt plats vid rätt tid. Ett sätt de gör detta på är genom att bilda små vätskeliknande droppar, eller kondensat, som samlar vissa proteiner samtidigt som andra utesluts. I denna studie studeras ett sådant droppbildande protein i bakterier, kallat PopZ, och visar att dess interna skelett av små fibrer är avgörande för att cellens livsviktiga processer ska fungera korrekt.
En mikroskopisk organisatör vid cellens poler
I bakterien Caulobacter crescentus samlas PopZ vid cellens två ändar, eller poler, där det bildar koncentrerade områden. Dessa PopZ-berikade ”mikrodomäner” hjälper till att styra cellcykeln genom att attrahera specifika partnerproteiner och förankra kromosomen under delning. När PopZ tas bort delar cellerna sig dåligt, tappar sin normala form och hanterar sitt DNA felaktigt. Tidigare arbete visade att om PopZ-droppar är för rinniga eller för stela får cellerna också problem. Vad som var okänt var hur den detaljerade strukturen inuti dessa droppar — sättet PopZ-molekylerna monteras till större former — ger upphov till deras materialegenskaper och till korrekt cellulärt beteende.
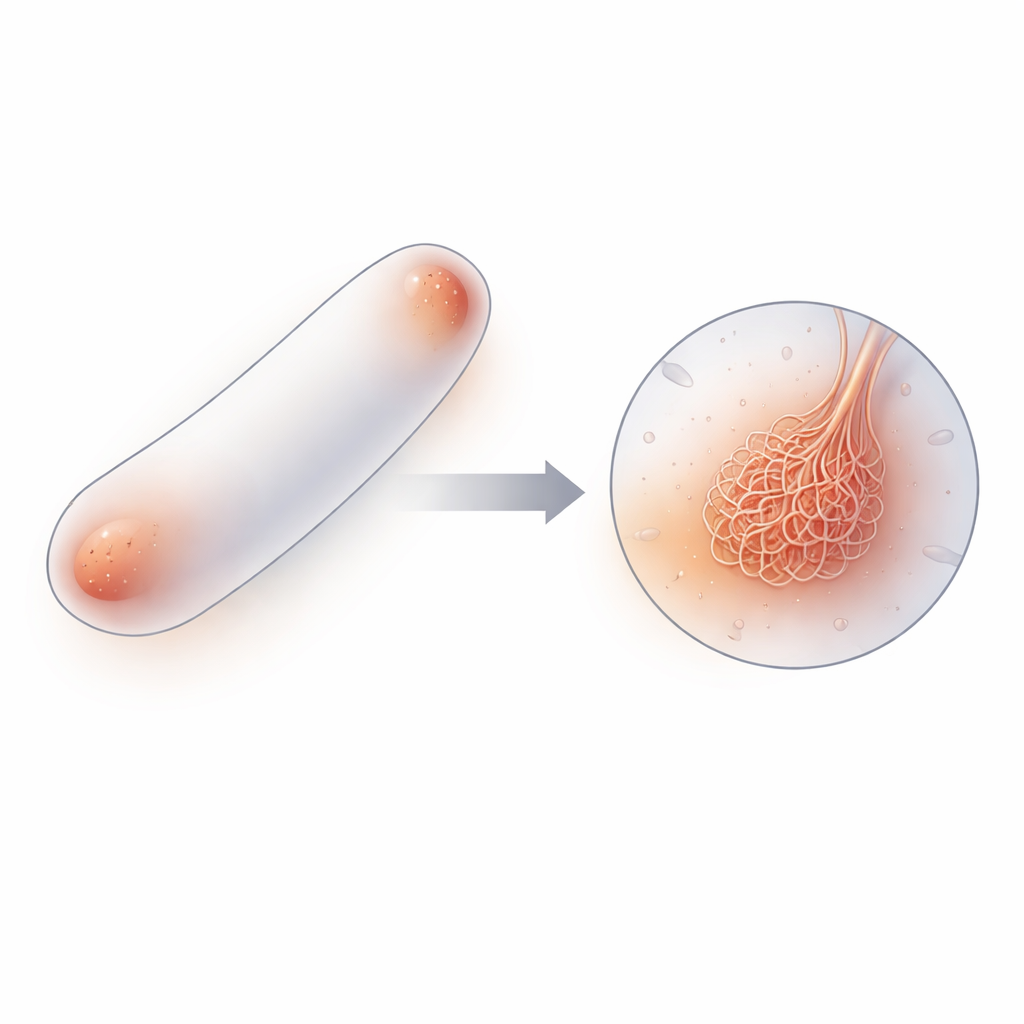
Från enskilda molekyler till ett nätverk av fibrer
Med en kombination av kryo-elektrontomografi (en 3D-avbildningsmetod vid mycket låga temperaturer), biokemiska tester, enkelmolekylsfluorescens och datorsimuleringar kartlade författarna hur PopZ-molekyler monteras över flera skalor. Enskilda PopZ-proteiner går först ihop i trepartsenheter (trimrar), som sedan parar sig för att bilda sexpartsenheter (hexamerer). Dessa hexamerer staplas ända-till-ända till korta, flexibla fibrer tiotals nanometer långa, och sammanflätade nätverk av dessa fibrer bygger upp PopZ-kondensatet. Avbildning av både renade PopZ-droppar och PopZ i intakta celler visade samma filamentösa nätverk, vilket visar att denna arkitektur inte är en artefakt av provrörsförsök utan en kärnmekanism i hur PopZ fungerar i levande bakterier.
Inbyggda bromsar och brytare för droppbildning
PopZ består av distinkta sektioner som var och en spelar en annan roll i denna monteringskedja. Ett kompakt helixsegment i svansänden fungerar som huvudmodul för oligomerisering och fibrbildning, tillräckligt kraftfullt i sig för att bygga fibrer och droppar. I kontrast tenderar en lös, negativt laddad del i mitten att hålla molekylerna isär, vilket försvårar kondensation. I motsatt ände rekryterar en kort helix klientproteiner och, i den utspädda staten, viker den tillbaka för att kontakta svansen och motverkar därigenom förtida klumpbildning. När omständigheterna förändras — till exempel när vissa salter är närvarande — försvagas dessa repulsiva interaktioner. PopZ skiftar då form: klientbindande helixen svänger bort från svansen, det hämmande molnet av oordnade segment öppnar upp, hexamerer staplas lättare till fibrer och inter-fiberkontakter blir gynnsamma. Denna fassberoende konformationsändring innebär att samma proteinregion som blockerar bindning i den utspädda staten blir en aktiv dockningsplats när ett kondensat väl har bildats.
Vad som händer när fibrerna tas bort
För att se hur fibrerna påverkar droppens fysikaliska beteende konstruerade teamet PopZ-mutanter som fortfarande kunde bilda hexamerer men inte stapla dem till fibrer. Dessa varianter producerade visserligen kondensat, men med slående olika egenskaper. Istället för att bilda prydliga sfärer som sitter på ytan plattades dropparna ut och spreds, vilket indikerar lägre ytspänning och starkare våtning av omgivningen. Inom dessa fibrerfattiga kondensat rörde sig både PopZ självt och dess klientproteiner mycket snabbare, mätt med fluorescensåterhämtning efter fotoblekning. Med andra ord gjorde borttagandet av fibrer dropparna mjukare och mer genomsläppliga. När sådana mutanter infördes i Caulobacter-celler störde de normal PopZ-aktivitet vid polerna, påverkade kromosomförankringen och försämrade tillväxten kraftigt, även när vildtyp-PopZ fortfarande fanns närvarande. Andra konstruerade varianter visade motsatt missanpassning: de kunde bilda fibrer men misslyckades med att kondensera effektivt, och dessa kunde inte heller fullt ut ersätta PopZ:s cellulära roll.
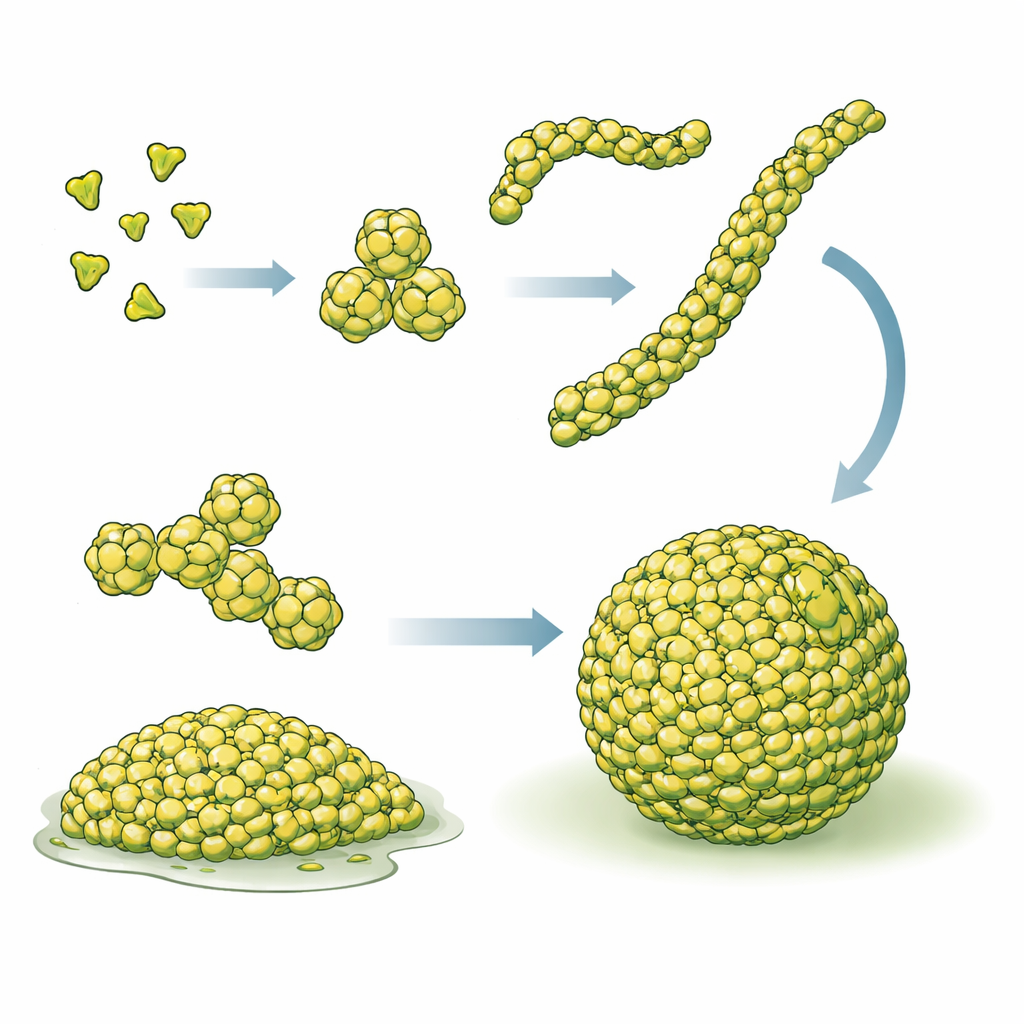
En receptbok för funktionella cellulära droppar
Arbetet visar ett tydligt budskap för icke-specialister: det räcker inte att ett protein som PopZ bara klumpar ihop sig, och det räcker inte att bilda fibrer isolerat. Det som betyder något för cellfunktionen är en mycket specifik ultrastruktur — kondensat som i sig består av korta, sammankopplade fibrer. Detta filamentösa ramverk ökar antalet kontaktpunkter mellan molekyler, höjer droppens ytspänning, saktar ner rörelsen hos viktiga klienter och tillhandahåller en inbyggd molekylär brytare som slår på klientbindning först i den täta fasen. Genom att spåra denna kedja av orsak och verkan från aminosyrasekvens till molekylära samlingar till hela cellens beteende erbjuder studien en generell ritning för hur celler kan avväga ”känslan” hos sina mjuka interna droppar för att styra livsviktiga processer.
Citering: Scholl, D., Boyd, T., Latham, A.P. et al. The filamentous ultrastructure of the PopZ condensate is required for its cellular function. Nat Struct Mol Biol 33, 420–432 (2026). https://doi.org/10.1038/s41594-025-01742-y
Nyckelord: biomolekylära kondensat, proteinfibrer, cellpolaritet, fasseparation, bakteriell celcykel