Clear Sky Science · sv
Mechanism and reconstitution of circadian transcription in cyanobacteria
Varför kroppsklockor spelar roll, även för bakterier
Alla levande varelser, från människor till mikroskopiska mikrober, håller tid. Dessa interna klockor hjälper organismer att förutse soluppgång och solnedgång och planera aktiviteter som födosök, reparation och tillväxt. Denna artikel undersöker hur en enkel fotosyntetisk bakterie, Synechococcus elongatus, använder en proteindriven klocka för att slå på och av gener med anmärkningsvärd precision över ett 24-timmarsdygn. Genom att återskapa detta tidtagarsystem i ett reaktionsrör visar forskarna en nedskalad version av en biologisk klocka som kan inspirera nya verktyg för bioteknik och syntetisk biologi.
En liten klocka som drivs av kemi
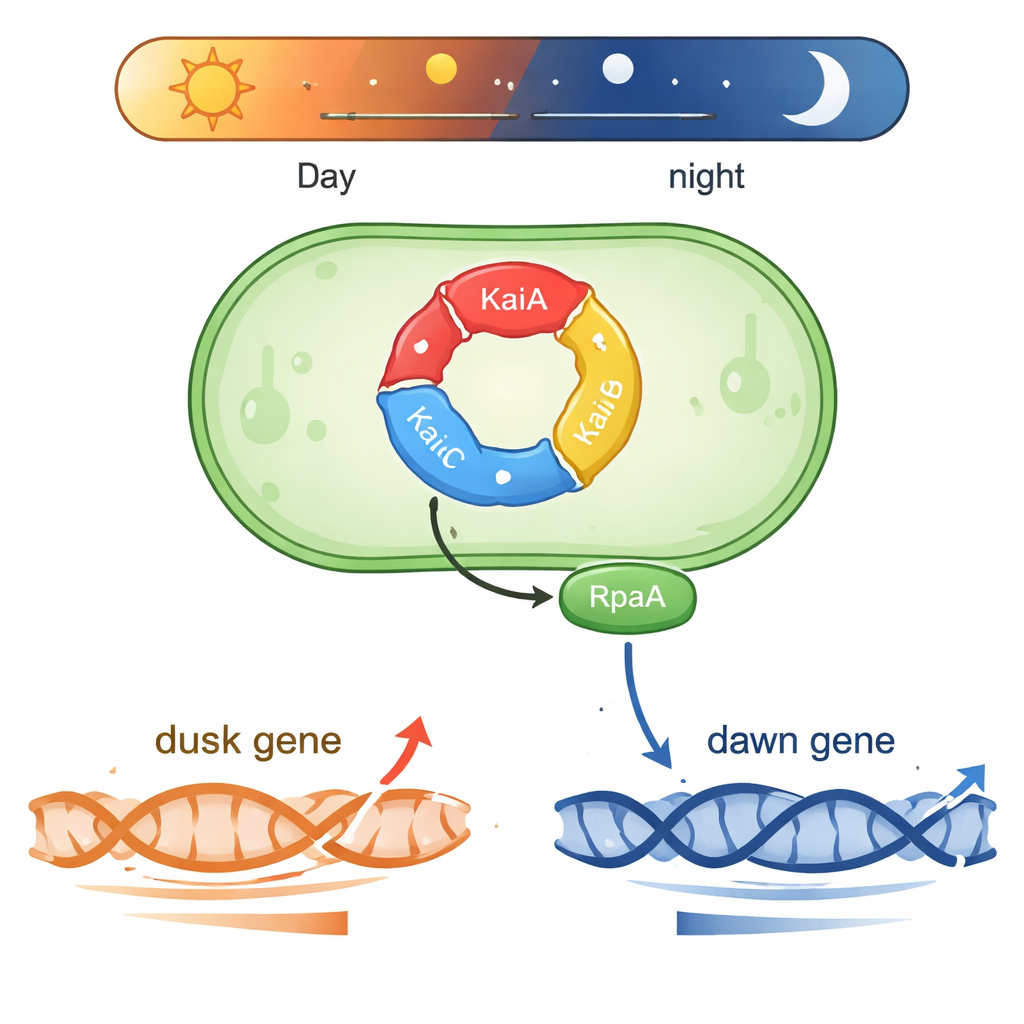
Synechococcus lever i solbelysta vatten och behöver förutsäga dagliga ljusförändringar. I dess centrum finns en tredelad proteinkonstruktion bestående av KaiA, KaiB och KaiC. Dessa proteiner för fosfatgrupper mellan varandra i en upprepad cykel som tar ungefär 24 timmar och bildar ett biokemiskt ”växelverk” som håller tiden även utanför cellen. Två andra proteiner, SasA och CikA, läser av KaiC:s fosforyleringsstatus och använder den för att styra ett annat protein, RpaA. När RpaA är fosforylerat binder det DNA och fungerar som en huvudomkopplare för hundratals gener som stiger och faller antingen kring subjektiv ”gryning” eller ”skymning” i konstant ljus.
Ett protein, två motsatta genprogram
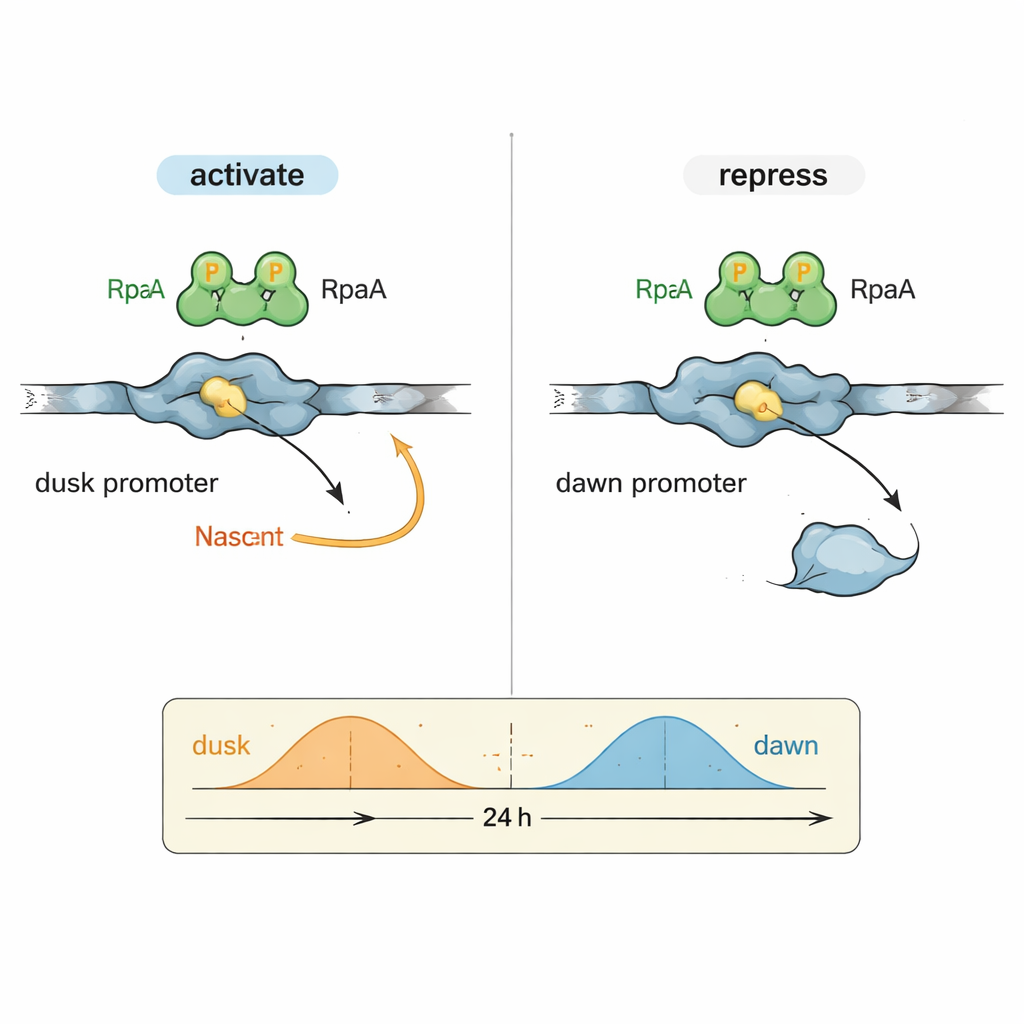
Ett gåtfullt problem inom cirkadbiologi har varit hur en enda utgångsfaktor, RpaA, kan samordna gener som når sina toppar vid mycket olika tidpunkter på dygnet. Författarna fokuserade på två representativa DNA-kontrollregioner (promotorer): kaiBC, som är mest aktiv vid skymning, och purF, som når sin topp vid gryning. I kontrollerade reaktioner med renat cyanobakteriellt RNA-polymeras och RpaA visade de att fosforylerat RpaA ökar transkriptionen från kaiBC-promotorn samtidigt som det minskar transkriptionen från purF-promotorn. Detaljerade footprinting-experiment kartlade exakt var RpaA binder på varje DNA-bit och avslöjade att dess position i förhållande till de vanliga promotorelementen avgör om det fungerar som accelerator eller broms.
Se klockans strömbrytare i atomär detalj
För att förstå detta dubbla beteende på molekylär nivå använde teamet högupplösande kryo-elektronmikroskopi för att fånga strukturen av RpaA bundet till kaiBC-promotorn tillsammans med RNA-polymeras. Bilderna visar RpaA som greppar DNA som ett asymmetriskt par och kontaktar två nyckeldelar av enzymet: alfaunderenhetens svans och en region av sigmafaktorn som normalt känner igen promotersekvenser. Dessa kontakter böjer DNA och hjälper till att positionera RNA-polymeraset vid en något omdefinierad startplats för transkription. Väl avvägda mutationer som försvagar någon av dessa kontaktpunkter minskar eller abolierar aktiveringen av kaiBC, både in vitro och i levande celler, vilket bekräftar att fysisk rekrytering av RNA-polymeras ligger bakom skymningsfasens genaktivering.
Bygga en klockstyrd gen från grunden
Eftersom det innata cyanobakteriella RNA-polymeraset är komplext och svårt att hålla aktivt i flera dagar vände forskarna sig nästa till det mycket enklare T7-bakteriofagpolymeraset, som ofta används i laboratorier. RpaA kan inte rekrytera detta orelaterade enzym, men det kan fortfarande blockera det genom att sitta på DNA. Teamet konstruerade en syntetisk DNA-mall där en T7-promotor driver en fluorescerande RNA-rapportör (“Broccoli”), med en RpaA-bindningsplats placerad nedströms. När de kombinerade denna mall med KaiA–KaiB–KaiC-klockan, CikA-kinas/fosfatas, RpaA och T7-polymeras i en enda optimerad buffert observerade de ökande och avtagande transkriptionshastigheter med en period på cirka 24 timmar. Rytmen kunde nollställas genom att ändra ATP-till-ADP-förhållandet och körde med nästan samma period över ett temperaturområde — klassiska kännetecken för en verklig cirkadisk klocka.
Från enkla klockor till konstruerad tidhållning
Studien visar att endast sex proteiner är tillräckliga för att koppla en kemisk pacemaker till rytmisk genavläsning: de tre Kai-klockproteinerna, CikA, RpaA och ett RNA-polymeras. Genom att ändra var RpaA sitter på DNA kan samma molekyl få vissa gener att nå topp vid skymning och andra vid gryning, vilket hjälper till att förklara de komplexa vågorna av genaktivitet som ses i cyanobakterier. Eftersom repressionsbaserad utformning fungerar även med ett främmande polymeras som T7 bör det vara möjligt att transplantera denna minimala klockmodul till andra mikrober eller cellfria system, vilket gör det möjligt för forskare att programmera gener att slå på och av med dagliga rytmer för forskning, industriell produktion eller framtida terapeutiska tillämpningar.
Citering: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Nyckelord: circadian clock, cyanobacteria, transcription regulation, RpaA, synthetic biology