Clear Sky Science · sv
Cereblon förmår G3BP2 som neosubstrat att degraderas genom molekylär ytmimikry
Att göra cellulär städning till ett smart riktverktyg
Moderna läkemedel försöker i allt högre grad åtgärda sjukdomar inte bara genom att blockera skadliga proteiner utan genom att avlägsna dem helt. Denna studie undersöker en smart metod för att omprogrammera en av cellens egna ”städmaskiner” så att den, i kombination med ett litet molekylärt ämne, kan känna igen och förstöra ett protein kopplat till cancer och andra störningar. Arbetet avslöjar ett oväntat knep: städmaskinen omformar en del av sin yta för att efterlikna en av proteinets naturliga partners, vilket gör att den kan haka fast och skicka proteinet till cellens sopstation.
Cellens sopinsamlande maskin med dold flexibilitet
Våra celler märker ständigt ut slitna eller oönskade proteiner för nedbrytning med ett system centrerat kring E3-ligasernas komplex—stora proteinkomplex som bestämmer vad som bör kasseras. Ett sådant komplex är beroende av en komponent kallad cereblon, som fungerar som en sensor som känner igen specifika egenskaper (”degroner”) på andra proteiner. Vissa godkända läkemedel utnyttjar redan cereblon genom att verka som ”molekylära lim”: de binder till cereblon och skapar en ny dockningsyta som drar till sig sjukdomsrelaterade proteiner, som då taggas och degraderas. Hittills använde de flesta kända mål ett särskilt strukturmönster, vilket gjorde att antalet proteiner som kunde avlägsnas på detta sätt verkade begränsat.
Upptäckten av ett nytt mål utanför de gamla reglerna
I den nya studien screenade författarna en samling cereblonfokuserade molekylära lim i humana celler och identifierade en förening kallad MRT-5702. Denna lilla molekyl orsakade en snabb förlust av ett protein med namnet G3BP2, som hjälper till att hantera RNA och ingår i stressgranuler—aggregat kopplade till cancer, hjärtproblem och neurodegenerativa sjukdomar. Viktigt är att G3BP2 saknar det vanliga degronmönster som cereblon känner igen. Uppföljande cellexperiment, inklusive känsliga ljusbasserade avläsningar av proteinproximitet, bekräftade att MRT-5702 drar samman cereblon och G3BP2 i ett tredelat komplex som leder till G3BP2-degradering, samtidigt som dess närbesläktade syskonprotein G3BP1 i regel lämnas orört om inte dess nyckeldomän byts ut.
Imitation som bindningsstrategi
När forskarna gick djupare frågade de hur G3BP2 kunde binda cereblon utan det standardmässiga igenkänningsmotivet. Istället för att söka efter likheter mellan G3BP2 och kända cereblonmål vände de på frågan: kunde cereblon likna en av G3BP2:s vanliga bindningspartners? G3BP-proteiner interagerar ofta med andra molekyler via en hotspot på en region kallad NTF2-lik domän, som normalt känner igen korta sekvensmotiv. Med strukturella modeller av G3BP2:s naturliga partner USP10 skannade teamet cereblons yta beräkningsmässigt och fann en yta på en mindre förstådd region, LON-domänen, som nära efterliknar formen och kemin hos USP10:s bindningsmotif. Att mutera bara ett fåtal nyckelaminosyror på denna yta, eller i G3BP2-hotspotten, försvagade det tredelade komplexet, vilket tyder på att cereblon i praktiken låtsas vara USP10 för att docka mot G3BP2.
Fånga den nya gränsytan i atomär detalj
För att visualisera denna ovanliga interaktion använde teamet högupplöst kryo-elektronmikroskopi för att lösa strukturen av ett komplex innehållande cereblon, en annan kärnligaskomponent, MRT-5702 och NTF2-liknande domänen av G3BP2. Bilderna visade att en flexibel loop i cereblons LON-domän böjer sig och omformar sig för att utgöra nästan halva kontaktytan med G3BP2. Den aktiva spegelbildsformen av MRT-5702 sitter i cereblons vanliga läkemedelsbindningsficka men hjälper, tillsammans med loopen, till att skapa en vid landningsplatta som omsluter ena halvan av G3BP2-dimeren. Slående nog använder denna ordning knappt den kanoniska cereblonplats som hanterar tidigare limmål, vilket visar att cereblon kan engagera mycket olika regioner av sin yta beroende på limmet och det protein som är involverat. Samtidigt förblir den orörda halvan av G3BP2-dimeren tillgänglig för bindning av andra partners, vilket ger en rimlig förklaring till ”kollateral” nedbrytning av proteiner som råkar sitta bundna.
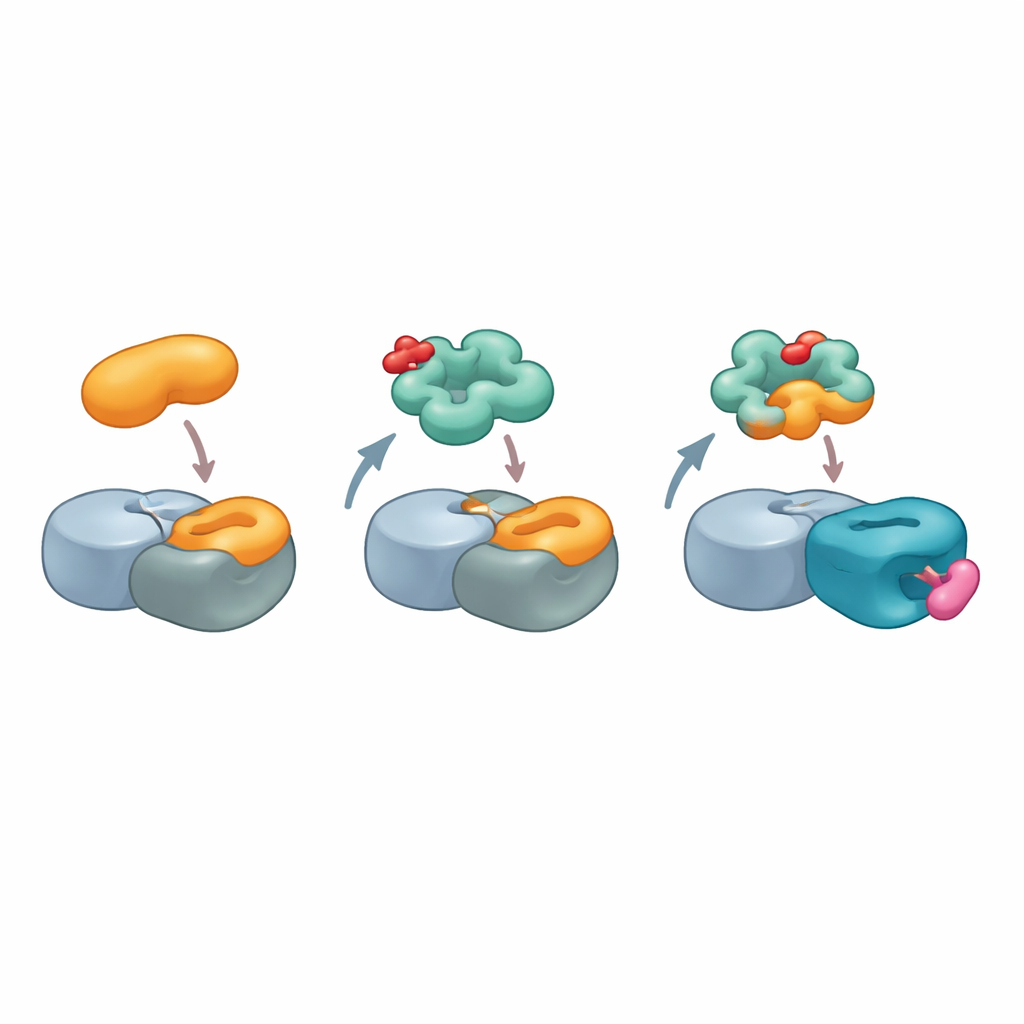
Glueprints för framtida läkemedelsdesign
Tillsammans målar fynden upp cereblon som en betydligt mer mångsidig matchmaker än man tidigare uppskattat. Istället för att kräva att mål bär på en enda typ av degron kan cereblon, när den är beväpnad med rätt molekylära lim, forma en sammansatt yta som imiterar naturliga protein–protein-kontakter någon annanstans i cellen. Författarna föreslår att sådana kombinerade protein-och-lim-y tor, som de kallar ”glueprints”, skulle kunna kartläggas och utformas för att efterlikna befintliga interaktionshotspots på många sjukdomsrelaterade proteiner. För en allmän läsare är huvudbudskapet att läkemedelsutvecklare kanske inte behöver upptäcka helt nya bindningsfickor på problematiska proteiner; istället kan de lära cellens egna återvinningsmaskineri att känna igen dessa proteiner genom att skickligt kopiera formerna av deras vanliga partners, vilket kraftigt vidgar menyn av mål som kan tas bort säkert och selektivt.
Citering: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Nyckelord: molekylära lim-degraderare, cereblon, målstyrd proteinnedbrytning, G3BP2, protein–protein-interaktioner