Clear Sky Science · sv
Ställningar med optimerad kvartär symmetri för de novo cryoEM-strukturdeterminering av små RNA
Att se RNAs minsta former
Inuti varje cell veckar korta RNA-strängar sig till små tredimensionella former som slår på och av gener, känner av cellulär skada eller lyser upp under ett mikroskop. Många av dessa RNA är så små att dagens avbildningsmetoder har svårt att avslöja deras precisa arkitektur. Denna artikel presenterar ett smart sätt att göra dessa svårfångade molekyler synliga: genom att fästa dem på en större, självmonterande RNA‑"ram" som tydligt kan ses med kryo‑elektronmikroskopi, en kraftfull teknik som avbildar frusna biomolekyler.
Bygga en hjälpsam RNA‑ram
Forskarlaget utgick från ett RNA‑segment från ett virus som naturligt tenderar att parar sig i en tvådelad struktur. De redesignade segmentet så att det, istället för att bara bilda par en liten del av tiden, nu nästan alltid monteras till högst regelbundna två‑ eller fyrdelade former i lösning. Dessa upprepande arrangemang skapar i praktiken en RNA‑ram, eller scaffold, med inbyggd symmetri. Symmetri är värdefull för kryo‑elektronmikroskopi eftersom identiska upprepade enheter kan medelvärdesbildas, vilket skärper slutbilden.
Fästa kända RNA som testgäster
För att testa om deras ställning kunde bära andra RNA in i sikte, ympade forskarna välstuderade molekyler på en region av ramen. En gäst var ett transfer‑RNA från bakterier, en klassisk L‑formad molekyl som levererar aminosyror under proteinsyntes. En annan var Mango‑III, ett litet konstruerat RNA som binder ett färgämne och lyser, ofta använt som ett fluorescerande fästmärke. I båda fallen veckade sig de kombinerade molekylerna och parade sig som avsett, och kryo‑elektronmikroskopi gav detaljerade kartor över de övergripande formerna. För transfer‑RNA:t var bilderna tillräckligt skarpa för att urskilja subtila skillnader mellan den omodifierade formen som användes här och tidigare studerade, kemiskt modifierade versioner. För Mango‑III visade kartorna att aptameren blir mycket mer styv när dess färgämne är bundet, vilket förklarar hur bindningen slår på fluorescensen. 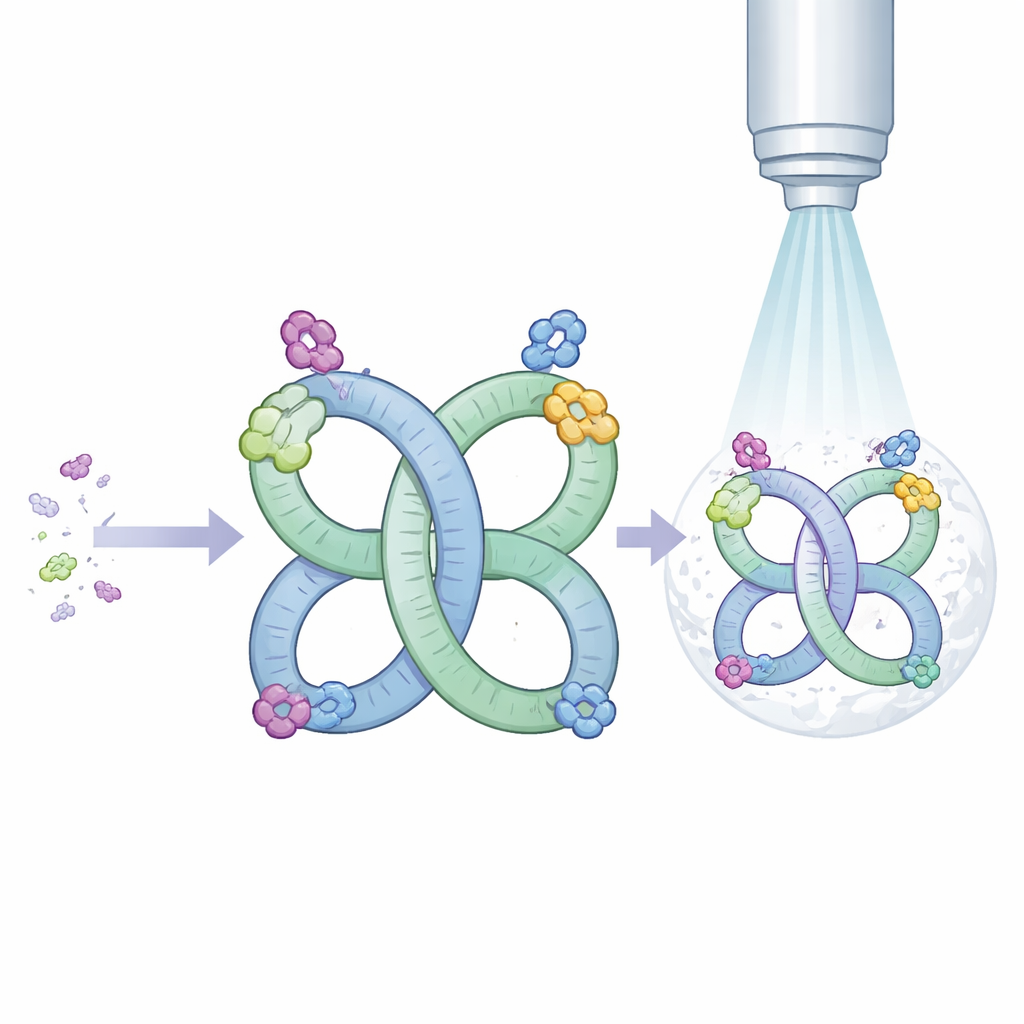
Avslöja hur designade RNA griper små molekyler
Teamet gick därefter bortom testsakerna till RNA vars fullständiga strukturer ännu inte setts. De fäste två små aptamerer — korta RNA utvalda i laboratoriet för att binda specifika små molekyler — på ställningen. En aptamer känner igen läkemedlet kinins; den andra känner av 8‑oxoguanin, en skadad form av en genetisk bas som signalerar oxidativ stress i bakterier. Tack vare ställningen levererade kryo‑elektronmikroskopin exceptionellt högkvalitativa kartor, tillräckligt fina för att följa varje RNA‑kedja från ände till ände och se var metalljoner och vattenmolekyler sitter. I kinins‑aptameren vaggar bindningsfickan läkemedlet främst genom tät stapling och formkomplementaritet, med förvånansvärt få direkta vätebindningar. I kontrast omsluter 8‑oxoguanin‑aptameren sitt ligand i ett intrikat nätverk av vätebindningar som berör nästan varje kemiskt distinkt site på den skadade basen, vilket förklarar dess skarpa diskriminering mellan 8‑oxoguanin och normal guanin.
Flexibel symmetri för klarare bilder
Intressant nog kan samma RNA‑ställning montera sig till antingen par eller fyrdelade strukturer beroende på förhållanden och den fästa gästen. När en fyrdelad arrangemang bildas förbättrar den upprepade geometrin bildkvaliteten ytterligare. I ett fall antog ställningen en fyrdelad form trots att dess sekvens var identisk med tvådelversionen, vilket belyser hur små skift i basparning kan omorganisera hela monteringen. Författarna utforskade också praktiska aspekter av kryo‑elektronmikroskopisk datainsamling, såsom hur tilting av provhållaren kan övervinna partiklars prefererade orienteringar på gallret, och hur påtvingad symmetri under bildbehandling måttligt men konsekvent skärper de resulterande strukturerna.
Ett nytt fönster mot små RNA‑maskiner
Sammanfattningsvis visar detta arbete att en kompakt, symmetrisk RNA‑ram kan förvandla annars osynliga små RNA till utmärkta kryo‑elektronmikroskopiska mål, vilket i gynnsamma fall möjliggör strukturer bortom atomdetalj. Genom att fästa ett okänt RNA vid ställningen via en enkel helixförbindelse kan forskare nu bestämma dess tredimensionella veckning, se exakt hur det griper en småmolekylspartner och upptäcka ordnade metalljoner och vattenmolekyler som finjusterar dess beteende. För en allmän publik är huvudbudskapet att vi nu har ett praktiskt verktyg för att noggrant studera några av naturens och bioteknikens minsta och mest mångsidiga RNA‑maskiner, vilket banar väg för rationell design av nya RNA‑baserade sensorer, läkemedel och molekylära enheter. 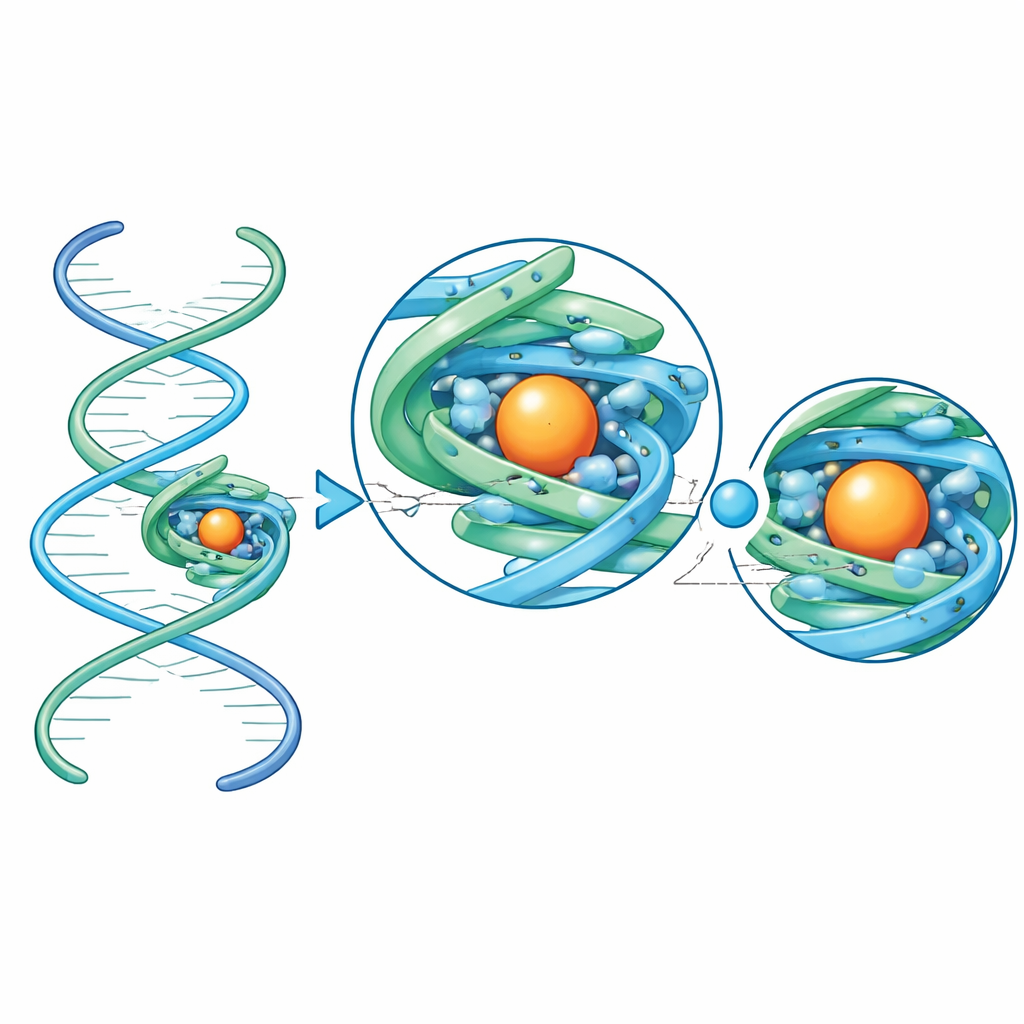
Citering: Jones, C.P., Ferré-D’Amaré, A.R. Scaffolds with optimized quaternary symmetry for de novo cryoEM structure determination of small RNAs. Nat Methods 23, 609–616 (2026). https://doi.org/10.1038/s41592-026-03016-x
Nyckelord: RNA-struktur, kryoelektronmikroskopi, aptamer, riboswitch, molekylära ställningar