Clear Sky Science · sv
Massutdelning av azitromycin och antibiotikaresistens i tarm och nasofarynx: en kluster-randomiserad studie
Varför det spelar roll att ge en tablett till många barn
I delar av Västra Afrika har ett enda antibiotikum, azitromycin, använts i masskampanjer för att minska antalet små barn som dör av infektioner. Strategin fungerar — men den väcker en allvarlig oro: odlar vi i tysthet fram hårdare, läkemedelsresistenta mikrober i barnens kroppar? Denna studie, genomförd i hundratals byar i Niger, granskar noggrant barnens tarmar och näsor för att se hur upprepade samhällsbehandlingar omformar deras dolda mikrobvärld och resistens mot antibiotika.
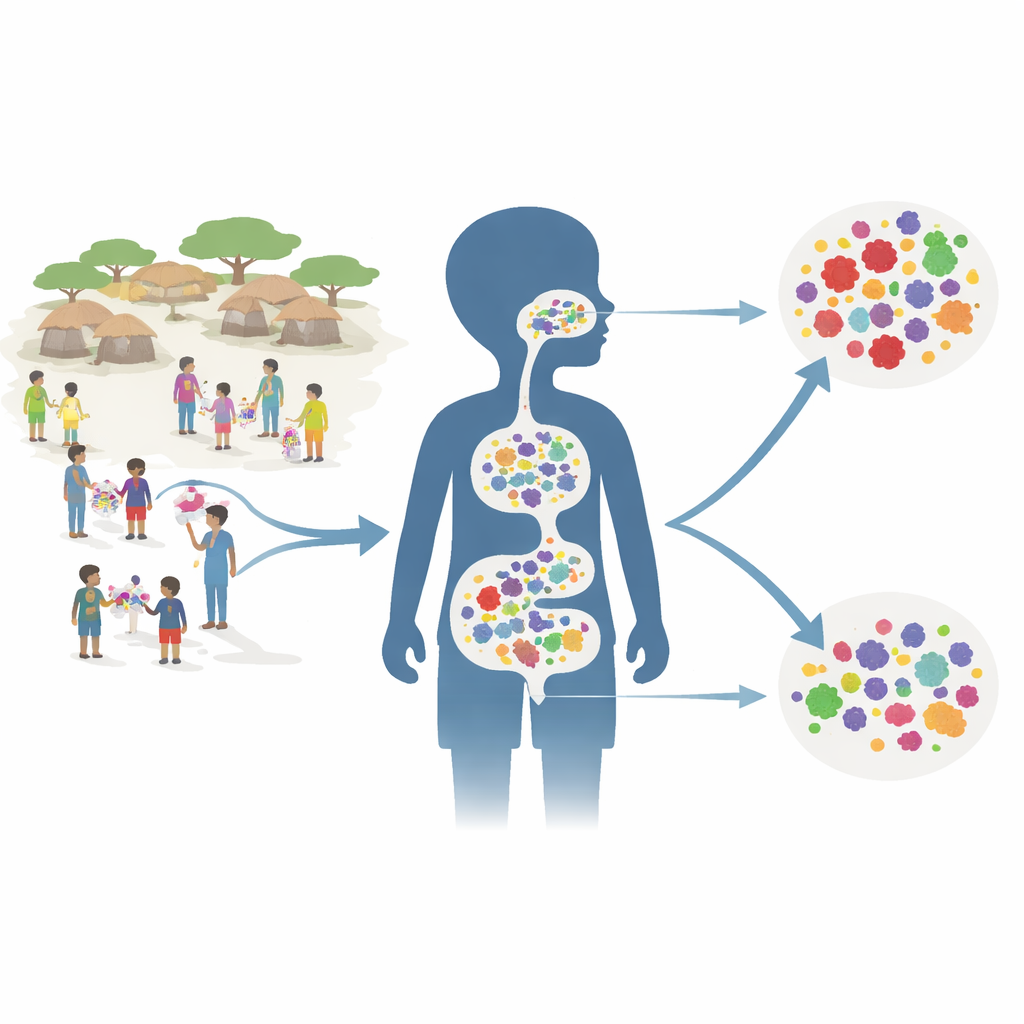
Att testa en samhällsomfattande medicinplan
Forskarna inramade sitt arbete i en stor prövning kallad AVENIR, som redan visat att ge azitromycin var sjätte månad till alla barn i åldern 1 till 59 månader kunde minska dödligheten i denna åldersgrupp. För resistensstudien fokuserade de på 150 slumpmässigt utvalda byar. Varje by tillhörde en av tre grupper: alla småbarn fick azitromycin; endast spädbarn upp till 11 månader fick azitromycin medan äldre småbarn och förskolebarn fick placebo; eller så fick alla barn placebo. Två år in i programmet — sex månader efter den fjärde behandlingsomgången — samlade teamet rektala och djupa nasala prov från ungefär 30 barn per by.
Att kika in i tarm och näsa
I stället för att odla bakterier i labbet poolade forskarna proverna från varje by och använde modern DNA-sekvensering. Det gjorde det möjligt för dem att katalogisera vilka bakterier som fanns och räkna genetiska markörer som signalerar resistens mot olika antibiotikafamiljer. De ägnade särskild uppmärksamhet åt makrolider — läkemedelsfamiljen som inkluderar azitromycin — samtidigt som de sökte efter resistens mot många andra vanliga antibiotikatyper, såsom penicillinlika läkemedel. Tarmarna och nasofarynx (den övre delen av halsen bakom näsan) undersöktes eftersom båda är stora reservoarer där resistensgener kan ackumuleras och potentiellt spridas.
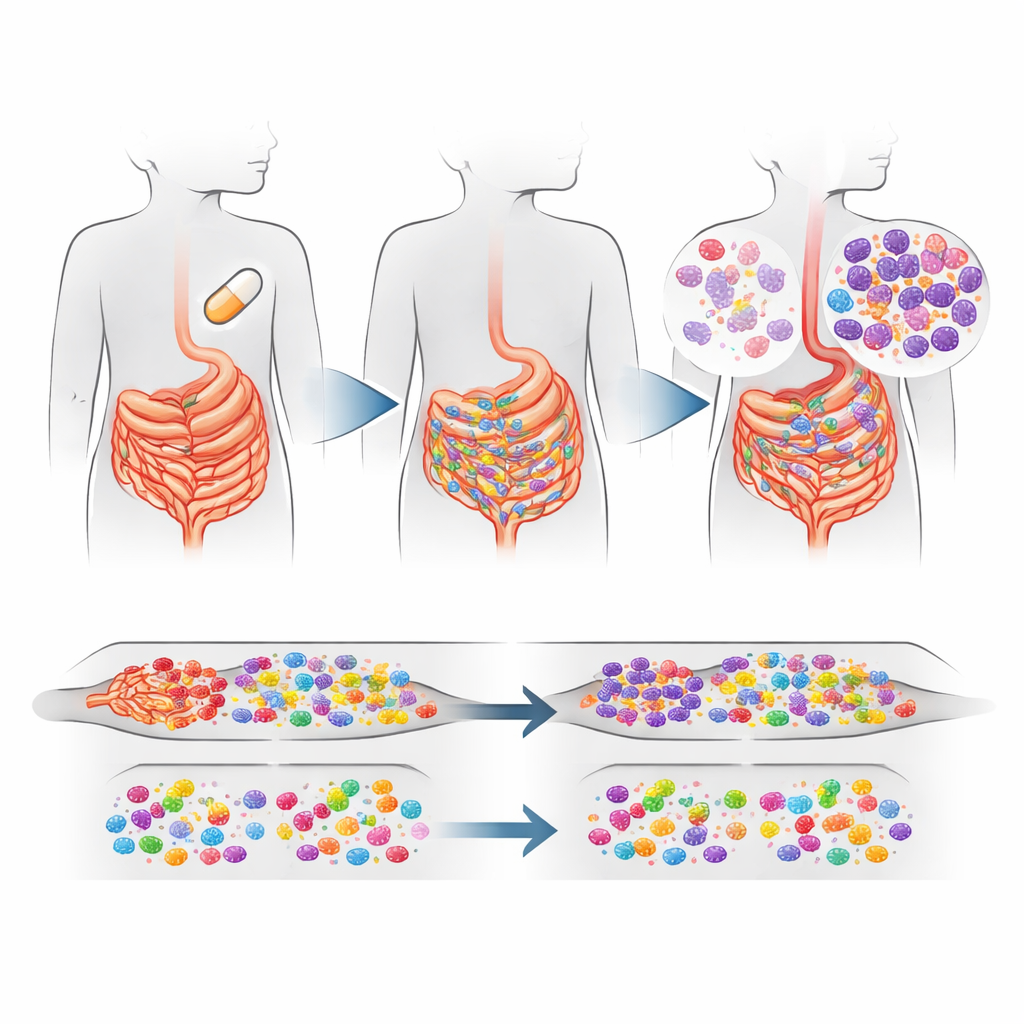
Vad som förändrades i barnens tarmar
Det tydligaste signalen kom från tarmen. Byar där alla barn fick azitromycin hade en måttlig men statistiskt säkerställd ökning — ungefär 16 % högre totalt — av makrolidresistensgener i tarmbakterier jämfört med placebobyar. Ökningen drevs i hög grad av en resistensgen kallad ermF, som hjälper bakterier att skydda sig mot makrolidläkemedel. Denna gen förekommer ofta hos vanliga tarmbakterier såsom Bacteroides och Prevotella, som vanligen lever ofarligt i tarmarna men ibland kan orsaka sjukdom. Intressant nog ökade inte resistensgener mot andra större antibiotikafamiljer, och den övergripande sammansättningen och diversiteten av tarmbakterier såg i stort sett likadan ut mellan behandlingsgrupperna, även om vissa specifika arter blev vanligare eller mindre vanliga.
Vad som förblev oförändrat i näsan
Nasala passager berättade i kontrast en tystare historia. Studien fann inga tydliga, statistiskt hållbara skillnader i makrolidresistensgener mellan behandlingsgrupperna i nasofarynx, och inget tecken på att resistens mot andra antibiotikaklasser selekterades där. De typiska näsborna — släkten som Moraxella, Haemophilus och Streptococcus — förblev dominerande. Några munrelaterade bakterier kopplade till tandköttssjukdom blev vanligare i azitromycinbehandlade samhällen, och några av dessa kan också bära resistensgener, men den totala resistensbördan i näsan förändrades inte på samma sätt som i tarmen.
Att balansera dagens vinster mot morgondagens risker
Tillsammans visar fynden att att ge azitromycin till alla småbarn i en community kan rädda liv, men att det också driver tarmbakterier mot större resistens mot denna läkemedelsfamilj, huvudsakligen genom expansion av specifika resistensgener som ermF. Studien såg ingen spridning till resistens mot andra antibiotikatyper under den tvååriga observationsperioden, och inga starka förändringar i det nasala reservoaren, men författarna varnar för att resistenta tarmbakterier och deras gener kan spridas över tid och mellan människor. De menar att alla breda antibiotikaprogram för att rädda barns liv bör inrymma noggrann, långsiktig övervakning av resistens så att hälsomyndigheter kan väga den omedelbara nyttan av färre barnadödsfall mot den långsammare, mindre synliga kostnaden av att stärka läkemedelsresistenta mikrober.
Citering: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Nyckelord: azitromycin, barnadödlighet, antibiotikaresistens, tarmmikrobiom, massbehandling