Clear Sky Science · sv
Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma
När cancern överlistar precisionsimmunterapi
Kraftfulla nya immunbaserade läkemedel förändrar behandlingen av multipelt myelom, en blodcancer som för de flesta patienter fortfarande är obotlig. Dessa terapier fungerar genom att omdirigera kroppens egna T‑celler för att söka upp och förstöra tumörceller märkta med särskilda ”flaggor” på ytan. En lovande flagga är molekylen GPRC5D. Men, som med många riktade behandlingar, kan tumörer utvecklas och smita förbi behandlingen. Denna studie redogör på ovanligt detaljerat sätt för hur myelomceller förändrar eller döljer GPRC5D‑flaggan för att undkomma mycket effektiva läkemedel som engagerar T‑celler.
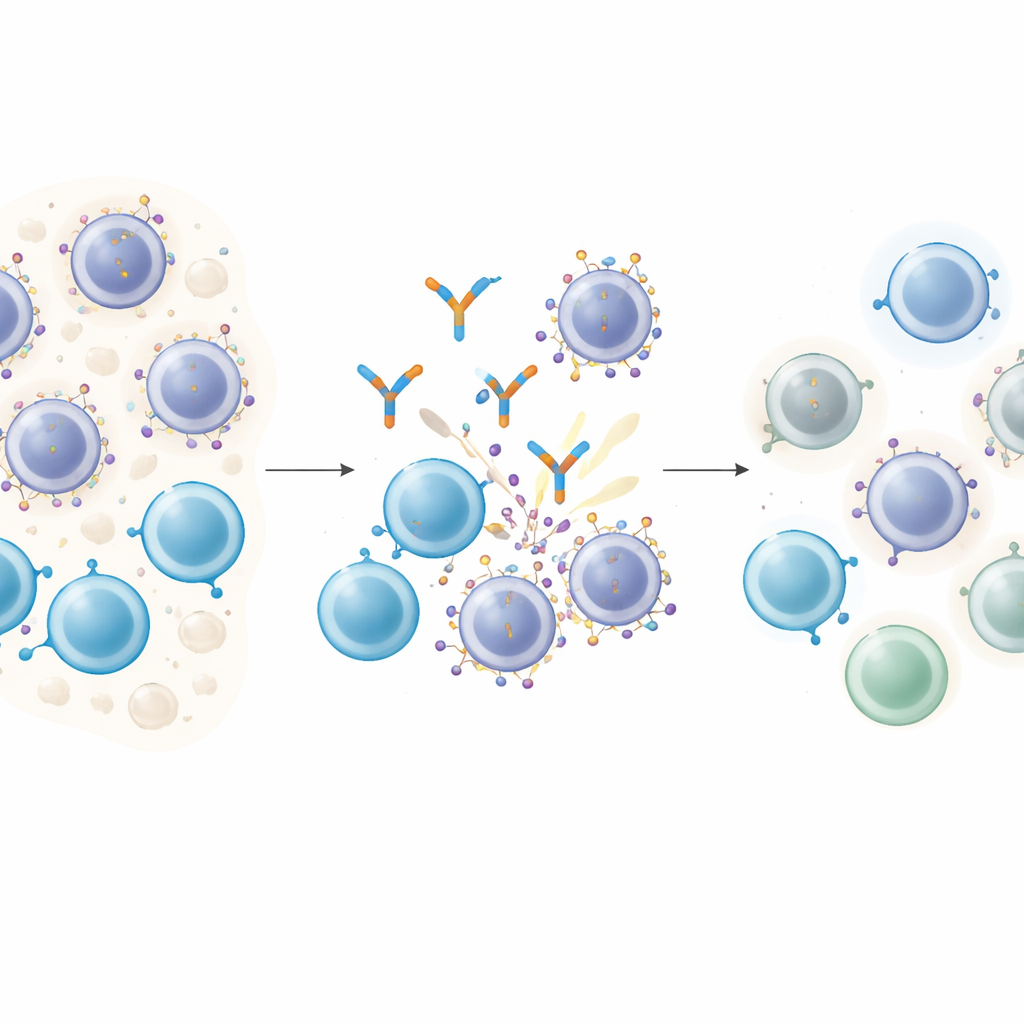
Hur smarta läkemedel låser sig fast vid cancerceller
T‑cellsengagerande antikroppar fungerar som molekylära matchmakare: ena änden greppar en T‑cell, den andra fäster vid en mål‑molekyl på cancercellen, och för dem i direkt kontakt så att T‑cellen kan döda sitt byte. Vid multipelt myelom är GPRC5D ett attraktivt mål eftersom det är rikt uttryckt på maligna plasmaceller men sparsamt på de flesta normala vävnader. Patienter som behandlats med ett GPRC5D‑riktat läkemedel kallat talquetamab får ofta djupa remissioner. Nästan alla får dock så småningom återfall, vilket väcker en avgörande fråga: förändrar cancercellerna själva det mål som dessa läkemedel är beroende av?
Spåra tumörevolution i realtid
Forskarna följde 21 personer med svårbehandlat myelom som fick talquetamab. De samlade benmärgsprover före behandlingen hos vissa patienter och igen när cancern kom tillbaka, och använde flera lager av DNA‑, RNA‑ och kromatinanalys för att undersöka tumörcellerna. Denna ultradetaljerade vy visade att hos ungefär två tredjedelar av de som återföll hade cancern förändrat GPRC5D på sätt som skulle dämpa eller blockera läkemedlets effekt. Slående nog samexisterade ofta flera olika resistenta subkloner — genetiskt distinkta grenar av tumören — i samma person, vilket visar att evolution mot undvikande kan följa flera vägar samtidigt.
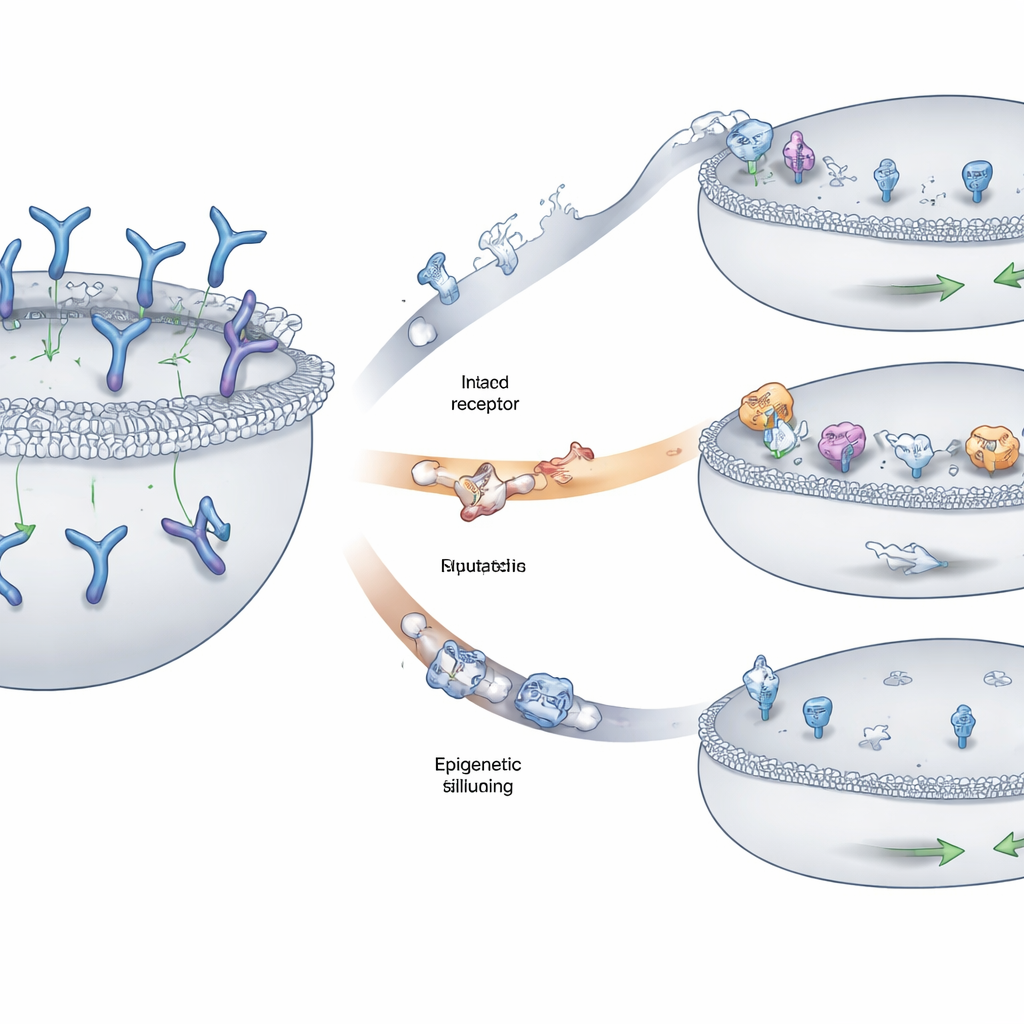
Tre huvudsakliga sätt tumörer döljer målet
Teamet fann tre återkommande mönster som myelomceller använde för att undvika igenkänning. Hos vissa patienter togs bitar av kromosomen som bär GPRC5D‑genen bort på båda kopiorna, vilket utplånade flaggan helt från cellens yta. Hos andra skapade mindre förändringar — enstaka basbyten eller små insättningar och deletioner — förvrängningar i viktiga regioner av GPRC5D‑proteinet. Många av dessa förändringar störde delar av proteinet som behövs för att det ska transporteras korrekt från cellens inre till yttre membranet, vilket gjorde att GPRC5D fastnade i ett internt fack istället för att visas där läkemedlet kunde se det. En tredje väg involverade epigenetisk tystnad: DNA‑regionen kring GPRC5D blev tätt packad och kemiskt märkt så att genen knappt lästes, trots att den underliggande sekvensen i stort var intakt. Tumörceller som använde denna strategi producerade mycket lite eller inget GPRC5D alls.
När flaggan finns men låset inte längre passar
Inte alla undanflykter tog bort GPRC5D från cellytan. I vissa fall såg proteinet normalt ut i standardtester men passade inte längre läkemedlet som en nyckel i ett lås. Teamet återskapade specifika patient‑härledda mutationer i laboratorieceller och testade hur väl olika GPRC5D‑riktade antikroppar kunde binda och döda dessa celler. En mutation ändrade subtilt den exakta plats där talquetamab greppar receptorn, vilket skarpt minskade läkemedlets förmåga att binda och utlösa celldöd, trots att receptorn fortfarande var synlig med rutinmässig färgning. Intressant nog förblev ett annat GPRC5D‑riktat läkemedel som binder receptorn på två platser effektivt mot flera av dessa mutanter, vilket belyser hur läkemedelsdesign — till exempel användning av multivalenta eller multi‑epitopbindande konstruktioner — kan påverka om resistenta kloner överlever.
Bortom målet: andra begränsningar för immunsvaret
Medan de flesta återfall visade någon form av GPRC5D‑förlust eller förändring, återföll ett fåtal patienter utan uppenbara förändringar i själva målet. I dessa fall verkade problemet ligga i T‑cellerna: de var mindre välfungerande och sämre på att döda cancerceller i laboratorietester, vilket tyder på att långvarig kontinuerlig exponering för engagerande terapi kan trötta ut immunsystemet. Studien avslöjade också att en särskild genetisk undergrupp av myelom (involverande en kromosomal omlokalisering kallad t(11;14)) naturligt håller GPRC5D‑genen i ett mer ”stängt” kromatinläge, med lägre grunduttryck. Detta väcker möjligheten att vissa patienter kan vara predisponerade för svaga svar eftersom deras tumörer från början har dämpade nivåer av målflaggan.
Vad detta betyder för patienter och framtida behandlingar
För patienter och kliniker förklarar detta arbete varför även mycket potenta GPRC5D‑riktade terapier ännu inte är botande: myelomceller kan ta bort, omarrangera, felrouta eller stänga av just den flagga som dessa läkemedel förlitar sig på, och de gör det ofta på flera sätt samtidigt. Resultaten antyder att övervakning av tumör‑DNA, snarare än enbart mätning av proteinnivåer, kommer att vara viktigt för att upptäcka framväxande undkomsmutationer som standardtester kan missa. De pekar också mot nästa generations strategier — såsom läkemedel som binder GPRC5D mer avidt på flera platser, kombinationer som träffar mer än ett mål samtidigt, eller medel som återöppnar tystade gener — för att ligga steget före tumörevolutionen. I huvudsak kartlägger denna studie de flyktrutter myelom använder så att framtida terapier kan utformas för att blockera dem och hålla T‑cellsbaserade behandlingar effektiva längre.
Citering: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Nyckelord: multipelt myelom, T‑cellsfångare, GPRC5D, antigenflykt, cancerimmunterapi