Clear Sky Science · sv
Linavonkibart och pembrolizumab vid immuncheckpoint‑blockad‑resistenta avancerade solida tumörer: en fas 1‑studie
Varför envisa cancerformer berör oss alla
Immunterapiläkemedel som ”släpper bromsen” på immunsystemet har förändrat behandlingen av många cancerformer, men de flesta patienter får antingen aldrig nytta eller ser så småningom att tumörerna börjar växa igen. Den här studien prövar ett nytt antikroppsbaserat läkemedel, linavonkibart, utformat för att slå ut en kraftfull sköld som tumörer använder för att gömma sig från immunsvar, och kombinerar det med en befintlig immunterapi, pembrolizumab. Resultaten ger en tidig inblick i att det kanske är möjligt att återställa immunkontroll även hos patienter vars cancer redan slutat svara på checkpoint‑läkemedel, samtidigt som biverkningarna hålls under kontroll.
En dold sköld runt tumörer
Många moderna immunterapier fungerar genom att blockera så kallade checkpoints, som PD‑1, som normalt dämpar T‑celler. När dessa bromsar släpps kan immunceller angripa cancern mer kraftfullt. Men tumörer anpassar sig ofta genom att bygga ett fientligt närområde runt sig som håller ute eller försvagar mördande T‑celler när de väl anländer. En central arkitekt bakom denna skyddande bubbla är ett signalprotein som kallas TGFβ1, som produceras både av cancerceller och omkringliggande stödjande celler. Tidigare försök att blockera hela TGFβ‑familjen visade löfte men stötte på allvarliga hjärt‑ och blödningsproblem, eftersom andra familjemedlemmar är viktiga för friska vävnader. Linavonkibart har konstruerats för att träffa rätt genom att selektivt neutralisera endast den latenta, inaktiva formen av TGFβ1 innan den aktiveras, samtidigt som nära besläktade molekyler som kroppen behöver lämnas i fred.
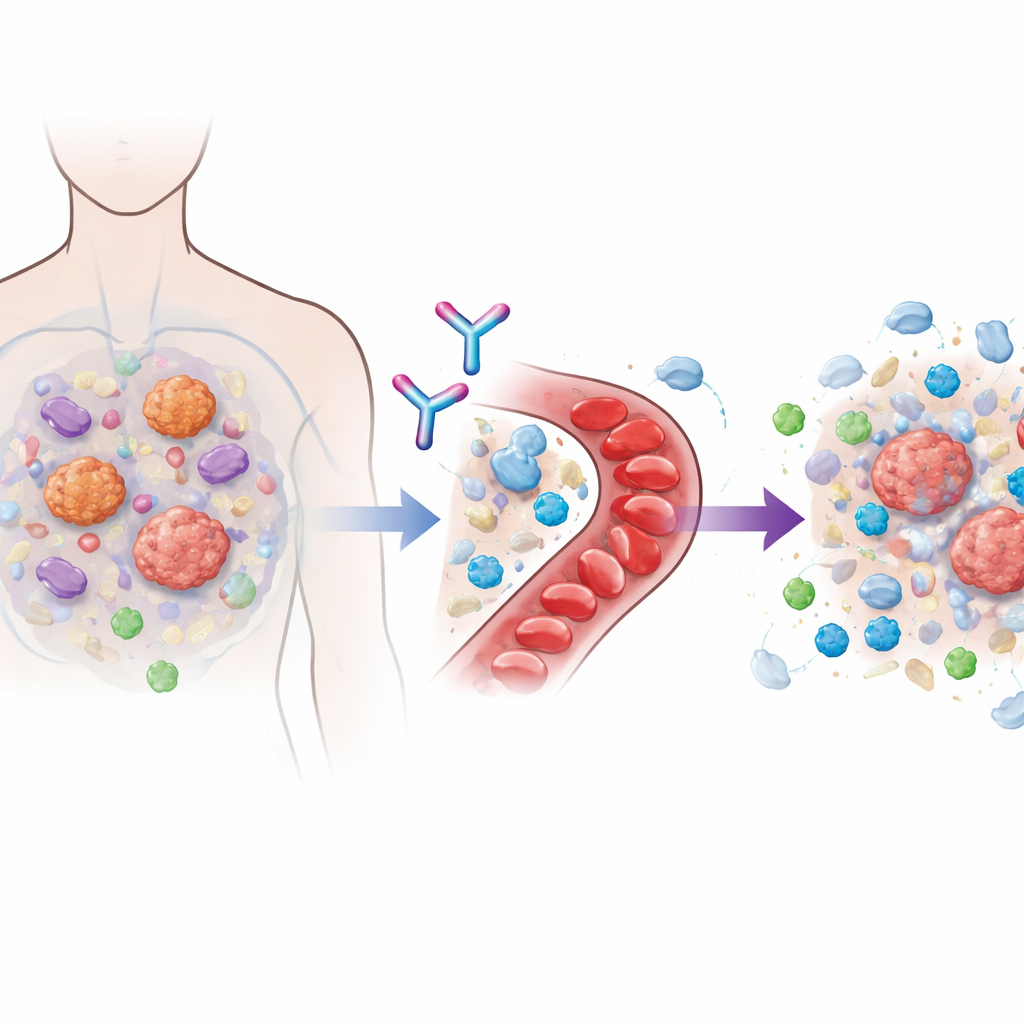
Utformning av ett omsorgsfullt först‑i‑människa‑test
DRAGON‑studien var en multicenter fas 1‑studie som genomfördes vid 22 sjukhus i USA och Sydkorea. Den inkluderade 112 vuxna med avancerade solida tumörer, som alla hade begränsade behandlingsalternativ. I första delen av studien gavs linavonkibart ensamt i stegvis ökande doser till små patientgrupper, eller i kombination med deras tidigare PD‑1‑baserade läkemedel. Denna stegvisa ansats användes för att kartlägga säkerhet, hur läkemedlet fördelades och kvarstod i blodomloppet, och för att välja en dos för bredare prövning. I andra delen fick 78 patienter vars tumörer redan varit resistenta mot minst en kur PD‑1‑immunterapi en fast dos linavonkibart tillsammans med pembrolizumab. Dessa patienter hade svårbehandlade cancerformer, inklusive klarcelligt njurcellscancer, melanom, huvud‑ och halscancer, urotelial (blåscancer) och lungcancer, och de flesta hade genomgått flera tidigare behandlingar.
Säkerheten först: vad hände med patienterna
Huvudmålet för denna tidiga fas var säkerhet, och linavonkibart visade lovande resultat på den fronten. Över alla dosnivåer nåddes ingen maximalt tolererad dos, och inga dosbegränsande eller dödliga biverkningar kopplade till läkemedlet noterades. När linavonkibart kombinerades med pembrolizumab vid fas 2‑dosen upplevde ungefär tre fjärdedelar av patienterna någon behandlingsrelaterad biverkning, liknande vad som ofta ses med immunterapi ensam. Utslag och klåda var de vanligaste ytterligare problemen, och ett litet antal patienter utvecklade mer allvarlig hud‑ eller lunginflammation. Viktigt är att den farliga immöna överreaktionen kallad cytokinfrisättningssyndrom, som kan förekomma vid vissa antikroppsbehandlingar, inte observerades, och den övergripande säkerhetsprofilen liknade till stor del den som ses med enbart pembrolizumab.
Tecken på att immunsystemet kan återväckas
Även om detta inte var en stor, avgörande effektstudie, pekade flera tecken på att avstängning av TGFβ1 kunde hjälpa till att återuppliva svar på PD‑1‑blockad. I expansionsfasen krympte den kombinerade behandlingen linavonkibart–pembrolizumab mätbara tumörer hos en anmärkningsvärd andel patienter som tidigare slutat ha nytta av PD‑1‑läkemedel. Bekräftade responsfrekvenser var 20 % vid klarcelligt njurcellscancer, 18,2 % vid melanom och strax över 9 % vid huvud‑ och hals‑ respektive uroteliala tumörer, med en njurcancerpatient som uppnådde fullständig försvinnande av synlig sjukdom. Många av dessa svar varade i flera månader, och patienter som svarade stannade i allmänhet längre på kombinationen än de gjort på sin tidigare PD‑1‑terapi. Biopsier tagna före och efter behandling gav en biologisk förklaring: tumörer visade större infiltration av CD8 ”mördande” T‑celler, högre nivåer av aktiverade T‑celler, färre immunhämmande regulatoriska T‑celler och myeloida celler, samt en övergripande förskjutning mot en mer inflammerad, attackbered mikromiljö.
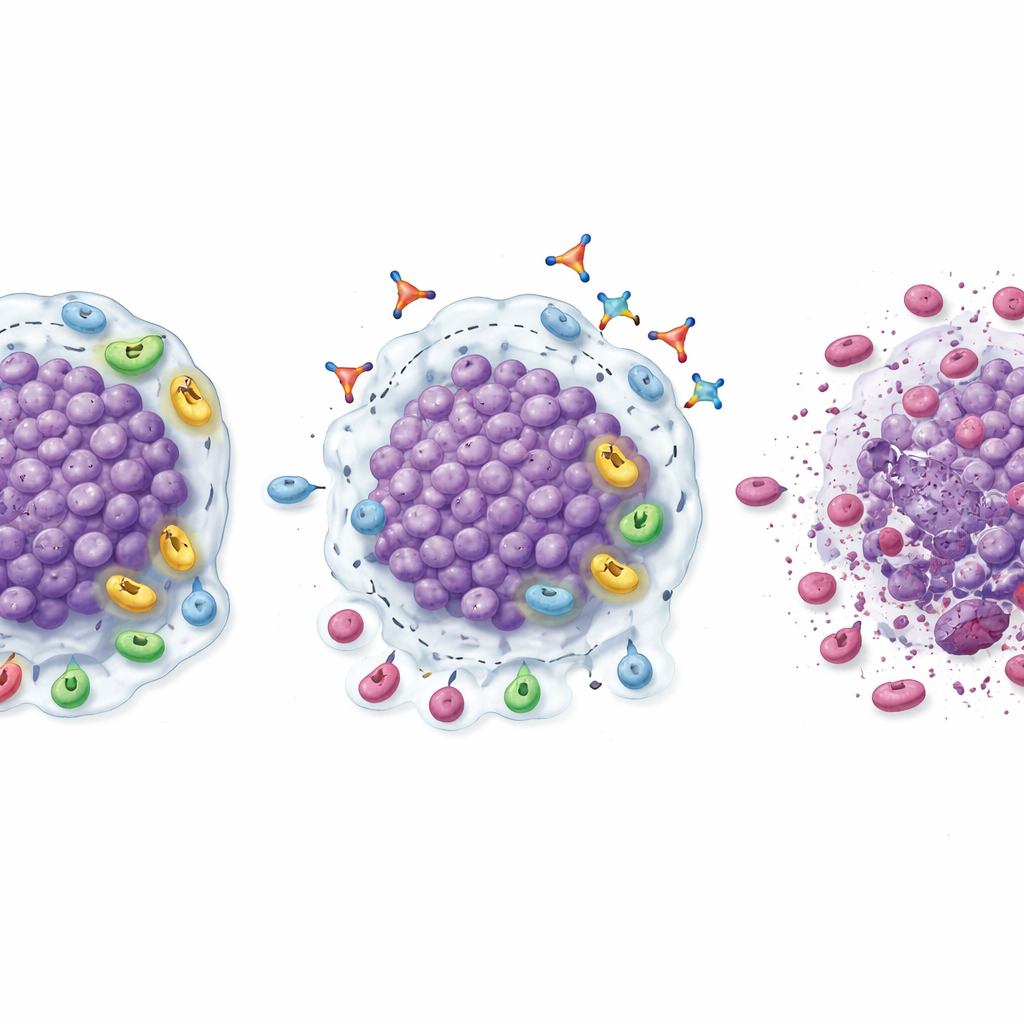
Att hitta vilka som kan ha mest nytta
Forskarna undersökte också vilka patienter som särskilt kunde tänkas svara. Vid klarcelligt njurcellscancer var tumörer som redan innehöll många CD8 T‑celler vid baslinjen — men som också var rika på regulatoriska T‑celler och uttryckte höga nivåer av TGFβ1 — mer benägna att krympa med kombinationsbehandlingen. Hos dessa patienter var responsfrekvenser och progressionsfri överlevnad avsevärt högre än i den bredare njurcancergruppen. Detta mönster tyder på en ”sötpunkt”: tumörer som har många närvarande immonsoldater men hålls tillbaka av TGFβ1‑driven suppression kan vara idealiska kandidater för linavonkibart plus PD‑1‑blockad. Om detta valideras i större studier skulle enkla vävnadstester för dessa markörer kunna hjälpa läkare välja de patienter som mest sannolikt får nytta.
Vad detta arbete betyder framöver
För personer med avancerad cancer som redan varit resistenta mot immunterapi är utsikten att återenergize sitt eget immunsystem utan att lägga till svår toxicitet tilltalande. Denna först‑i‑människa‑studie ger tidiga bevis för att selektivt inaktivera TGFβ1‑skölden med linavonkibart kan göras säkert och kan återställa meningsfull tumörkontroll när den kombineras med en PD‑1‑hämmare, särskilt vid vissa njurcancerformer. Även om studien var liten och icke‑randomiserad, bygger dess säkerhetsdata, biologiska utfall och bestående svar tillsammans ett starkt underlag för större fas 2‑studier. Om framtida prövningar bekräftar dessa fynd kan detta tillvägagångssätt utöka kretsen av patienter som kan dra nytta av immunterapi, och göra vissa i dag svårbehandlade tumörer återigen sårbara för kroppens egna försvar.
Citering: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Nyckelord: cancerimmunterapi, hämning av TGFβ1, resistens mot immuncheckpoint, klarcelligt njurcellscancer, tumörmikromiljö