Clear Sky Science · sv
Tydlig karta över inflammation i cirkulerande immunceller
Varför inflammation i blodet har betydelse för dig
Inflammation ligger i centrum för många sjukdomar, från ledgångsreumatism och astma till COVID-19 och cancer. Trots det har läkare fortfarande svårt att avläsa kroppens inflammationssignaler på ett sätt som tydligt förklarar vad som går fel och vilken behandling som fungerar bäst. Denna studie bygger en stor "karta" över immunceller som cirkulerar i blodet och visar hur dessa celler kan fungera som levande, lättprovtagna biomarkörer för att klassificera ett brett spektrum av inflammatoriska sjukdomar.
Att bygga en jättelik karta över immunceller
För att kartlägga detta landskap analyserade forskarna mer än 6,5 miljoner immunceller tagna från blodet hos 1 047 personer. Dessa försökspersoner representerade 19 tillstånd, inklusive autoimmuna sjukdomar som lupus och reumatoid artrit, kroniska lungsjukdomar som astma och KOL, infektioner som COVID-19 och HIV samt flera cancerformer, tillsammans med friska donatorer. Med single-cell RNA-sekvensering mätte de vilka gener som var aktiva i varje enskild cell, och använde sedan avancerade statistiska metoder för att korrigera tekniska skillnader mellan studier och för att gruppera cellerna i 64 distinkta immuncellstillstånd. Denna "Inflammationsatlas" fångar både välkända aktörer—såsom T‑celler, B‑celler och monocyter—och mer specialiserade undertyper som skiftar med sjukdom.
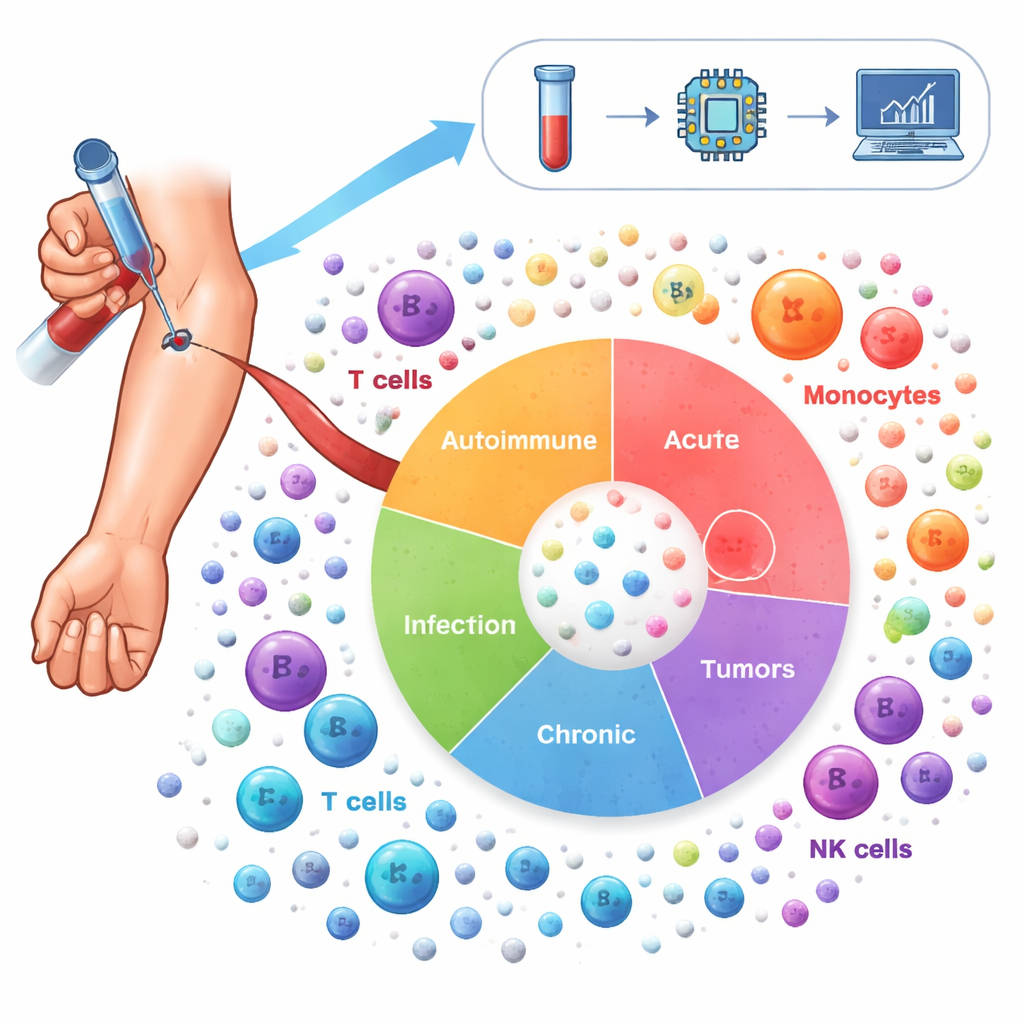
Att läsa kroppens inflammatoriska signaturer
Teamet fokuserade nästa steg på gener som kontrollerar hur immunceller aktiveras, rör sig genom kroppen, presenterar antigen och svarar på signalsubstanser som interferoner och tumörnekrosfaktor. De grupperade dessa gener i 21 biologiska "signaturer" och förfinade dem för varje huvudcelltyp. Genom att jämföra patienter med friska donatorer kunde de se vilka signaturer som var upp- eller nedreglerade i olika sjukdomar. Till exempel visade många immunmedierade inflammatoriska sjukdomar ökad aktivitet av adhesionmolekyler och antigenpresenterande maskineri, medan interferonsvar var dämpade i de flesta celltyper men förhöjda i vissa CD8‑T‑celler. Virala infektioner som influensa och COVID‑19 ökade interferoninducerade program, medan kroniska infektioner som HIV och hepatit B försvagade dem.
Inzoomning på viktiga gener och regulatoriska strömbrytare
Eftersom breda signaturer ändå döljer viktiga detaljer grävde forskarna djupare i individuella gener och deras regulatorer. I icke-naiva CD8‑T‑celler fann de att två gener, FGFBP2 och GZMB, var särskilt aktiva i specifika effektorminnesubtyper, särskilt vid ulcerös kolit. Dessa gener har kopplats till skada vid epiteliala ytor, och deras starka signal i blodet tyder på att dessa aggressiva celler redan är förberedda innan de går in i vävnader. En separat analys av genregleringsnätverk framhävde två transkriptionsfaktorer, STAT1 och SP1, som centrala kontrollörer av interferoninducerade program. Deras aktivitetsmönster skiljde sig mellan sjukdomar och celltyper—till exempel motsatt beteende i monocyter jämfört med CD8‑T‑celler vid lupus, och skift mellan skov och icke‑skov—vilket antyder hur samma vägar kan vara skyddande i ett sammanhang och skadliga i ett annat.
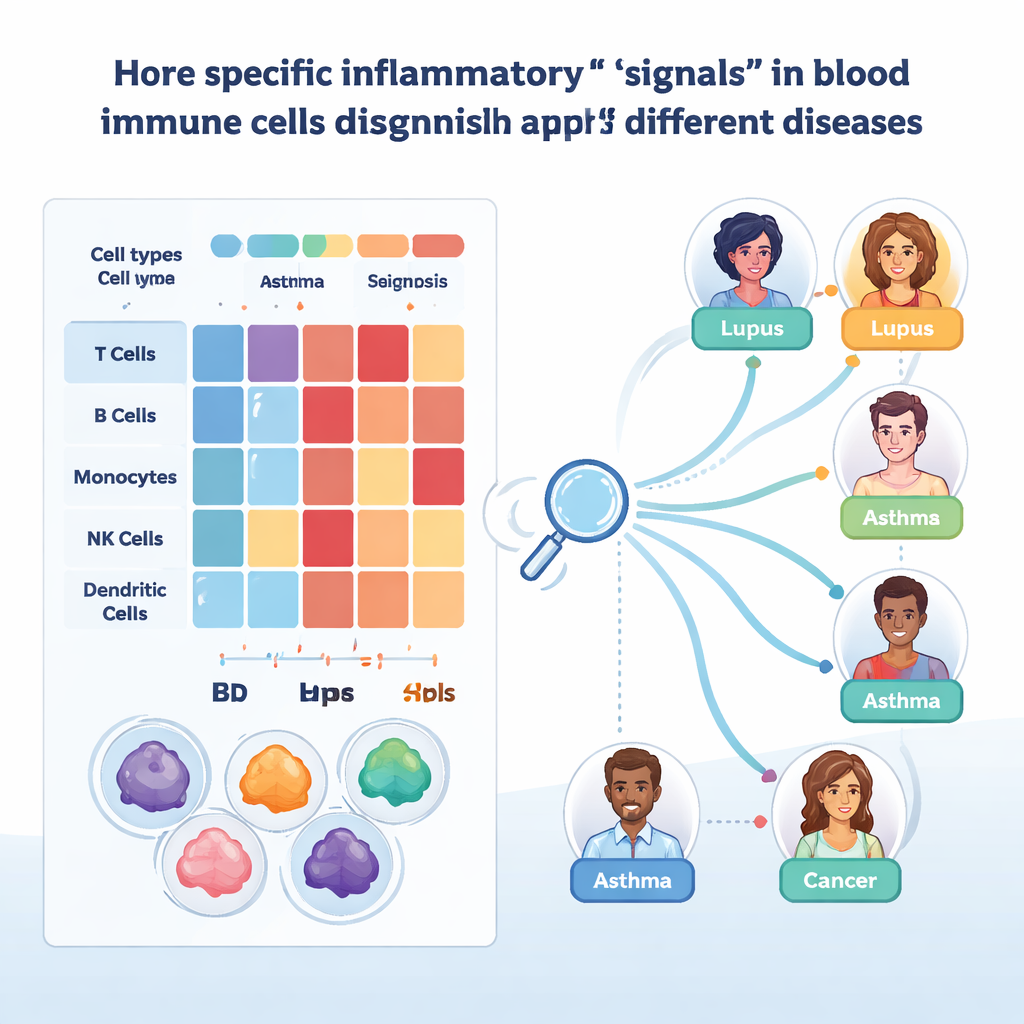
Att träna maskiner att upptäcka sjukdom från blodceller
För att göra atlasen praktisk tillämpade teamet tolkbar maskininlärning. De tränade gradientförstärkta beslutsträdmodeller separat för varje huvudcelltyp och bad algoritmerna att märka enskilda celler med rätt sjukdom baserat på deras genuttryck. Dessa modeller nådde hög noggrannhet när de testades på avhållna prover, särskilt efter korrigering för tekniska skillnader. Genom att använda SHAP, en metod som förklarar vilka gener som driver varje beslut, kunde forskarna identifiera kandidatbiomarkörer. Ett exempel är CYBA i monocyter, vars nivåer hjälpte till att skilja hudsjukdomar som psoriasis från tarminflammation vid Crohns sjukdom och ulcerös kolit. Ett annat är IFITM1 i vissa T‑celler och medfödda lymfoida celler, som skiljer astma från KOL och antyder olika mönster av kroniskt antiviralt försvar.
Mot en blodbaserad diagnostisk kompass
Slutligen undersökte författarna om hela patienter—inte bara enskilda celler—kunde klassificeras utifrån sina cirkulerande immunprofiler. De projicerade varje cells data in i ett komprimerat "embedding"‑utrymme, beräknade medelvärden av dessa embeddingar per celltyp för varje patient och tränade klassificerare för att förutsäga sjukdom. När nya patienter liknade dem i träningsdata var prestandan utmärkt. Men när prover kom från helt oberoende studier som använde andra laboratoriemetoder sjönk noggrannheten kraftigt, vilket visar hur känsliga sådana verktyg är för teknisk variation. En mer kontrollerad "centraliserad" datamängd, genererad vid ett center med en enda sekvenseringskemi, återställde mycket av prestandan och pekar på behovet av standardiserade protokoll eller mycket stora, mångsidiga träningsset.
Vad detta betyder för framtida diagnostik och behandling
För en lekmannapublik är huvudbudskapet att dina cirkulerande immunceller bär ett rikt fingeravtryck av hur din kropp är inflammerad. Genom att läsa dessa fingeravtryck cell för cell visar arbetet att det är möjligt att skilja mellan många sjukdomar, att upptäcka gener som kan driva specifika symtom och att börja bygga universella blodtester som klassificerar inflammatoriska sjukdomar. Studien är ännu inte ett färdigt kliniskt test—tekniska skillnader mellan studier begränsar fortfarande tillförlitligheten—men den lägger grunden för framtida "liquid biopsy"‑verktyg som kan hjälpa läkare att identifiera rätt diagnos och behandling tidigare, med ett enkelt blodprov.
Citering: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Nyckelord: inflammation, immunceller, single-cell RNA-sekvensering, biomarkörer, maskininlärning