Clear Sky Science · sv
Repotrectinib vid NTRK-fusionspositiva avancerade solida tumörer: en fas 1/2-studie
Nytt hopp från en riktad cancerpiller
Cancerbehandlingar utformas alltmer som precisa verktyg snarare än som trubbiga instrument. Denna studie granskar repotrectinib, en riktad tablett för personer vars tumörer bär på sällsynta genetiska förändringar kallade NTRK-fusioner. Även om dessa fusioner förekommer i färre än 1 av 100 solida tumörer kan de uppträda i många organ — från lunga till sköldkörtel till mjukdelar — och svarar ofta dramatiskt på specialdesignade läkemedel. Problemet har varit att tidigare läkemedel så småningom slutar fungera. Den här prövningen ställer en enkel fråga med stora konsekvenser: kan ett smartare, nästa generationens läkemedel hålla cancer under kontroll längre, även efter att andra riktade terapier har misslyckats?
En sällsynt men kraftfull cancerswitch
Vissa cancerformer drivs av fusioner i gener som kallas NTRK1, NTRK2 och NTRK3. Dessa fusioner fungerar som fastlåsta på-tillväxtbrytare i tumörceller. Förstagenerationsläkemedel som blockerar de resulterande TRK-proteinerna har redan hjälpt många patienter, men med tiden lär sig ofta cancern att undvika dem genom att skaffa nya mutationer i just den ficka där läkemedlen binder. Repotrectinib är konstruerat för att vara mindre och mer kompakt, så att det fortfarande kan passa in i denna ficka även efter sådana förändringar. Den internationella TRIDENT‑1-prövningen testade detta läkemedel hos vuxna med avancerade solida tumörer med NTRK-fusioner, inklusive personer som aldrig tidigare fått en TRK-blockerande behandling och de vars cancer redan hade vuxit förbi en eller två tidigare TRK-hämmare.
Vad prövningen gjorde
Studien rekryterade 144 patienter med NTRK-fusionspositiva solida tumörer vid centra runt om i världen; 120 av dem utgjorde huvudgruppen för effektmätning. Deras cancerformer täckte minst 18 olika typer, vanligast icke-småcellig lungcancer, sköldkörtelcancer, spottkörteltumörer och mjukdelssarkom. Alla hade lokalt avancerad eller metastaserad sjukdom, och många hade redan testat flera andra behandlingar, inklusive cytostatika, immunterapi eller tidigare TRK-hämmare. Patienterna tog repotrectinib per oralt varje dag enligt ett doseringsschema som togs fram i en tidigare fas av prövningen. Forskare följde hur många patienter som såg sina tumörer krympa, hur länge dessa svar varade, hur länge patienterna levde utan att sjukdomen förvärrades och hur väl de tålde läkemedlet.
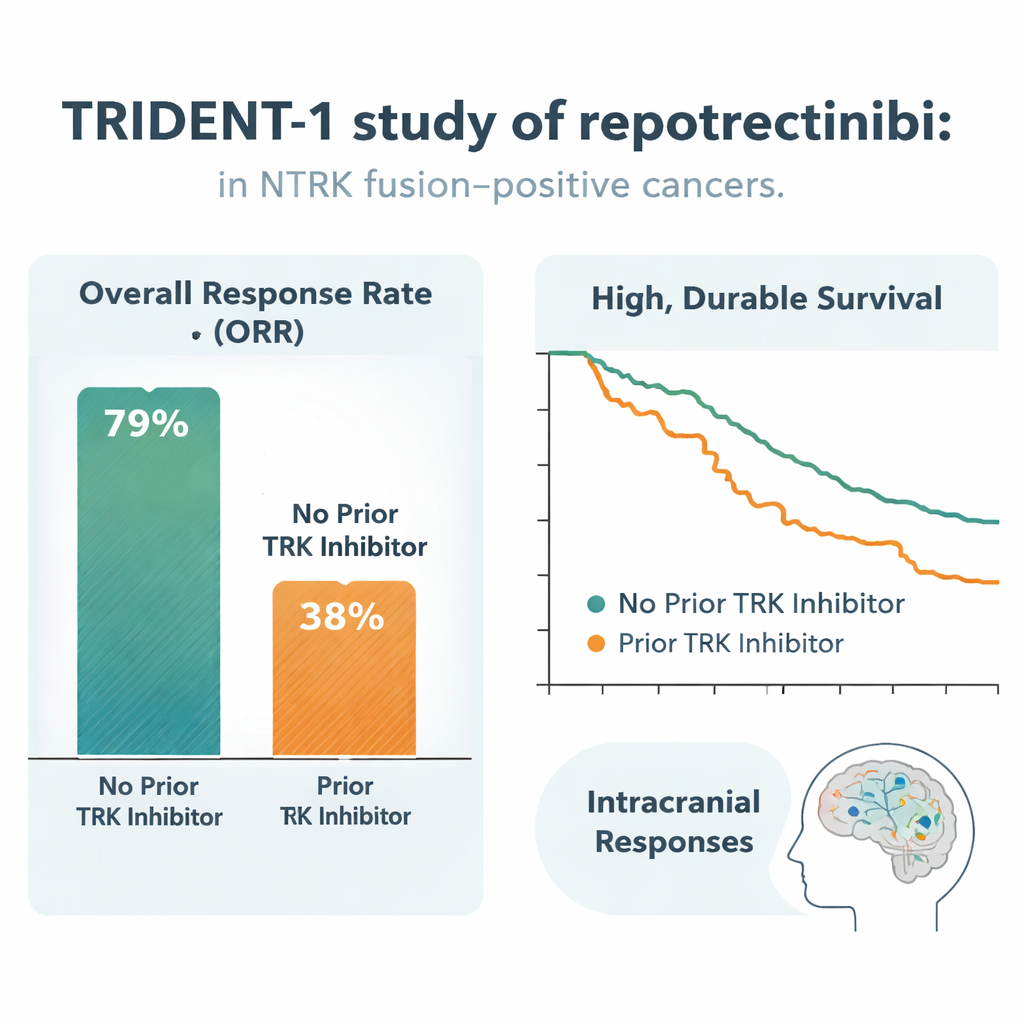
Starka och långvariga svar
Bland 51 patienter som aldrig tidigare fått en TRK-hämmare minskade tumörerna hos 59 % tillräckligt för att räknas som ett objektivt svar, och 16 % såg sina tumörer försvinna på skanningar. Svaren tenderade att dyka upp snabbt — inom ungefär två månader — och var anmärkningsvärt långvariga: efter två år uppskattades 85 % av dem som svarat fortfarande ha nytta, och cirka 60 % av hela gruppen hade ännu inte fått sin sjukdom försämrad. Även i den mer tungt behandlade gruppen av 69 patienter vars cancer redan gått förbi ett annat TRK-läkemedel svarade 48 % på repotrectinib, med ett typiskt svar som varade omkring 10 månader och ungefär en fjärdedel av patienterna fortfarande fria från progression efter ett år. Viktigt är att nytta sågs över många tumörtyper och oberoende av vilken NTRK-gen eller fusionpartner som var involverad.
Nå mot resistenta och hjärnsjukdom
En huvudutmaning för TRK-läkemedel är så kallade solvent front-mutationer, specifika förändringar i läkemedelsbindningsfickan som kan blockera tidigare läkemedel. I denna prövning bar nästan hälften av tidigare behandlade patienter sådana mutationer vid studiestart. Även i denna svårbehandlade undergrupp uppnådde 53 % meningsfull tumörminskning med repotrectinib, vilket bekräftar att läkemedlet kan övervinna åtminstone vissa former av resistens. Hjärnan, en vanlig gömställe för cancer, var ett annat fokus. Bland patienter med mätbara hjärnmetastaser vid baslinjen krympte hjärntumörerna hos två av tre i den obehandlade gruppen och fyra av sex i den tidigare behandlade gruppen, ofta under många månader. För patienter som började utan hjärninblandning förblev majoriteten fria från nya hjärnläsioner under uppföljningen.
Biverkningar och vad det betyder för patienter
Bland mer än 500 personer som behandlats med repotrectinib i denna och närliggande grupper var de vanligaste biverkningarna yrsel, förändrad smakupplevelse och stickningar, de flesta milda till måttliga. Mer allvarliga behandlingsrelaterade problem, såsom anemi eller förhöjda muskelenzymnivåer, var mindre frekventa, och endast omkring 4 % av patienterna avbröt läkemedlet på grund av biverkningar. Mått på den övergripande livskvaliteten förblev stabila eller förbättrades för de flesta deltagare över många behandlingscykler. Tillsammans visar resultaten att repotrectinib kan ge varaktig kontroll av NTRK-fusionspositiva cancerformer — inklusive sådana som redan visat motstånd mot tidigare TRK-läkemedel och sådana som spridit sig till hjärnan — samtidigt som det generellt är tolerabelt. För patienter med dessa sällsynta men aggressiva tumörer stödjer studien repotrectinib som ett viktigt nytt alternativ i det växande verktygslådan för precisionsmedicin mot cancer.
Citering: Besse, B., Lin, J.J., Bazhenova, L. et al. Repotrectinib in NTRK fusion–positive advanced solid tumors: a phase 1/2 trial. Nat Med 32, 682–689 (2026). https://doi.org/10.1038/s41591-025-04079-7
Nyckelord: riktad cancerterapi, NTRK-fusion, repotrectinib, motstånd mot TRK-hämmare, hjärnmetastaser