Clear Sky Science · sv
Flt3L‑medierad expansion av tumör cDC1 förbättrar immunterapi genom att primära stamliknande CD8+ T‑celler i lymfkörtlar
Hjälpa immunsystemet minnas hur man bekämpar cancer
Varför försvinner vissa människors tumörer med modern immunterapi medan andra får liten nytta? Denna studie undersöker immunförsvaret på djupet för att besvara den frågan. Forskarna visar att genom att förstärka en särskild grupp vaktsceller i tumörer kan man skapa ett förråd av långtlevande, "stamliknande" cytotoxiska T‑celler i närliggande lymfkörtlar. Dessa celler får i sin tur vanliga kontrollpunktspreparat, särskilt anti‑CTLA‑4‑terapi, att fungera starkare och under längre tid.
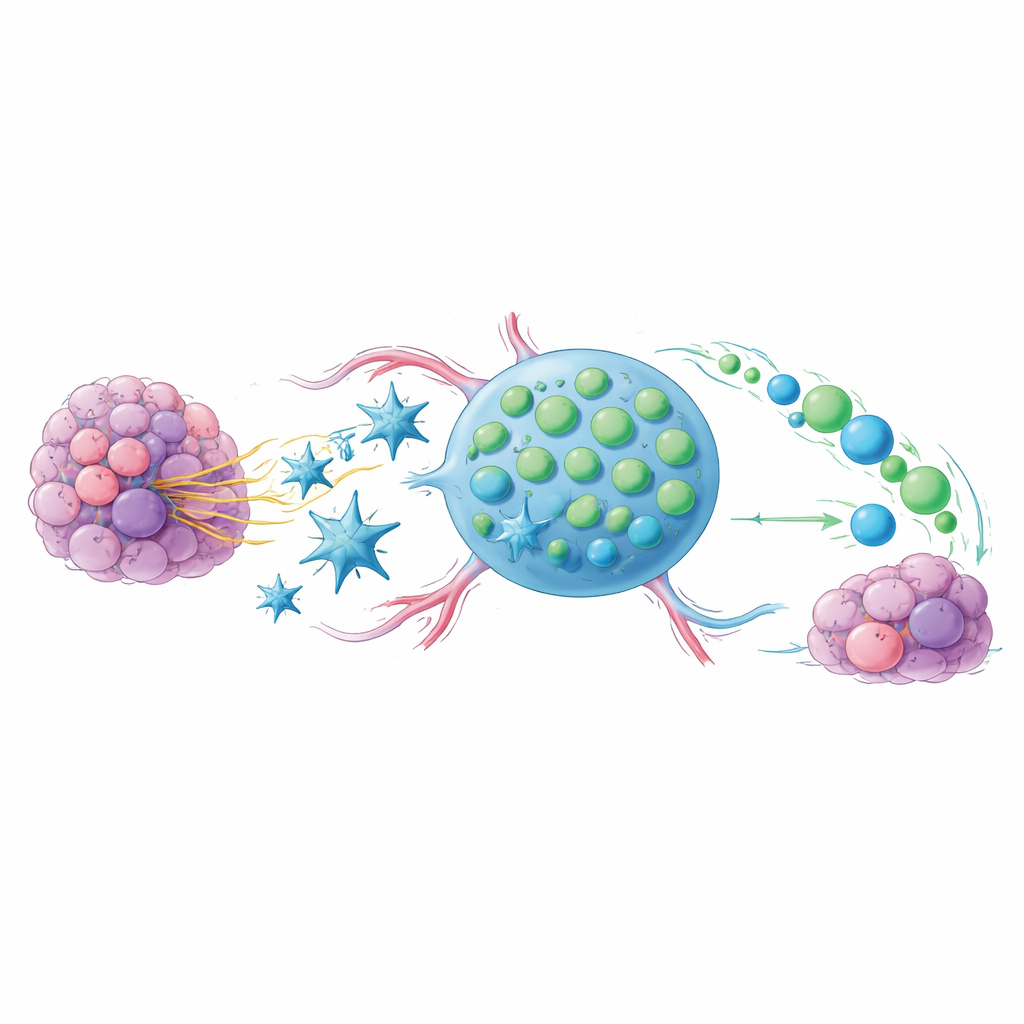
Problemet med uttröttade tumörbekämpande celler
Hämmare av kontrollpunkter såsom anti‑PD‑1 och anti‑CTLA‑4 frigör immunceller mot cancer, men de fungerar väl endast hos en del av patienterna. En ledtråd finns i tillståndet hos CD8‑T‑cellerna, huvudmördarna av infekterade eller cancerösa celler. När dessa T‑celler pressas för hårt under för lång tid glider de in i ett slitet, "uttröttat" tillstånd och slutar föröka sig effektivt. En mindre undergrupp behåller dock ett mer ungdomligt, stamliknande uttryck: de delar sig lätt, ger upphov till nya kämpar och är starkt kopplade till goda behandlingssvar hos patienter som får kontrollpunktsterapi. Den centrala frågan i detta arbete är hur man får tumörer och deras omgivning att gynna dessa stamliknande celler framför deras utbrända motsvarigheter.
Superladdning av tumörens vaktsceller
Teamet fokuserade på konventionella dendritiska celler av typ 1, en sällsynt men kraftfull klass av immunsensorer som är skickliga på att visa tumörfragment för T‑celler. De använde en tillväxtsignal kallad Flt3‑ligand (Flt3L) för att expandera dessa celler inne i mössens tumörer, antingen genom att konstruera cancerceller som utsöndrar den eller genom att ge den som läkemedel. Enkelcells‑RNA‑sekvensering visade att Flt3L‑rika tumörer innehöll många fler dendritiska celler och lymfocyter och färre tumörceller. Inom den dendritiska populationen expanderade tre distinkta grupper, inklusive en som var mycket mogen och primad för att resa till lymfkörtlar, där T‑celler först tränas. Samtidigt skiftade CD8‑T‑cellerna inne i dessa tumörer bort från ett terminalt uttröttat profil mot ett stam‑ eller minnesliknande tillstånd.
Bygga ett stamliknande T‑cellsförråd i lymfkörtlar
Genom att spåra tumörspecifika T‑celler och använda genetiska verktyg visade forskarna att Flt3L‑behandling ökar en population CD8‑T‑celler som bär ytmarkörer kopplade till stamliknande potential och aktiv delning. Dessa celler var beroende av XCR1‑positiva dendritiska celler och av CCR7‑styrd migration av dendritiska celler från tumören till dränerande lymfkörtel. När dendritiska celler utplånades, eller deras migration avaktiverades, krympte poolen av stamliknande T‑celler. Blockering av lymfocytutflöde från lymfkörtlar hade en liknande effekt och avbröt tillförseln av förnyade T‑celler till tumören. Molekylär profilering visade att denna process var beroende av transkriptionsfaktorn Myb och gynnade T‑celler med relativt svag igenkänning av tumörmål, en typ som i allt större utsträckning erkänns som viktig för hållbar cancerkontroll.
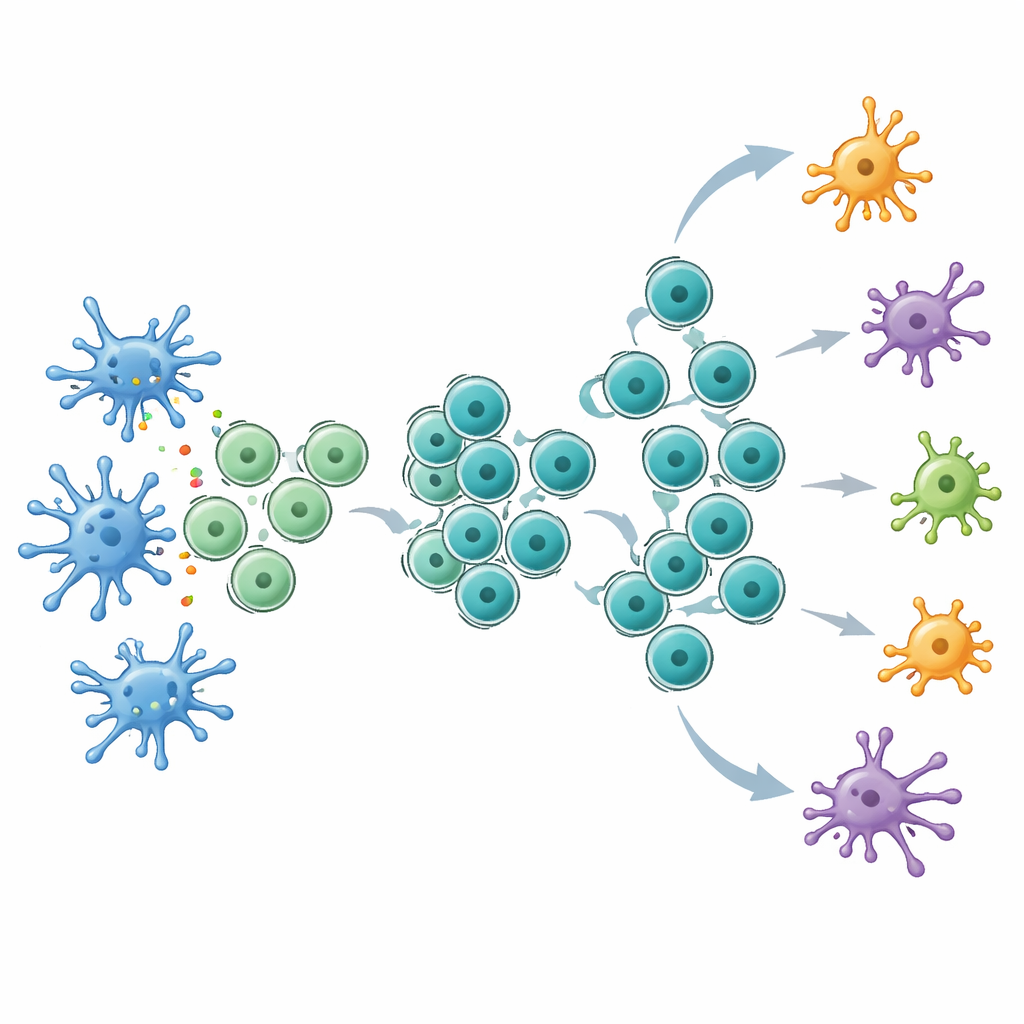
Få kontrollpunktsterapi att arbeta hårdare
Utrustade med detta utökade förråd av stamliknande T‑celler svarade mössen mycket bättre på kontrollpunktshämning, särskilt anti‑CTLA‑4‑behandling. Tumörer i Flt3L‑behandlade djur krympte mer, överlevnaden förbättrades och blodet samt lymfkörtlarna innehöll fler tumörspecifika T‑celler. Inne i tumörerna ökade Flt3L stamliknande CD8‑celler, medan efterföljande CTLA‑4‑blockad tycktes driva dessa celler att mogna till potent effektorceller som producerade höga nivåer av viktiga antitumörmolekyler. Sekvensering av T‑cellsreceptorer visade att kombinationsbehandlingen breddade antalet T‑cellskloner som expanderade, inklusive många subdominanta, vilket tyder på en mer diversifierad attack mot cancern. Detaljerad enkelcellsanalys avslöjade en unik CD8‑T‑cellsgrupp, markerad av uttryck av receptorn för immunsignalämnet IL‑21, som låg mitt emellan stamliknande och uttröttade tillstånd och delade T‑cellsreceptorer med både tidiga och sena populationer. Blockering av IL‑21‑signalering försvagade fördelarna med att kombinera Flt3L med anti‑CTLA‑4.
Vad detta betyder för framtida cancerbehandlingar
För en allmän läsare innebär budskapet att framgångsrik immunterapi inte bara handlar om att sparka immunsystemet hårdare, utan om att ha rätt slags celler att sparka. Detta arbete visar att genom att mata och styra dendritiska celler med Flt3L kan man fylla närliggande lymfkörtlar med ett förnybart förråd av stamliknande cytotoxiska T‑celler. När kontrollpunktspreparat såsom anti‑CTLA‑4 sedan appliceras kan de använda detta förråd för att generera vågor av nya kämpar som är fler, mer mångsidiga och bättre i stånd att kontrollera tumörer. Analyser av humana cancer‑datamängder tyder på att genuttryckssignaturer kopplade till denna väg också förutsäger bättre utfall hos patienter. Tillsammans pekar dessa fynd mot kombinationsbehandlingar som först bygger rätt immuncells‑"moderspann" med medel som Flt3L och sedan frigör den med kontrollpunktspreparat för starkare och mer bestående cancerkontroll.
Citering: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Nyckelord: cancerimmunterapi, dendritiska celler, stamliknande CD8 T‑celler, hämmare av kontrollpunkter, Flt3‑ligand