Clear Sky Science · sv
CD38 ger lokala antigen-specifika Treg-celler stressresiliens för kontroll av kompartmentaliserad inflammation i CNS
Varför hjärnbevakande immunceller är viktiga
Många autoimmuna sjukdomar i hjärnan, som multipel skleros, beter sig som glödande bränder: en initial inflammatorisk utbrott lugnar sig, men skadan kan blossa upp igen år senare. Denna studie ställer en förenklat enkel fråga med stora följder: efter en attack i centrala nervsystemet (CNS), vad upprätthåller freden — och vad förskjuter balansen tillbaka mot sjukdom? Författarna fokuserar på en liten population immunceller kallade regulatoriska T‑celler som bosätter sig i hjärnan och ryggmärgen efter en inflammation, och avslöjar hur en enda ytmolekyl ger dem förmåga att överleva i en fientlig miljö och förhindra återfall.
Immunfredsbevarare som stannar kvar
Med en musmodell som efterliknar aspekter av multipel skleros spårade forskarna olika typer av T‑celler när sjukdomen nådde sin topp och sedan gick in i en återhämtningsfas. Medan vanliga hjälpar‑T‑celler som driver inflammation minskade i antal när symptomen förbättrades, stannade de regulatoriska T‑cellerna — specialiserade celler som normalt dämpar immunsvar — kvar i CNS. Deras relativa andel inom den lokala T‑cellspopulationen ökade faktiskt, och de klustrade i särskilda nischer runt hjärnvätskans utrymmen och de skyddande hinnorna som täcker hjärnan. Genom att märka var inkommande T‑celler kom ifrån visade teamet att efter återhämtningen anlände mycket få nya regulatoriska T‑celler från lymfknutor. Istället underhölls CNS‑populationen i stort sett lokalt, vilket antyder en långsiktig resident "fredsbevarande" styrka. 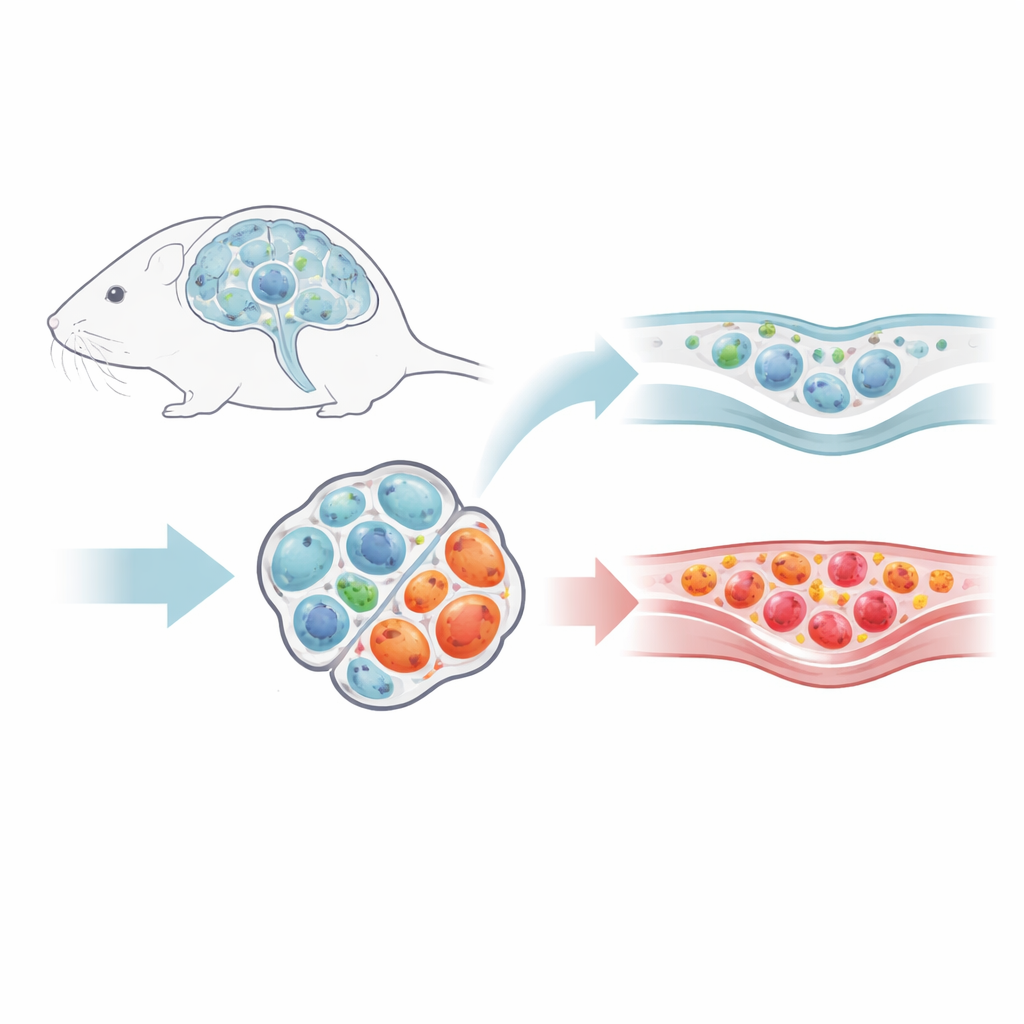
Stresståliga väktare i en fientlig nisch
Det postinflammatoriska CNS är allt annat än bekvämt för dessa väktare. Efter huvudvågen av sjukdom sjunker nivåerna av tillväxtsignalen interleukin‑2 (IL‑2) — som regulatoriska T‑celler starkt är beroende av — eftersom de flesta konventionella T‑celler har dragit sig tillbaka. Samtidigt är vävnaden rik på det metaboliska molekylet NAD+, vilket kan utlösa celldöd eller dämpa viktiga ytreceptorer när det modifieras av ett särskilt enzym. Genom att genetiskt tagga och följa individuella regulatoriska T‑celler skiljde författarna mellan "stabila" celler som behöll sin identitet och "instabila" som förlorade sitt kännetecken Foxp3‑program. Stabila celler visade ett mycket starkare signatur av IL‑2‑signalering och högre nivåer av IL‑2‑receptorer, vilket tyder på att förmågan att uppfatta knapp IL‑2 är central för att överleva i denna stressade miljö.
Lokal kontroll av återfall inifrån hjärnan
För att testa om dessa residenta regulatoriska T‑celler verkligen spelar roll för långsiktig sjukdomskontroll avlägsnade forskarna selektivt dem från CNS med ett toxin som levererades direkt i hjärnvätskan, samtidigt som de flesta systemiska regulatoriska T‑celler i resten av kroppen lämnades intakta. Inom dagar utvecklade möss som hållit på att återhämta sig svåra återfall med förnyad förlamning. Däremot utlöste inte uttömning av regulatoriska T‑celler endast i kroppen, medan de i CNS sparades, några utbrott. Återfallet involverade snabb reaktivering och expansion av effektor‑T‑celler som redan var förankrade i CNS, även när deras rekrytering från blodet blockerades. Detta visar att lokala regulatoriska T‑celler, snarare än cirkulerande sådana, är avgörande för att hålla kvarstående aggressiva celler i schack som dröjer kvar efter den akuta attacken.
Hur ett enzym skyddar regulatoriska celler
När forskarna gick vidare sökte de efter molekyler som skiljer stresståliga CNS‑regulatoriska T‑celler åt. En nyckelaktör framträdde: CD38, ett enzym på cellens yta som bryter ner extracellulärt NAD+. I det inflammerade CNS ökade regulatoriska T‑celler kraftigt uttrycket av CD38, medan konventionella T‑celler inte visade en lika markant förändring. När teamet överförde myelinspecifika regulatoriska T‑celler utan CD38 till möss nådde dessa celler visserligen CNS men misslyckades med att kontrollera sjukdomen, till skillnad från deras normala motsvarigheter. I blandade kimära djur, där endast de residenta regulatoriska T‑cellerna saknade CD38, var det tillräckligt att ta bort den CD38‑tillräckliga fraktionen för att framkalla återfall, vilket visar att CD38 verkar på ett cellintroniskt sätt för att möjliggöra effektiv kontroll.
Skydda livsnödvändiga signalen
Mekanistiska experiment visade hur CD38 förser denna resiliens. Höga NAD+‑nivåer i CNS kan driva kemisk modifiering av ytliga proteiner via enzymet ARTC2.2. Ett känsligt mål är IL‑2‑receptorns högaffinitetssubenhet, som regulatoriska T‑celler uttrycker i mycket höga nivåer, särskilt när de känner igen hjärnantigen. I CD38‑bristande regulatoriska T‑celler exponerade för NAD+ blev majoriteten av IL‑2‑receptorerna modifierade, vilket ledde till svagare aktivering av den nedströms budbäraren STAT5 och minskad respons på IL‑2. I kontrast minskade CD38‑uttryckande celler lokalt NAD+ runt sig, vilket begränsade denna skadliga modifiering och bevarade stark IL‑2‑signalering. I levande möss dödade injektion av NAD+ i hjärnan selektivt de flesta regulatoriska T‑celler via denna väg, medan konventionella T‑celler skonades, vilket understryker hur prekär nischen är utan detta skyddande enzym. 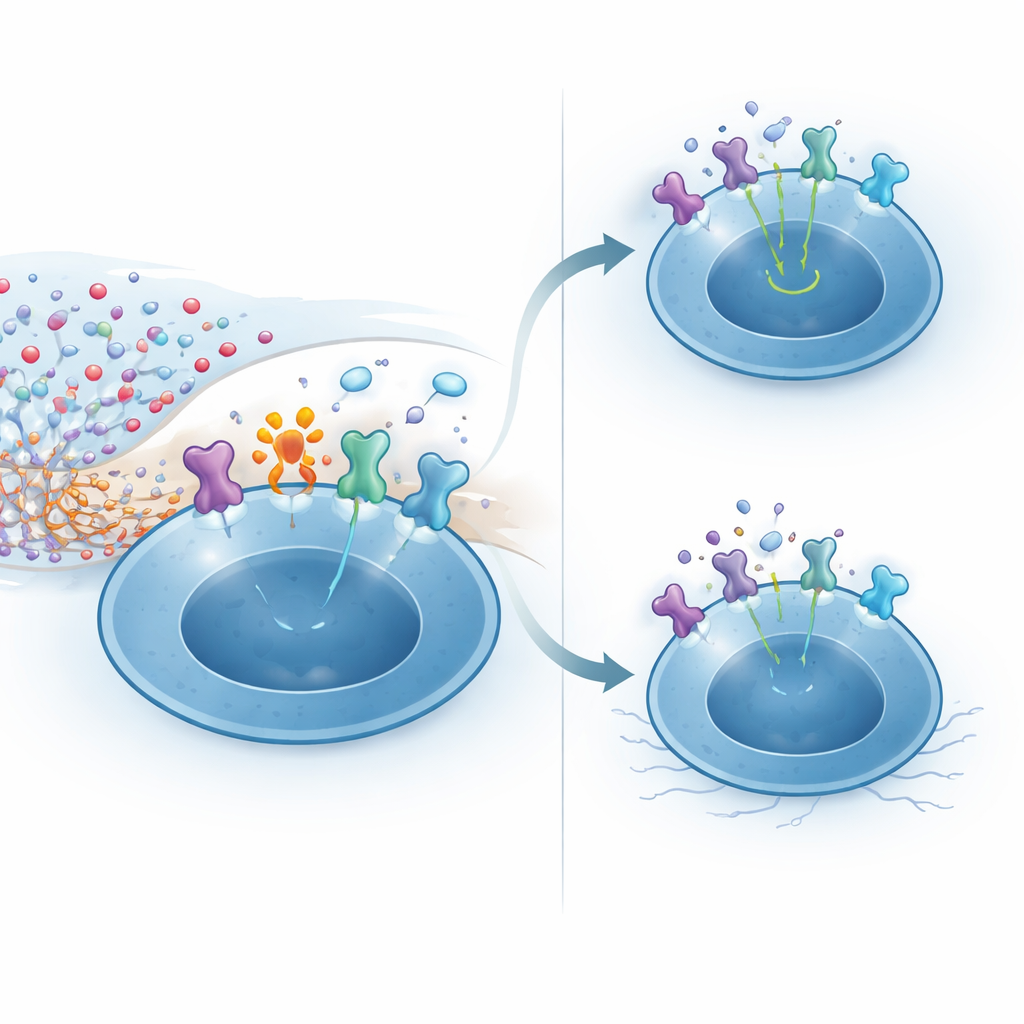
Vad detta betyder för kronisk autoimmunitet i hjärnan
Detta arbete målar upp en bild av kronisk CNS‑autoimmunitet som en kompartmentaliserad strid: små kluster av kvarstående aggressiva T‑celler finns i hjärnan och ryggmärgen, hållna i schack av lika specialiserade lokala regulatoriska T‑celler. Dessa väktare är "stresståliga" eftersom CD38 gör att de klarar höga NAD+‑nivåer och fortsätter att uppfatta minimala mängder IL‑2, vilket bevarar deras identitet och suppressiva funktion. För icke‑experter är huvudpoängen att långsiktig kontroll av sjukdomar som multipel skleros kan bero mindre på det cirkulerande immunsystemet och mer på att vårda och skydda dessa residenta fredsbevarare inom hjärnan — potentiellt genom att rikta in sig på vägar som stärker CD38‑funktionen eller IL‑2‑känsligheten i regulatoriska T‑celler.
Citering: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Nyckelord: regulatoriska T‑celler, multipel skleros, inflammation i centrala nervsystemet, CD38-enzym, immuntolerans