Clear Sky Science · sv
Cellcykelstopp förbättrar CD8+ T-cellers effektorfunktion genom att förstärka glukosmetabolism och IL-2-signalering
Att sätta cancermotverkande celler på paus
De flesta cancerläkemedel som stoppar celldelning är utvecklade med tumörer i åtanke, men de påverkar också immunsystemets främsta soldater—CD8 T-celler. Denna studie ställer en oväntad fråga: vad händer om man kortvarigt pausar dessa mördarceller—kan det faktiskt göra dem bättre på att jaga tumörer? Svaret, grundat på mössmodeller, mänskliga celler och patientprover, är att en väl tajmad ”stopp”-signal kan superladda dessa celler för en starkare och mer långvarig antitumörrespons.
Ett kort uppehåll före anfallet
När CD8 T-celler först känner igen cancer- eller virussignaler brukar de skynda igenom delningscykler samtidigt som de mognar till effektorceller. Forskarna använde vanliga cellcykelhämmande läkemedel, såsom hydroxyurea och CDK4/6-hämmare, för att tillfälligt skilja dessa två processer åt: cellerna fick aktiveras och börja differentieras, men deras delning pausades kortvarigt. Överraskande nog blev inte dessa arresterade T-celler utmattade eller dysfunktionella. Istället, efter att läkemedlet avlägsnats, delade de sig snabbare och nådde högre cellantal än T-celler som aldrig pausades, både i rör-experiment och i vaccinerade möss. Effektoregenskaper—som produktion av toxiska molekyler som dödar cancerceller—bevarades eller förstärktes till och med efter frisättning.
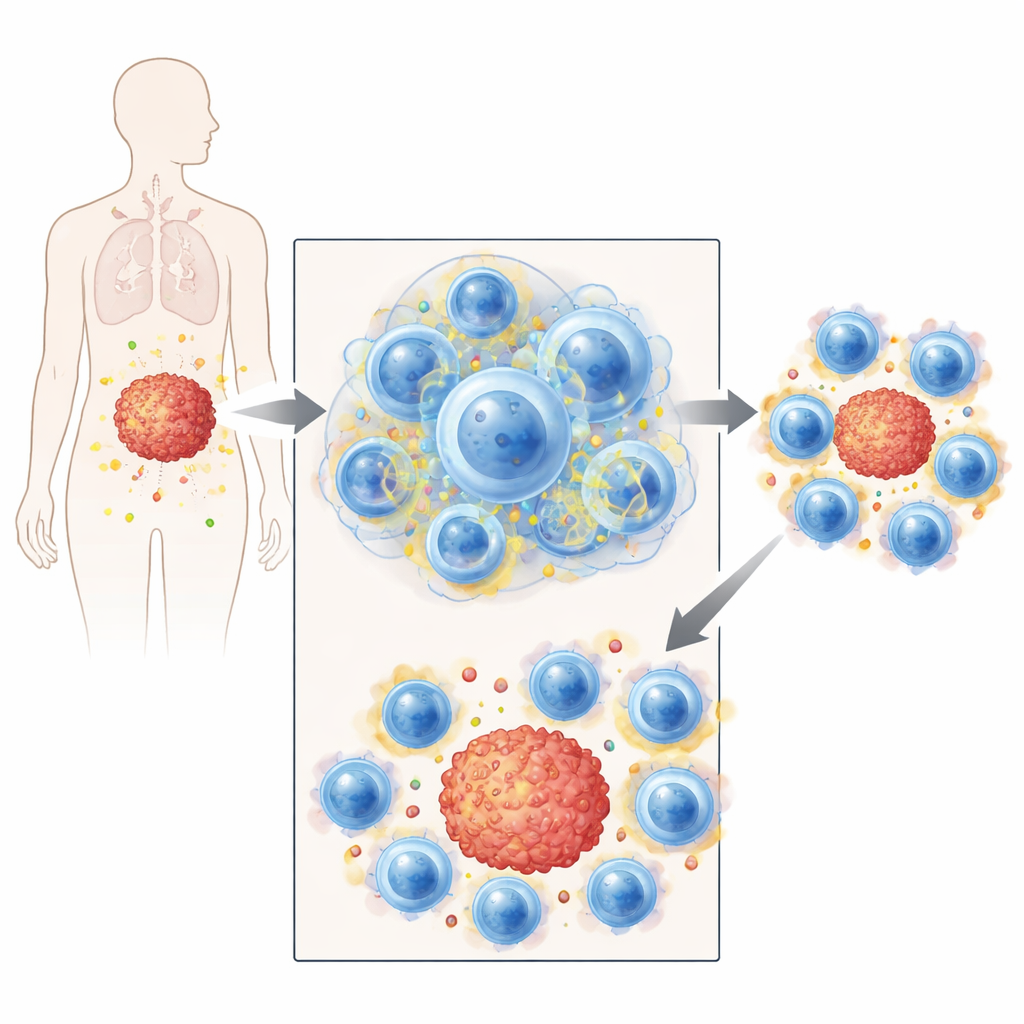
Lagring av bränsle i vilande krigare
För att förstå hur en icke-delande T-cell senare kunde växa om sin kontinuerligt cyklande motsvarighet undersökte teamet dess interna kemi. Under arresteringsperioden betedde sig dessa T-celler som idrottare som kolhydratladdar inför ett lopp. De ökade antalet transportörer som tar upp glukos och aminosyror, ackumulerade sockerarter och byggde upp glykogenlager—reserver av kolhydrat. De ökade även nivåerna av enzymer som driver glykolys, den snabba nedbrytningen av socker för energi, och intensifierade mitokondriell och kolesterolmetabolism som är viktig för att skapa nya membran. I praktiken, medan cellerna inte förbrukade energi på delning, fyllde de tyst sina tankar och uppgraderade sina kraftverk. När blockaden lyftes förbrände de snabbt dessa reserver för att driva intensiv proliferation.
En självskapad tillväxtsignal
Bränslet ensam förklarade inte uppsvinget. De pausade T-cellerna ökade också produktionen av interleukin-2 (IL-2), en potent immun tillväxtfaktor som T-celler både kan utsöndra och själva känna av. Under arresteringsperioden producerade många celler stora mängder IL-2 och visade fler av dess receptorer, vilket gjorde dem mycket responsiva för sin egen signal. Nedströmsvägar som involverar proteinet STAT5 aktiverades starkt när cellerna åter släpptes, vilket stödde kraftig delning även när en huvudregulator av tillväxt, mTORC1-vägen, var delvis blockad. Genetiska och läkemedelsbaserade experiment visade att borttagande av IL-2 kraftigt försämrade denna förstärkta proliferation, medan återtillförsel av IL-2 återställde den. Pausen präglade därför ett minnesliknande tillstånd: metabolt primade celler som är redo att explosivt svara på sina egna tillväxtsignaler.
Bättre tumörkontroll och kombinationsbehandlingar
Det verkliga testet var om denna strategi förbättrar cancerkontroll. I flera mössmodeller för tumörer ökade en kortvarig behandling med cellcykelhämmande läkemedel antalet och aktiviteten hos metabolt primade CD8 T-celler i blodet, lymfknutor och inom tumörer. Dessa celler uppvisade högre upptag av glukos och förhöjda markörer för kolesterol- och energimetabolism. Tumörspecifika T-celler expanderade starkare efter att läkemedlet avlägsnats och uttryckte markörer kopplade till effektiv tumördöd. Ett kort uppehåll samverkade med flera immunoterapeutiska angreppssätt: adoptivt överförda T-celler förbehandlade med hydroxyurea utrotade tumörer mer effektivt; att kombinera transient stopp med PD-L1-checkpointblockad fördröjde tumörtillväxt och förlängde överlevnad; och att para en terapeutisk cancervaccinering med arrest förbättrade resultaten avsevärt. Tidiga kliniska biopsidata från kvinnor som fått ribociclib plus hormonbehandling för bröstcancer antydde en liknande metabolisk förstärkning i tumörinfiltrerande CD8 T-celler.
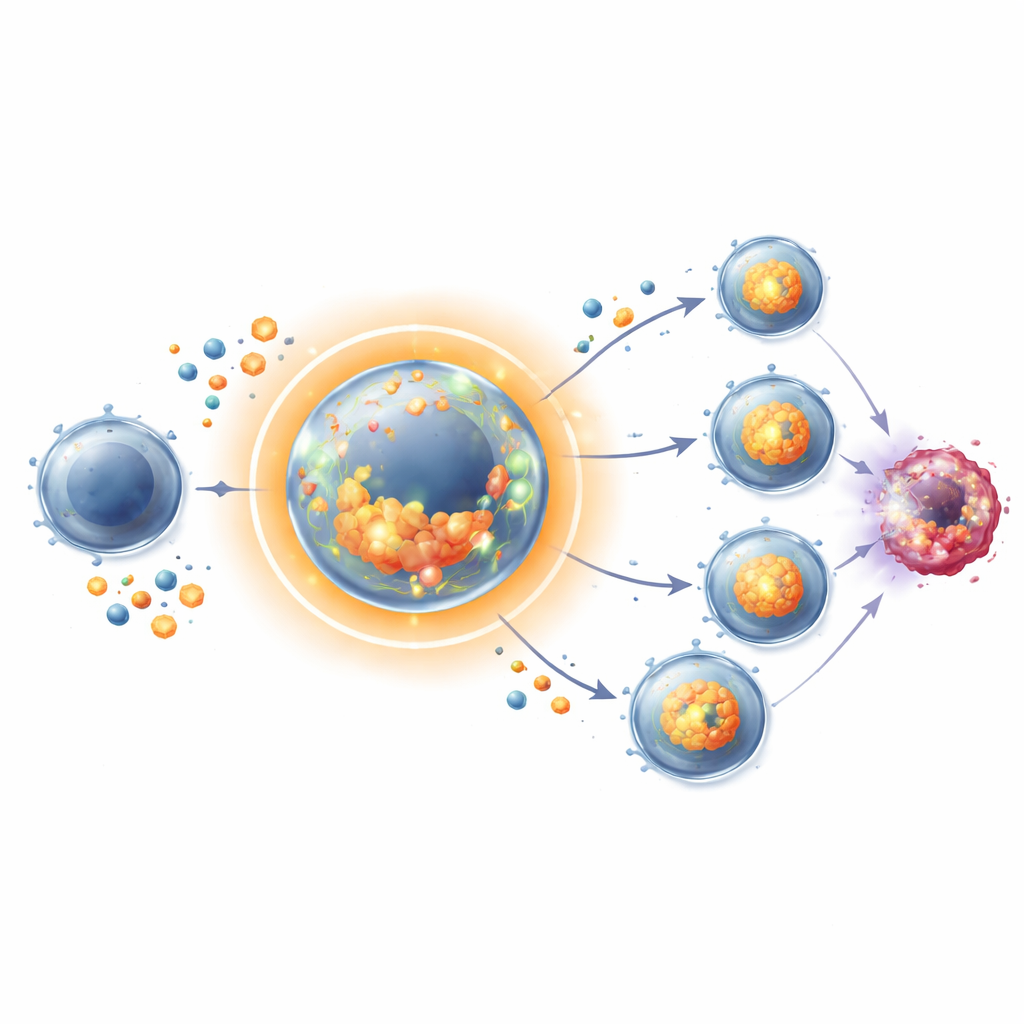
Att vända en cytostatikabiverkning till en fördel
Sammanfattningsvis visar studien att ett tillfälligt uppehåll i delning kan vändas från en nackdel till en fördel för cancermotverkande T-celler. Genom att pausa vid rätt tidpunkt lagerför dessa celler näring, ökar sin metaboliska kapacitet och badar sig i sina egna tillväxtsignaler. När de åter släpps expanderar de snabbt och angriper tumörer mer effektivt, särskilt i kombination med befintliga immunoterapier. För patienter antyder detta arbete att noggrant tajmad användning av cellcykelhämmare kan omdesignas inte bara för att förgifta tumörer utan också för att träna immunsystemet att bekämpa dem hårdare och längre.
Citering: van Haften, F.J., van der Sluis, T.C., Hepp, H.S. et al. Cell cycle arrest enhances CD8+ T cell effector function by potentiating glucose metabolism and IL-2 signaling. Nat Immunol 27, 463–475 (2026). https://doi.org/10.1038/s41590-025-02407-0
Nyckelord: CD8 T-celler, cellcykelstopp, cancerimmunoterapi, T-cellsmetabolism, interleukin-2