Clear Sky Science · sv
Fininställning av BACH2-dosering balanserar stamcellsdrag och effektorfunktion för att förbättra antitumör T-cellsbehandling
Hjälpa cancerbekämpande celler att hålla längre
Många av dagens mest lovande cancerbehandlingar bygger på uppgraderade versioner av kroppens egna immunceller. Dessa konstruerade T‑celler blir dock ofta snabbt utmattade inne i tumörer, vilket begränsar deras effektivitet. Den här studien undersöker ett sätt att få cancerbekämpande T‑celler att hålla längre utan att tappa sin dödande förmåga genom att noggrant justera aktiviteten hos en enda styrande molekyl i cellerna.
Varför immunceller behöver både ungdom och styrka
Vårt immunsystem bygger på arbetsdelning. Vissa T‑celler fungerar som tåliga, stamliknande ”frö”-celler som lever länge och kan fortsätta skapa nya kämpar. Andra blir kortlivade ”soldat”-celler som gör det mesta av det omedelbara tumördödandet men snabbt slits ut. Effektiv cancerterapi behöver båda: en bestående reservoar av frön och en stadig tillförsel av soldater. Vid kroniska infektioner och tumörer glider många T‑celler däremot in i ett utmattat, terminalt tillstånd där de varken kan dela sig eller svara väl på behandling. Kliniska resultat med befintliga T‑cellsbehandlingar visar att patienter mår bättre när de infunderade cellerna innehåller fler stamliknande celler och kvarstår längre i kroppen.
En molekylär ratt för T‑cellsvila och aktivitet
Forskarna fokuserade på ett protein kallat BACH2, som hjälper till att hålla T‑celler i ett vilande, minneslikt tillstånd. I naturliga immunsvar är BACH2‑nivåerna höga i naiva och stamliknande T‑celler och sjunker när cellerna blir fullfjädrade mördare. Tidigare arbete visade att BACH2 skyddar mot överaktivering och till och med kan fungera som en tumörsuppressor i konstruerade T‑celler, vilket gör det till ett lockande men knepigt verktyg: för mycket vila kan göra cellerna för sömniga för att bekämpa cancer. När teamet tvingade T‑celler att producera stora mängder BACH2 hände just detta. Cellerna förblev i ett kviescent, stamliknande tillstånd, uttryckte färre aktiveringsmarkörer, producerade lite av de giftiga molekyler som behövs för att döda tumörceller och kontrollerade tumörer dåligt i möss.
Att hitta den "precis lagom" dosen
För att se om BACH2 kunde hjälpa snarare än hindra terapin om den ställdes in på rätt nivå, byggde författarna genetiska konstruktioner som gav endast en liten fraktion av den vanliga överuttrycksnivån—ungefär så mycket BACH2 som finns i friska minnes‑T‑celler. De bekräftade dessa doser genom att tagga proteinet och med masspektrometri för att räkna antalet kopior. Med detta lågdosystem i händerna stimulerade de upprepade gånger mus‑T‑celler i odling för att efterlikna den kroniska stressen i en tumör. Både hög och låg BACH2 minskade uppkomsten av terminalt utmattade celler och bevarade markörer för stamlikt beteende. Den avgörande skillnaden var att lågdos BACH2 tillät cellerna att behålla stark produktion av centrala cytokiner och enzymer, medan högdos BACH2 kraftigt undertryckte dessa effektorfunktioner och till och med minskade cellstorleken, ett tecken på svag aktivering.
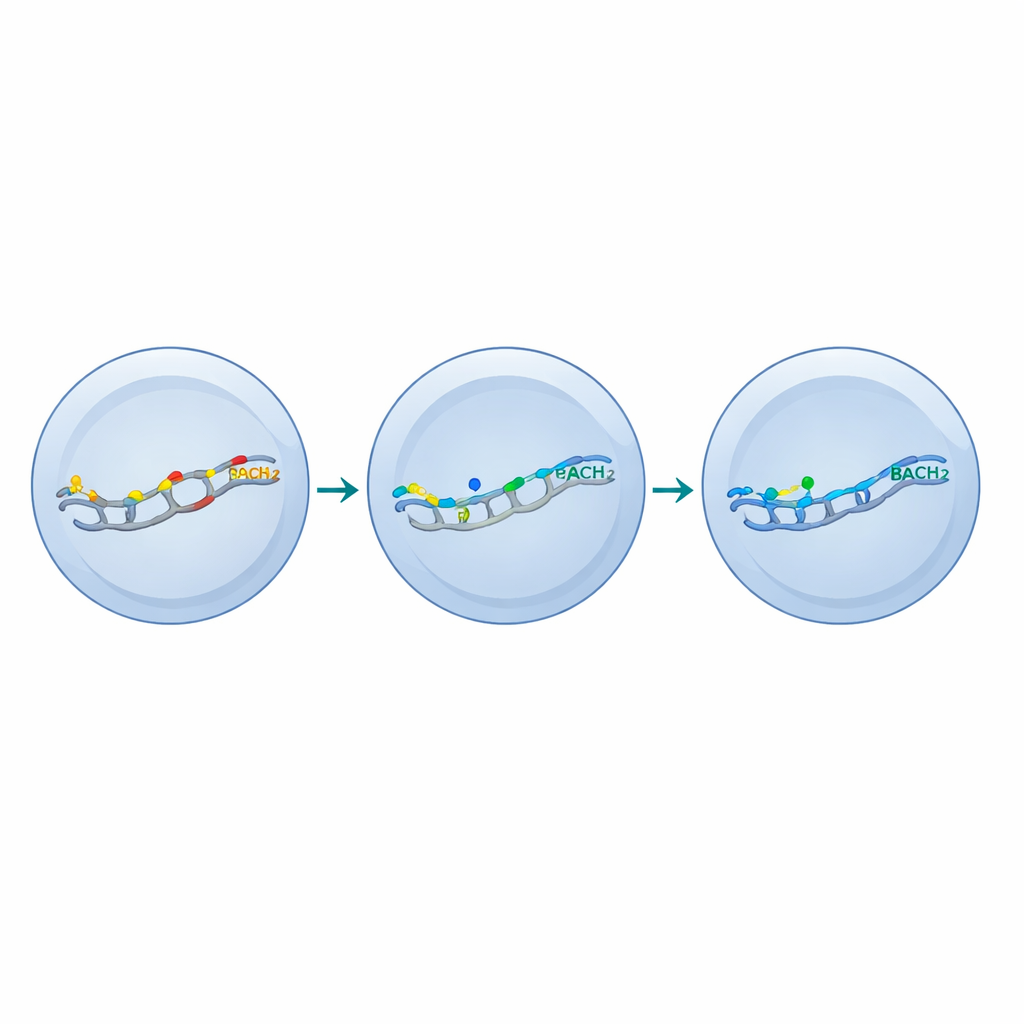
På molekylär nivå fann teamet att BACH2 verkar genom att konkurrera med en familj av aktivatorproteiner som gemensamt kallas AP‑1 vid specifika DNA‑motif. Gener som är starkt beroende av AP‑1 bar många av dessa motif och var särskilt känsliga för BACH2. Hög BACH2 trängde nästan fullständigt ut AP‑1 från dessa ställen och slog av många effektorgener. Lågdos BACH2 minskade endast delvis AP‑1‑bindningen, dämpade selektivt gener som driver terminal utmattning samtidigt som en stor del av det fördelaktiga effektorprogrammet sparades. I tumörer ackumulerade T‑celler konstruerade med lågdos BACH2 bättre, bibehöll både stamliknande och mer differentierade delmängder och genererade fler cytokinproducerande celler per gram tumör, vilket ledde till markant förbättrad kontroll av melanom och kolorektal cancer i musmodeller. 
Skapa hybrida T‑celler som uthärdar och attackerar
Genom att studera T‑celler som antingen uttryckte eller inte uttryckte en ytmolekyl kopplad till stamlikt beteende visade forskarna att lågdos BACH2 omformade de mest differentierade, utmattade cellerna till ett hybridtillstånd. Dessa celler fick utvalda egenskaper från stamliknande T‑celler—såsom gener associerade med långlivighet och homing—samtidigt som de behöll kärnegenskaper hos aktiva effektorceller, inklusive kraftfull cytokinproduktion och proliferation. Med andra ord, istället för att tvinga alla celler in i ett tyst stamtillstånd höjde dosanpassad BACH2 en minimumnivå av självförnyelse och återhållsamhet, särskilt i celler som annars skulle brinna ut.
En bredare strategi för säkrare, starkare cellterapier
För att testa om detta koncept sträcker sig bortom BACH2 applicerade författarna samma doseringstrick på ett annat kviescensfrämjande protein, FOXO1. Återigen ökade höga nivåer stamliknande markörer men försvagade effektorfunktionerna, medan låga, noggrant satta doser bevarade både hållbarhet och dödande kapacitet och förbättrade tumörkontrollen i möss. Tillsammans visar dessa fynd att hur mycket av ett reglerande protein som uttrycks kan helt förändra beteendet hos konstruerade T‑celler. Istället för att förlita sig på permanent hyperaktiverade, potentiellt cancerframkallande kretsar kan kliniker utforma säkrare terapier genom att finjustera naturliga "vila‑ och reparations"‑faktorer så att T‑celler stannar kvar i striden längre utan att tappa sin styrka.
Citering: Conti, A.G., Evans, A.C., von Linde, T. et al. Fine-tuning BACH2 dosage balances stemness and effector function to enhance antitumor T cell therapy. Nat Immunol 27, 436–451 (2026). https://doi.org/10.1038/s41590-025-02389-z
Nyckelord: T-cellsbehandling, cancerimmunterapi, BACH2, cellulär kviescens, gen-dosering