Clear Sky Science · sv
Ingenjörsarbete med xylosyltransferaser för att manipulera proteoglykaner i däggdjursceller
Varför cellernas “rockar” spelar roll
Varje cell i vår kropp bär en molekylär ”rock” som hjälper den att kommunicera med grannar och känna av omgivningen. En viktig del av denna rock utgörs av proteoglykaner—proteiner dekorerade med långa sockerkedjor som fungerar som små antenner för tillväxtfaktorer, immunsignaler och strukturella ledtrådar. När denna sockerdekoration går fel kan utveckling störas och vävnader som ben och muskler bli hårt drabbade. Trots det har forskare haft svårt att kartlägga exakt vilka proteiner som bär dessa kedjor och hur enskilda komponenter i rocken påverkar cellbeteende. Denna studie presenterar en precis kemisk strategi för att tagga och återskapa dessa sockerkedjor på levande däggdjursceller, vilket öppnar en väg för att läsa och skriva om den information som finns på deras ytor. 
Omkoppling av det första steget i sockerfästande
Bygget av proteoglykaner börjar när en särskild enzymfamilj, xylosyltransferaserna XT1 och XT2, sätter den första sockern på ett protein och markerar platsen där en lång kedja kommer att växa. Eftersom båda enzymerna kan utföra detta första steg har det varit svårt att avgöra vilka proteiner vardera arbetar på inne i celler. Författarna använde en ”grop‑och‑knöl”‑design—vanlig inom modern kemisk biologi—för att lösa detta. De formade försiktigt om XT1:s aktiva säte, skapade extra utrymme (”gropen”) och introducerade en matchande, något bulkigare sockerbyggsten, 6AzGlc (”knölen”). Det konstruerade XT1 kan nu använda detta modifierade socker, medan det naturliga enzymet inte kan det, vilket tillåter forskarna att endast tagga de proteiner som berörs av det omdesignade enzymet.
Smuggla in ett skräddarsytt socker i cellerna
För att få detta till att fungera i levande celler var teamet tvunget att leverera den bumpade sockern i en form som cellens ämnesomsättning kunde känna igen. Istället för att förlita sig på normala sockerupptagsvägar—som inte hanterar xylose‑analoger väl—byggde de en inkapslad version av 6AzGlc med en dold fosfatgrupp. När den väl kom in i cytosolen blottar cellulära enzymer denna grupp och omvandlar molekylen till UDP‑6AzGlc, den aktiverade formen som krävs av de konstruerade xylosyltransferaserna. Noggrann kromatografi bekräftade att celler behandlade med rätt konfigurerad inkapslad förening producerade betydande mängder av den aktiverade designersockern, medan en spegelbilds‑kontroll producerade nästan inget. 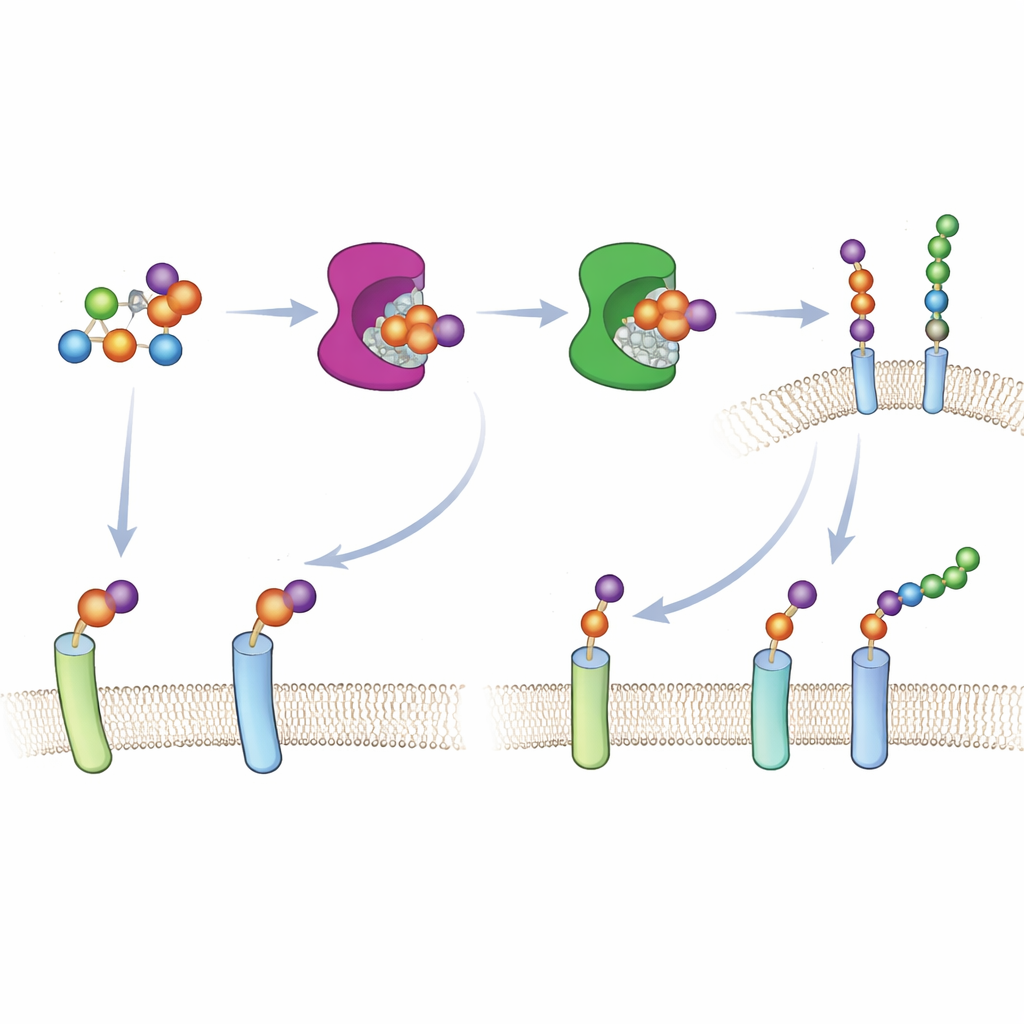
Tagga och identifiera de dolda aktörerna
Med både det modifierade enzymet och den aktiverade sockern på plats visade forskarna att endast celler som uttryckte det konstruerade XT1 eller XT2 inkorporerade 6AzGlc‑taggen i sina ytegende proteoglykaner. Azidgruppen på 6AzGlc fungerar som ett litet kemiskt handtag som kan ”klickas” till fluorescerande färgämnen eller biotin, vilket möjliggör visualisering och berikning av taggade proteiner. Masspektrometri av berikade prover avslöjade en rik samling av kända proteoglykaner—inbegripet decorin, flera glypicaner, syndecan‑4, CD44 och versican—vilket bekräftar att systemet markerar genuina sockerbärande proteiner. Viktigt är att de konstruerade enzymerna bevarade samma sekvenspreferenser som sina naturliga motsvarigheter, vilket innebär att den kemiska taggen installeras vid autentiska fästpunkter snarare än vid nya, artificiella positioner.
Bygga designer‑proteoglykaner
En oväntad bonus med 6AzGlc‑taggen är att den, till skillnad från den naturliga startsockern, inte kan förlängas till en fullängdskedja av nedströms enzymer. Detta kapslar effektivt kedjan och förenklar den molekylära struktur som behöver analyseras med masspektrometri. Författarna vände denna egenskap till ett verktyg: efter att XT1 har satt 6AzGlc vid en naturlig fästpunkt använder de klickkemi för att fästa syntetiska heparinfragment, och skapar så ”designer‑proteoglykaner” med precist definierade sockerkedjor. I bröstcancerceller som saknar sitt eget syndecan‑1 återställde tillskottet av sådana designer‑versioner normalt utbredningsbeteende på en proteinbeklädd yta, vilket visar att den kemiskt återbyggda proteoglykanen funktionellt kan ersätta den naturliga.
Vad detta betyder för biologi och medicin
Detta arbete levererar ett kraftfullt verktygsset för att selektivt märka och manipulera de sockerkedjor som styr hur celler kommunicerar. Genom att skilja på rollerna för XT1 och XT2 och endast tagga deras direkta mål kan forskare nu kartlägga vilka proteoglykaner som verkar i specifika vävnader och sjukdomstillstånd. Möjligheten att stoppa naturlig kedjeutväxt och ersätta den med skräddarsydda sockerstrukturer gör det också möjligt att dissekera hur mycket av en proteoglykanfunktion som bärs av dess proteinryggrad jämfört med dess sockerrock. På längre sikt kan sådan precisionsingenjörskonst hjälpa till att avkoda komplex signalering vid cellytan och inspirera terapier som reparerar eller omprogrammerar defekta cellulära rockar vid utvecklingsstörningar, cancer och andra sjukdomar.
Citering: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Nyckelord: proteoglykaner, glykosaminoglykaner, xylosyltransferas, kemisk biologi, cellsignalering vid ytan