Clear Sky Science · sv
En enda allosterisk plats förenar aktivering, modulering och hämning i TRPM5
Hur en liten grindvakt formar smak och ämnesomsättning
De livsmedel vi njuter av och hur våra kroppar hanterar socker beror båda på mikroskopiska ”grindvakt”-proteiner i våra celler. En sådan grindvakt, en kanal kallad TRPM5, hjälper oss att uppfatta sött, bittert och umami och deltar i bukspottkörtelns frisättning av insulin. Den här studien visar hur ett enda litet fack på TRPM5 kan fungera som en huvudkontrollknapp — slå på kanalen, finjustera dess känslighet och till och med stänga av den — insikter som kan vägleda framtida behandlingar för diabetes, fetma och tarmrubbningar.
En kanal i skärningspunkten mellan smak och blodsocker
TRPM5 sitter i membranen hos smakceller på tungan, hormonproducerande celler i tarmen och insulinfrisättande celler i bukspottkörteln. När kalciumnivåerna inne i dessa celler stiger öppnas TRPM5 och släpper igenom positivt laddade joner, vilket kortvarigt ändrar cellens spänningsnivå. I smaklökarna berättar denna elektriska signal för hjärnan att något sött, bittert eller umami finns på tungan. I bukspottkörteln hjälper den till att finjustera insulinpulser efter en måltid. Människor och djur med nedsatt TRPM5-funktion visar problem med insulinfrisättning och blodsockerreglering, vilket tyder på att läkemedel som riktar sig mot TRPM5 en dag kan hjälpa till vid metabola sjukdomar. Ändå saknade forskare fram tills nyligen precisa verktyg för att slå på eller av denna kanal.
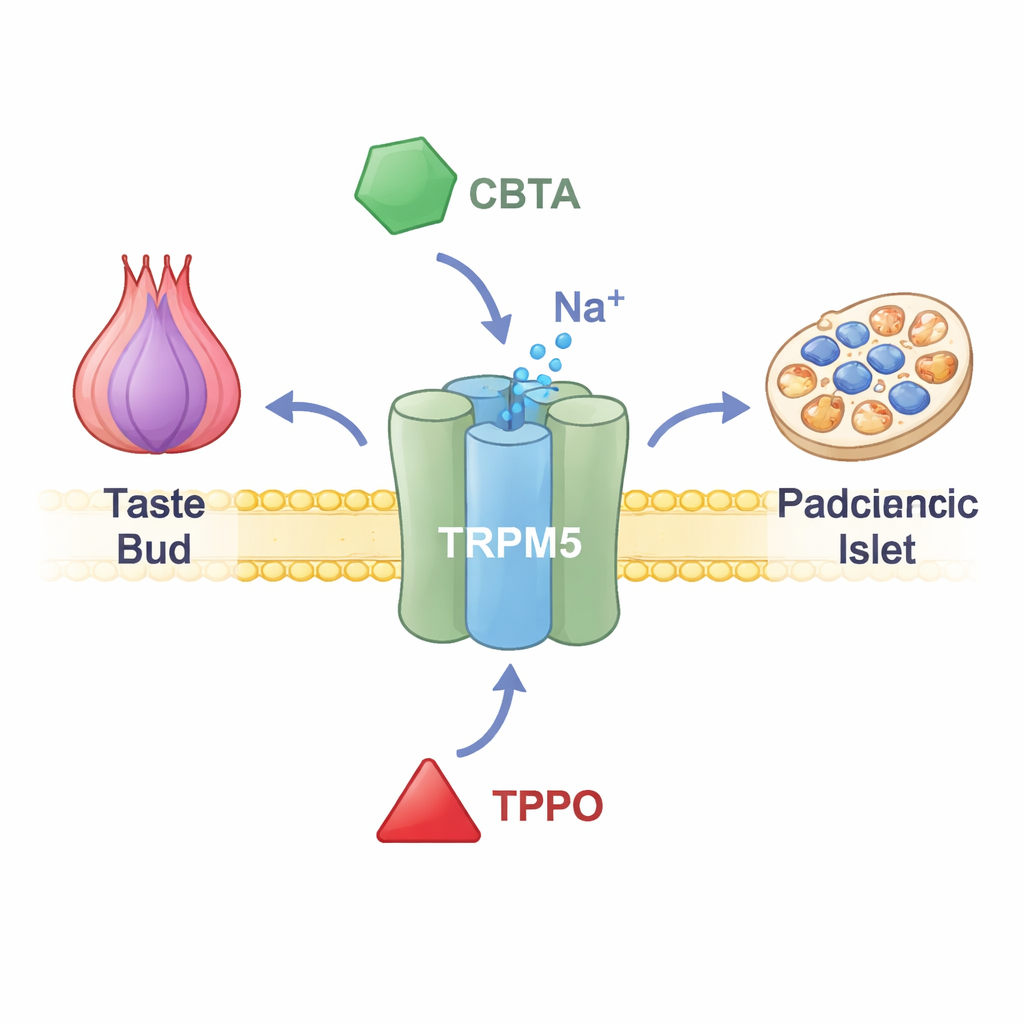
En ny kemisk strömbrytare som överladdar kanalen
Forskarna fokuserade på en syntetisk förening kallad CBTA, tidigare känd för att stimulera TRPM5 men inte väl förstådd. Med elektriska inspelningar från celler som konstruerats för att producera TRPM5 visade de att CBTA kan öppna kanalen även när kalcium nästan saknas, vilket bevisar att den fungerar som en sann aktivator snarare än bara förstärker kalciums effekter. När små mängder kalcium finns — nivåer som normalt låter TRPM5 förbli tyst — verkar CBTA och kalcium tillsammans och genererar mycket större strömmar än någon av dem ensam. Det innebär att CBTA gör TRPM5 ovanligt känslig, så att nästan vilande kalciumnivåer plötsligt blir tillräckliga för att slå kanalen helt öppen.
En dold kontrollficka avslöjad med cryo-EM
För att se hur detta fungerar på atomnivå använde teamet kryoelektronmikroskopi för att få tredimensionella ögonblicksbilder av TRPM5 under olika förhållanden. De upptäckte att CBTA väljer sig en tidigare oupptäckt kavitet i den övre delen av en spänningskänslig region av kanalen, precis ovanför där kalcium vanligtvis binder. Denna kavitet, formad av en klunga aminosyror, fungerar som en precis dockningsplats. När forskarna muterade nyckelbyggstenar som beklädde denna ficka kunde CBTA inte längre aktivera TRPM5, även om kalcium fortfarande fungerade, vilket bekräftar att denna lilla nisch är avgörande för läkemedlets verkan. Slående nog omformar CBTA-bindningen subtilt närliggande delar av proteinet på ett sätt som gör det mycket lättare för kalcium att inta sin vanliga plats, och förklarar den dramatiska synergin som observerades i de elektriska mätningarna.
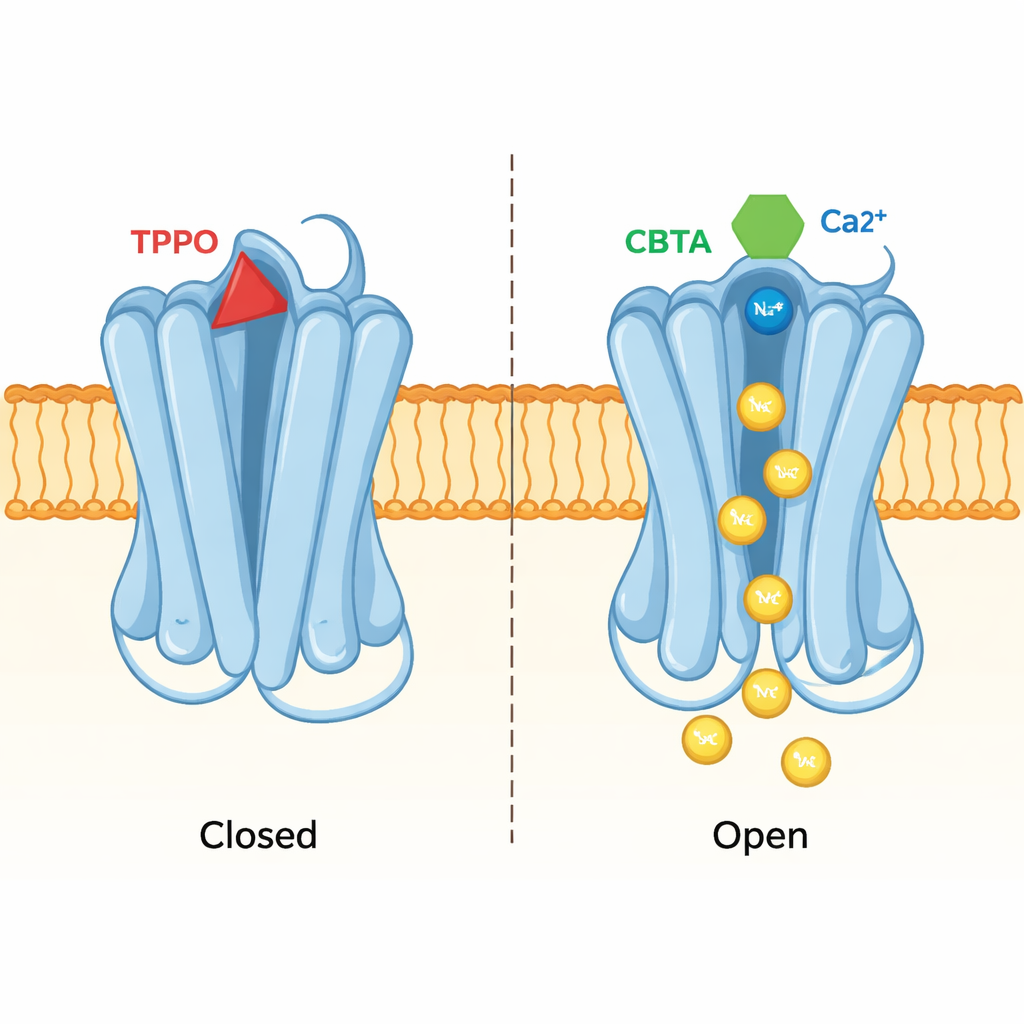
En ficka, två motsatta utfall
Samma strukturella ansats avslöjade hur en hämmare kallad TPPO använder exakt samma ficka för att ge motsatt effekt. När TPPO binder förblir båda kalciumsätena på TRPM5 fyllda, men kanalens centrala por förblir tilltryckt stängd och inga joner passerar. Jämförelser mellan TPPO-bundna och CBTA-bundna strukturer visade att deras olika former trycker på närliggande protegment åt motsatta håll. CBTA uppmuntrar rörelser som sprider sig till poren och öppnar den; TPPO istället stör kommunikationen mellan fickan och poren, vilket håller grinden stängd. I praktiken kan denna enda ficka fungera antingen som en gaspedal eller som en broms, beroende på vilken molekyl som ockuperar den.
Omdirigering av kanalens interna kopplingar
Studien visar också att denna kontrollficka kan ta över uppgifter som normalt sköts av en separat kalciumbindande region inne i cellen. I mutanta kanaler där den vanliga interna kalciumplatsen är inaktiverad kunde kalcium ensam inte öppna TRPM5. Ändå kunde CBTA fortfarande slå på dessa mutanter och omforma ett centralt strukturellt element som länkar kanalens inre och yttre delar. I andra mutanter som bryter kopplingen mellan kalciumbindning och porets öppnande återställde tillsats av CBTA normal funktion. Dessa resultat visar att den nyligen identifierade platsen kan omdirigera eller reparera kommunikationen mellan olika kanaldomäner och fungerar som en flexibel nav för långdistanssignalering inom proteinet.
Varför detta är viktigt för framtida läkemedel
För icke-specialister är huvudbudskapet att forskarna har funnit en enda läkemedelskänslig ficka på TRPM5 som kan integrera aktivering, finjustering och avstängning. En liten aktivator som CBTA kan både efterlikna kalcium och kraftigt öka kanalens känslighet, medan en annan förening, TPPO, kan låsa samma kanal stängd — allt genom att docka på samma plats. Denna enhetliga bild av hur TRPM5 kontrolleras öppnar dörren för att designa skräddarsydda molekyler som antingen förstärker eller dämpar dess aktivitet i specifika vävnader, med potentiella tillämpningar från förbättrade smakbaserade terapier och läkemedel för tarmmotilitet till nya strategier för att hantera blodsocker och metabola sjukdomar.
Citering: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Nyckelord: TRPM5-kanal, smakuppfattning, insulinutsöndring, jonkanalsstyrning, allosterisk modulering