Clear Sky Science · sv
Genomeomfattande associationsanalyser av autoimmun hypotyreos visar autoimmuna och sköldkörtelspecifika bidrag samt ett omvänt samband med cancerrisk
Varför detta spelar roll för vardagshälsan
Många känner sig trötta, frusna eller mentalt dimmiga utan att inse att sköldkörteln kan vara orsaken. Autoimmun hypotyreos, där kroppens eget försvar långsamt angriper sköldkörteln, drabbar mer än en av tjugo personer. Denna studie använder genetiska data från hundratusentals frivilliga för att ställa två stora frågor: vilka ärftliga förändringar i vårt DNA ökar sannolikheten för detta tillstånd, och hur hänger dessa förändringar ihop med risken att utveckla cancer? Svaren visar en överraskande avvägning mellan ett immunsystem som ibland skadar sköldkörteln men som samtidigt kan ge ett extra skydd mot tumörer.
Över hela genomet
Forskarna kombinerade journalsuppgifter och genetisk information från två stora befolkningsprojekt, FinnGen i Finland och UK Biobank i Storbritannien. De fokuserade på personer som behövde långvarig ersättning med sköldkörtelhormon och uteslöt noggrant dem vars sköldkörtelproblem berodde på operation, cancer eller andra icke-autoimmuna orsaker. Detta gav över 81 000 fall av autoimmun hypotyreos och mer än 700 000 kontroller, vilket gör det till den hittills största studien av detta tillstånd. Genom att skanna miljontals DNA-markörer över genomet upptäckte de 418 oberoende genetiska signaler utanför huvudklustret av immungen, fördelade över minst 280 regioner i genomet. Många av dessa signaler involverade sällsynta eller lågfreventa DNA-förändringar som ändrar proteiners struktur och därmed ger direkta ledtrådar till den bakomliggande biologin.
Att skilja generella immuneffekter från sköldkörtelspecifika
Autoimmun hypotyreos ligger i skärningspunkten mellan generell autoimmunitet och sköldkörtelns unika biologi. För att separera dessa komponenter jämförde teamet sina resultat med genetiska studier av andra autoimmuna sjukdomar och med blodnivåer av sköldkörtelstimulerande hormon, den centrala kliniska markören för att upptäcka underfunktion i sköldkörteln. Med en bayesiansk klassificeringsmetod grupperade de genetiska signalerna i sådana som delas med breda autoimmuna sjukdomar och sådana som är mer specifika för reglering av sköldkörtelhormon. De uppskattade att ungefär 38 % av signalerna verkar via generella immunvägar som påverkar många autoimmuna tillstånd, medan omkring 20 % verkar främst genom sköldkörtelfunktion. De sköldkörtel-fokuserade varianterna påverkade ofta hormonnivåer och gener som är aktiva i sköldkörtelvävnad, medan de generella immunsignalvarianterna var mer aktiva i T‑celler, de vita blodkroppar som koordinerar immunsvar.
Inzoomning på en viktig immunomkopplare
Ett särskilt iögonfallande fynd rörde en sällsynt DNA-förändring i genen ZAP70, som kodar för ett centralt signalprotein i T‑celler. Svåra defekter i detta protein är kända för att orsaka djup immunbrist, men varianten som identifierats här ger endast en partiell funktionsminskning. Laboratorieexperiment i konstruerade T‑celler visade att det förändrade ZAP70 försvagar, men blockerar inte helt, den signaleringskaskad som normalt följer igenkänning av ett mål. Celler med varianten hade svårare att slå på aktiveringsmarkörer och efterföljande signalsteg. Detta dämpade svar verkar rubba den känsliga balans som normalt rensar bort självreaktiva T‑celler, vilket predisponerar bärare för autoimmuna sjukdomar samtidigt som det måttligt ökar risken för vissa immunbrister.
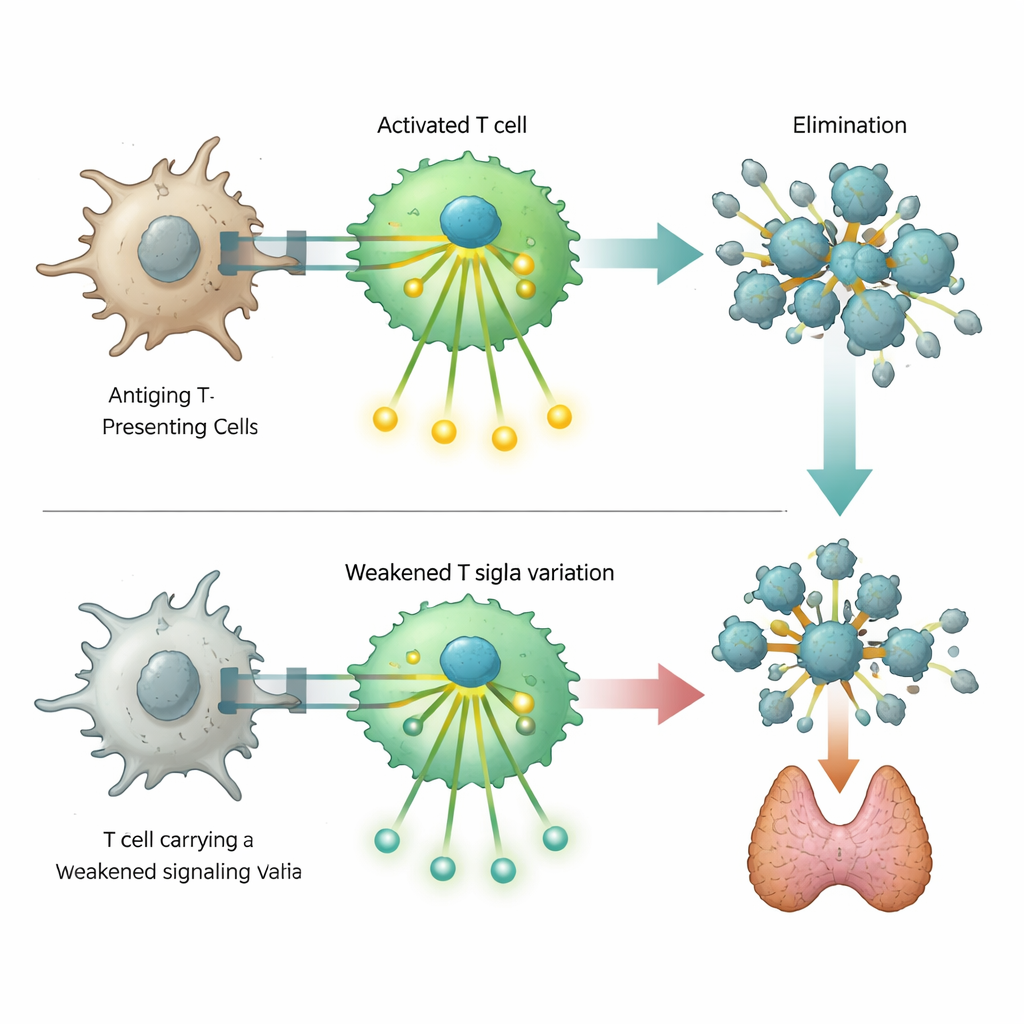
En oväntad koppling till cancerskydd
Där samma immunsystemsvägar som driver autoimmunitet också kan attackera tumörer, frågade författarna hur den genetiska risken för autoimmun hypotyreos förhåller sig till cancerrisk. De räknade fram en polygen riskpoäng som sammanfattar varje persons ärftliga benägenhet för hypotyreos och testade dess samband med många sjukdomar i de finska uppgifterna. Som förväntat korrelerade en högre poäng med ökad risk för olika autoimmuna tillstånd. Mer överraskande var ett konsekvent mönster av lägre risk för flera cancerformer, särskilt basalcellscancer och andra hudcancerformer, men också bröst‑ och prostatacancer samt en totalgrupp för ”alla cancerformer”. När teamet undersökte cancerstudier på genomnivå direkt, påverkade ungefär 10 % av de hypotyreos‑länkade platserna också hudcancer, där samma genetiska variant i allmänhet ökade risken för sköldkörtelautoimmunitet samtidigt som den minskade risken för hudcancer. Dessa delade varianter koncentrerades till immungerelaterade gener, inklusive välkända läkemedelsmål som används i checkpoint‑immunterapi.
Vad detta innebär för patienter och medicin
Ur ett vardagligt perspektiv visar arbetet att vissa personer föds med ett immunsystem som är ställt lite ”hetare”, vilket gör dem mer benägna till långsam, ofta tyst skada på sköldkörteln men samtidigt bättre rustade att upptäcka och eliminera växande cancer. Studien skiljer ut vilka genetiska förändringar som verkar via generell immunsvarshöjning och vilka som specifikt påverkar produktionen av sköldkörtelhormon, vilket förklarar varför tillstånd som Hashimotos sjukdom och Graves sjukdom kan dela vissa riskgener men driva sköldkörtelfunktionen i motsatta riktningar. Den hjälper också att förklara varför patienter som utvecklar sköldkörtelproblem under behandling med immunstimulerande cancerläkemedel ofta svarar bättre på dessa behandlingar. Sammantaget tyder fynden på att vanlig, naturlig variation i immunkontrollpunkter och signaleringsgener formar både autoimmun sköldkörtelsjukdom och livstidscancerrisk, och ger nya ledtrådar för prevention och mer personanpassad användning av immunterapier.
Citering: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Nyckelord: autoimmun hypotyreos, sköldkörtelsjukdom, genetisk risk, immunsystem, cancerskydd