Clear Sky Science · sv
GGC-upprepningsexpansioner inom nya öppna läsramar översätts till toxiska polyglycinproteiner vid okulofaryngodistal myopati
Dolda budskap i vårt DNA
De flesta av oss lärde oss i skolan att bara en liten del av vårt DNA faktiskt kodar för proteiner, medan resten en gång avfärdades som ”skräp”. Denna studie vänder på den idén. Den visar att små, förbisettade avsnitt av repetitivt DNA i hemlighet kan ge upphov till nya proteiner som skadar muskler och hjärna, vilket hjälper till att förklara en grupp sällsynta men förödande neurologiska sjukdomar — och pekar på en möjlig behandlingsväg.
Repetitivt DNA och mystiska muskelsjukdomar
Vårt genom är fullt av små upprepade sekvenser, som trebokstavssyllabler kopierade gång på gång. När vissa av dessa upprepningar blir för långa kan de orsaka mer än 60 kända mänskliga sjukdomar. Vid okulofaryngodistal myopati (OPDM) och en närbesläktad sjukdom med hjärnförändringar kallad OPML utvecklar patienterna hängande ögonlock, sväljsvårigheter, svaghet i händer och fötter och ibland mer utbredda nerv- och hjärnproblem. Under mikroskopet ser läkare karaktäristiska klumpar av protein inne i muskel- och nervceller, men fram till nu har det varit oklart hur upprepningar som ligger i så kallade ”icke-kodande” delar av DNA kan producera toxiska proteiner.
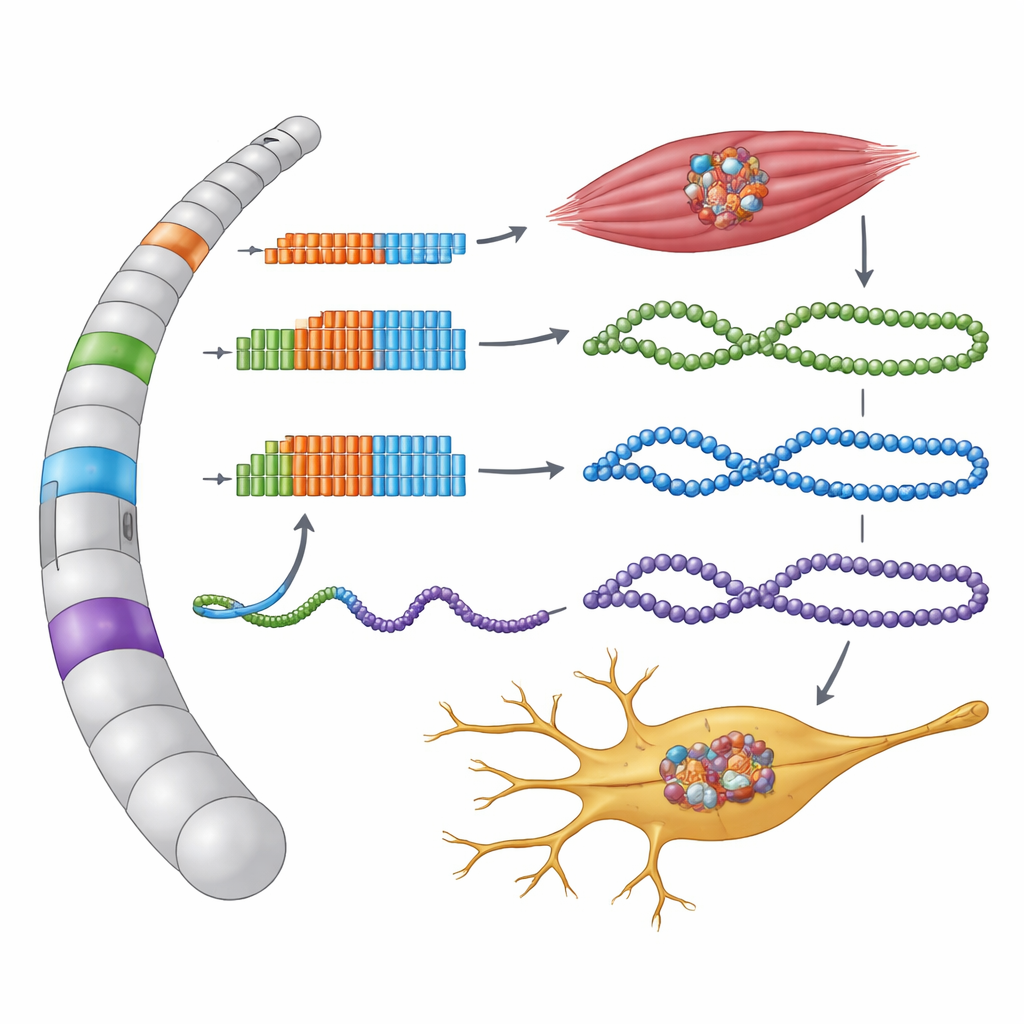
Icke-kodande regioner som i hemlighet tillverkar protein
Forskarlaget fokuserade på DNA-regioner där trebokstavssekvensen GGC upprepas många gånger inom flera gener som kopplats till OPDM och OPML. Dessa upprepningar ligger i områden som annoterats som icke-kodande — oöversatta ändar av gener eller långa RNA som man tidigare trott inte producerar protein alls. Genom att återskapa dessa mänskliga sekvenser i celler och följa hur de läses upptäckte gruppen att varje GGC-stretch faktiskt ligger inne i en liten, tidigare oigenkänd proteinkodande enhet kallad en liten öppen läsram. När cellerna läser dessa dolda instruktioner översätts varje GGC-upprepning till aminosyran glycin, vilket bildar ovanligt långa ”polyglycinkedjor” på nya mikroproteiner.
Nya toxiska proteiner som klumpar sig och dödar celler
Med hjälp av specialframställda antikroppar visade forskarna att dessa mikroproteiner som bär polyglycin finns i muskelfragment från patienter och koncentreras exakt där de underliga p62-positiva proteinklumparna hittas. De tvingade sedan mänskliga muskelceller, fruktflugor och möss att producera samma typer av polyglycinproteiner. I alla tre systemen kondenserade proteinerna till runda, täta inklusioner i cytoplasman och kärnan, liknande det som ses i patientvävnad. Celler som producerade dessa proteiner hade större benägenhet att dö, och hos möss visade de drabbade musklerna förtunnade fibrer, internaliserade cellkärnor och tecken på inflammation. När proteinerna ansamlades i hjärna och hjärta utvecklade djuren rörelseproblem, neurodegeneration, kardiomyopati och kortare livslängd, vilket matchar många av de symptom som rapporterats hos patienter.

En kärnfarlig egenskap, många lokala varianter
Även om dessa mikroproteiner delar samma centrala egenskap — en lång kedja av glycinrester — är de inte identiska. Var och en uppstår från en annorlunda liten läsram i en annan gen och har därför unika aminosyrasegment som flankar polyglycinsträckan. Forskarna fann att dessa omgivande segment starkt påverkar hur proteinerna beter sig: var i cellen de ansamlas, hur lätt de bildar aggregat, vilka cellulära partner de interagerar med och hur toxiska de är för muskel- och nervceller. Vissa varianter var särskilt skadliga och utlöste snabbt inklusionsbildning och celldöd, medan andra var något mildare. Detta tyder på en gemensam toxisk kärnmekanism, finjusterad av den lokala sekvenskontexten.
Ett första steg mot en gemensam behandlingsstrategi
Positivt nog identifierade forskarna även en liten molekyl, den katjoniska porfyrinen TMPyP4, som kan dämpa både uppbyggnaden och toxiciteten hos dessa polyglycinproteiner i celler och i en fruktflugemodell. TMPyP4 verkar främst verka genom att störa översättningen av GC-rika upprepningsregioner, vilket minskar produktionen av de skadliga proteinerna utan att allmänt stänga av proteinsyntesen. Även om den är långt ifrån ett färdigt läkemedel erbjuder den ett principbevis för att en enda terapeutisk strategi en dag kan hjälpa patienter med flera besläktade tillstånd drivna av liknande upprepningsexpansioner.
Vad detta betyder för vår förståelse av sjukdom
För en icke-specialist är huvudbudskapet slående: DNA-sekvenser som länge avfärdats som icke-kodande kan dölja små proteinkoncept som blir farliga när vissa upprepningar expanderar. Vid OPDM, OPML, neuronal intranukleär inklusionssjukdom och närbesläktade störningar översätts dessa expanderade GGC-upprepningar till klibbiga polyglycinproteiner som klumpar sig inne i celler och gradvis försämrar muskler, nerver och hjärna. Genom att avslöja denna gemensamma mekanism och en första kandidatförening som kan dämpa den, vidgar studien vår syn på vad som räknas som en gen och öppnar nya vägar mot behandling av en växande familj av upprepningsdrivna neurologiska sjukdomar.
Citering: Boivin, M., Yu, J., Eura, N. et al. GGC repeat expansions within new open reading frames are translated into toxic polyglycine proteins in oculopharyngodistal myopathy. Nat Genet 58, 517–529 (2026). https://doi.org/10.1038/s41588-026-02507-z
Nyckelord: okulofaryngodistal myopati, mikrosatellitisk upprepningsexpansion, polyglycinproteiner, översättning av icke-kodande DNA, neurodegenerativ muskelsjukdom