Clear Sky Science · sv
Minskad cyclin D3‑uttryck i erytrocyter skyddar mot malaria
Hur en subtil blodskillnad kan bekämpa en dödlig parasit
Malaria har format människans evolution i årtusenden och gynnat genetiska förändringar som hjälper människor överleva infektion. Denna studie upptäcker en sådan förändring i en sardinsk population: en liten förändring i DNA som svagt ändrar hur röda blodkroppar bildas. Den förändringen gör att de röda blodkropparna blir färre och större, höjer cellernas inre stresskemi och saboterar på så sätt tystmalariaparasiten som är beroende av dem för att växa.
En liten DNA‑förändring med stora konsekvenser
Forskarna fokuserade på en region i vårt DNA som kontrollerar ett protein kallat cyclin D3, som hjälper omogna blodceller att dela sig. I tidigare arbete kopplades en genetisk variant, rs112233623‑T, nära CCND3‑genen till röda blodkroppar som är färre till antal men större till storlek, samt till högre nivåer av vissa hemoglobinformer. Denna variant är ungefär tio gånger vanligare hos människor från Sardinien än i många andra europeiska grupper, vilket speglar öns långa historia som ett malaria‑hotspot. Teamet ställde en serie sammanhängande frågor: hur förändrar varianten blodcellsutvecklingen, varför är den så vanlig i Sardinien, och hindrar den faktiskt malariaparasiten?
Trögrande celldelningsmaskin för röda blodkroppar
För att se vad varianten gör i cellerna odlade forskarna förstadier till röda blodkroppar från volontärer som antingen bar två kopior av rs112233623‑T eller två kopior av den vanliga versionen. I celler med varianten var nivåerna av cyclin D3 tydligt lägre, och cellerna rörde sig långsammare genom den fas av cykeln där DNA kopieras och celler delar sig. Som ett resultat genomgick varje förstadie färre delningsrundor innan det mognade, vilket gav en blodbild med färre men större röda blodkroppar — mycket likt det som setts hos möss helt utan cyclin D3. I genetiska tester över tusentals sardinska volontärer framträdde rs112233623‑T som den huvudsakliga drivaren bakom detta blodcellsmönster.
Omkoppling av en genetisk strömbrytare i blodförstadier
Den avgörande DNA‑förändringen ligger i en "på‑av"‑kontrollregion, en förstärkare, som ökar CCND3‑aktiviteten i utvecklande röda celler. Teamet visade att insättning av rs112233623‑T kraftigt försvagade denna förstärkare i laboratoriets rapportörtester. Genom att dissekera den omgivande sekvensen fann de att den normala DNA‑sekvensen bildar en landningsplats för ett protein kallat SMAD3, som sätter igång CCND3. T‑versionen rubbar denna landningsplats och gynnar istället bindning av GATA1, ett protein som i detta sammanhang fungerar mer som en broms. I verkliga blodförstadier band SMAD3 starkt till den normala sekvensen men dåligt till varianten, och läkemedel som blockerade SMAD‑typens signaler ledde till att cyclin D3‑nivåerna föll. Tillsammans visar dessa experiment en enkel logik: färre SMAD3 "gå"‑signaler och fler GATA1 "stopp"‑signaler betyder mindre CCND3, långsammare celldelning och ändrad produktion av röda blodkroppar.
En evolutionär signatur från tidigare malaria
Varför blev denna till synes nackdelaktiga variant vanlig i Sardinien? Populationsgenetiska analyser gav en ledtråd. Jämfört med andra européer visar sardinerna ovanligt hög frekvens av rs112233623‑T, långa DNA‑stycken runt varianten med liten variation, och mönster som bäst förklaras av nylig positiv selektion snarare än slump. Med modeller för hur genvarianter ökar i frekvens över generationer uppskattade författarna att rs112233623‑T starkt gynnats i Sardiniens nära förflutna. Eftersom ön drabbades av intensiv malariasmittspridning fram till mitten av 1900‑talet resonerade författarna att skydd mot malaria var den mest sannolika fördelen.
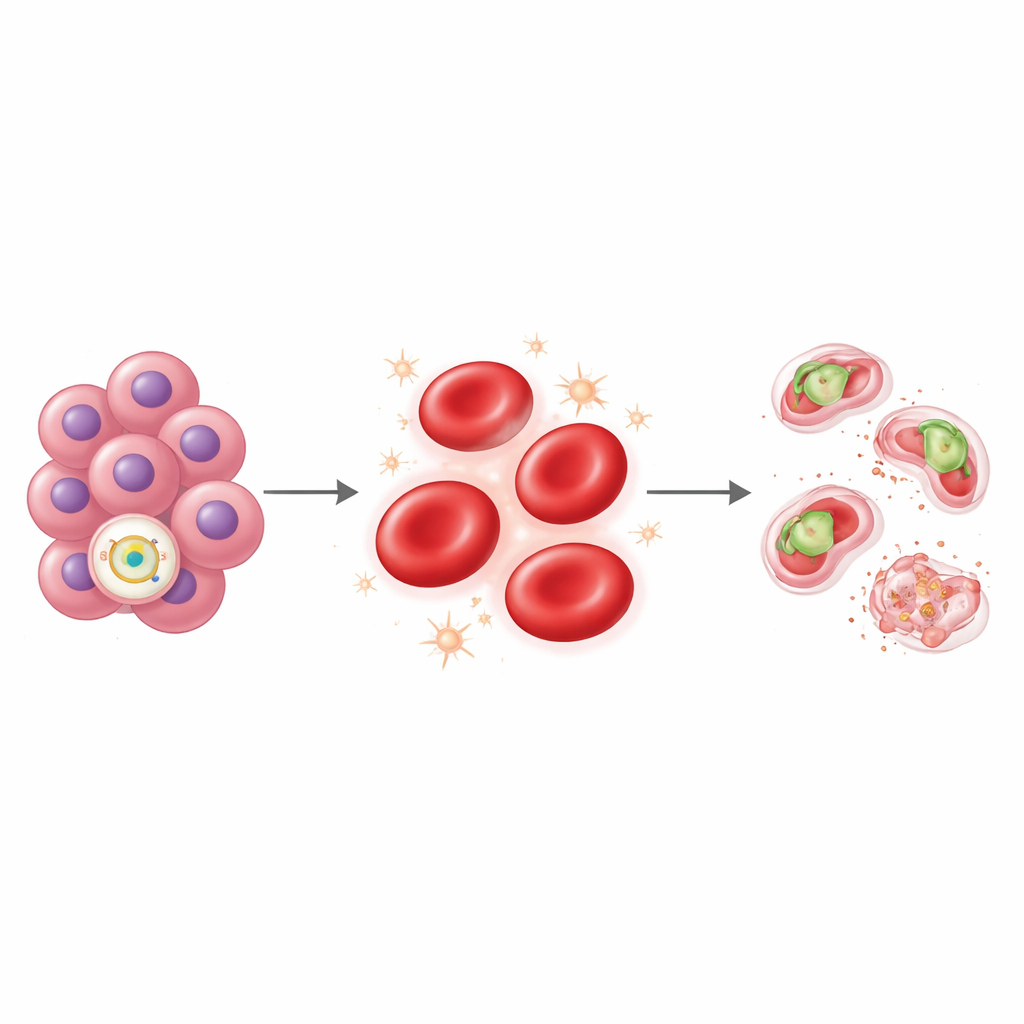
Stressa parasiten till döds inne i cellen
För att testa denna idé direkt infekterade teamet röda blodkroppar från noggrant genotypade sardinska volontärer med Plasmodium falciparum, parasiten som orsakar den dödligaste formen av malaria. Röda celler från personer som bar rs112233623‑T‑varianten tillät mycket sämre parasittillväxt över flera cykler än celler från dem utan varianten. Parasiter i dessa celler stannade ofta upp och dog istället för att slutföra sina vanliga utvecklingsstadier. Genom att mäta cellkemin inne i de röda cellerna fann forskarna högre nivåer av reaktiva syrearter — molekyler som orsakar oxidativ stress — hos variantbärarna. Ju högre den oxiderande stressen var, desto mindre växte parasiterna, vilket bildade en tydlig omvänd relation. Slående nog liknade detta stressbaserade handikapp det som ses hos personer med en välkänd skyddande egenskap: brist på enzymet G6PD, vilket länge kopplats till motstånd mot svår malaria.
Vad detta betyder för framtida malariakontroll
Enkelt uttryckt visar studien att en nedreglering av cyclin D3 i förstadier till röda blodkroppar gör de färdiga cellerna till en hårdare miljö för malariaparasiter, främst genom att öka den inre "rostningen" — oxidativa kemin — som parasiten inte fullt ut tål. Denna milda, ärftliga nedtrappning av rbc‑produktionen verkar ha belönats av naturligt urval i Sardinien eftersom den minskade risken för svåra infektioner med hög parasitmängd. Arbetet antyder att läkemedel som tillfälligt efterliknar denna genetiska effekt — genom att hämma CCND3 i benmärgen — skulle kunna komplettera befintliga antimalariabehandlingar och ytterligare rubba balansen till parasitens nackdel, samtidigt som man håller sig inom vad människokroppen tål.
Citering: Marini, M.G., Mingoia, M., Steri, M. et al. Reduced cyclin D3 expression in erythroid cells protects against malaria. Nature 651, 698–706 (2026). https://doi.org/10.1038/s41586-026-10110-9
Nyckelord: motstånd mot malaria, röda blodkroppar, mänsklig evolution, genetisk variant, oxidativ stress