Clear Sky Science · sv
GlycoRNA komplex med heparansulfat reglerar VEGF‑A‑signalering
Hur celler finjusterar kroppens blodkärlssignaler
Blodkärl uppstår inte bara där tillväxtsignaler förekommer—de måste kontrolleras noggrant för att ge näring åt vävnader utan att samtidigt gynna tumörer eller orsaka blindhet. Denna artikel avslöjar en oväntad "broms" på en huvudsaklig kärltillväxtsignal kallad VEGF‑A. Författarna visar att små RNA‑bitar, som pryder cellens utsida i samarbete med sockerarter och proteiner, kan dämpa VEGF‑A:s budskap och omforma vår bild av vilket språk celler använder vid sina ytor.
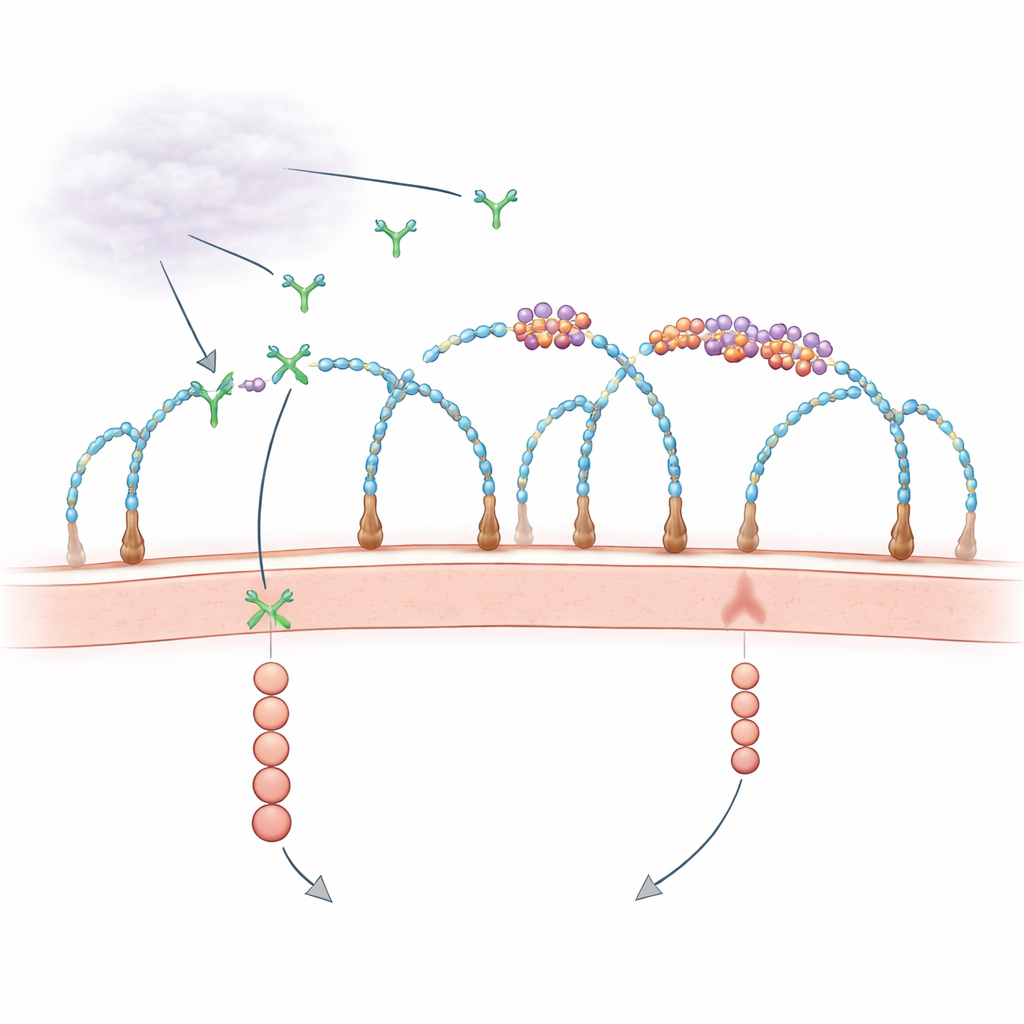
En överraskande roll för RNA på cellytan
I årtionden har biologer vetat att cellens yttre hölje, rikt på sockerdekorerade proteiner kallade heparansulfat‑proteoglykaner, fångar tillväxtfaktorer och visar upp dem för deras receptorer. Samtidigt har spridda observationer antytt att RNA‑fragment utanför celler kan påverka blodkärlsbildning, men aktörerna och mekanismerna var oklara. Nyare arbete visade att vissa små RNA är kemiskt förenade med komplexa sockerstrukturer och bildar ”glycoRNA”, och att vissa RNA‑bindande proteiner även finns på cellytan och klustrar tillsammans med dessa RNA. Den nya studien ställer en riktad fråga: styr dessa små RNA–protein‑öar vid membranet verkligen hur tillväxtsignaler som VEGF‑A tas emot?
Bygga klustrade RNA–protein‑öar med sockerkedjor
Genom att använda genomomfattande CRISPR‑knockout‑skärmar och högupplöst mikroskopi upptäckte forskarna att specifika sockerkedjor—heparansulfat med bestämda sulfateringstyper—är nödvändiga stommar för att montera dessa RNA–proteinkluster, som de kallar cell‑yt‑ribonukleoproteiner (csRNPs). När nyckelenzymer som bygger eller sulfaterar heparansulfat togs bort försvann klustren av glycoRNA och deras partnerproteiner från cellytan, trots att RNA och proteiner fortfarande fanns kvar inne i cellerna. Enzymer som klipper bort heparansulfatkedjor från ytan eller kemiskt blockerar sulfatering gav samma effekt. Dessa resultat visar att intakta, korrekt sulfaterade heparansulfatkedjor organiserar csRNPs till nanoskaliga öar vid membranet.
RNA‑kluster fungerar som bromsar på en stark kärltillväxtsignal
Teamet vände sig sedan till mänskliga endotelceller, som bekläder blodkärl och svarar på VEGF‑A. De fann att dessa celler också visar heparansulfat‑förankrade csRNP‑kluster. Behandling av levande celler med RNaser, enzymer som bryter ner RNA, avlägsnade RNA‑komponenten utan att störa de underliggande sockerkedjorna. Under dessa förhållanden gav VEGF‑A:s vanligaste, heparan‑bindande form (VEGF‑A165) mycket starkare aktivering av den nedströms ERK‑signalvägen, medan en kortare form som saknar den heparanbindande svansen (VEGF‑A121) var oförändrad. Fler VEGF‑A165‑molekyler bundet till cellytan efter RNA‑borttagning, trots att receptornivåerna var oförändrade. I tredimensionella mikrofluidiska enheter växte endotelceller exponerade för RNas längre in i kollagengeleer och bildade rörliknande strukturer mer robust, vilket indikerar att förstörelse av ytrna släpper loss pro‑angiogeniskt beteende.
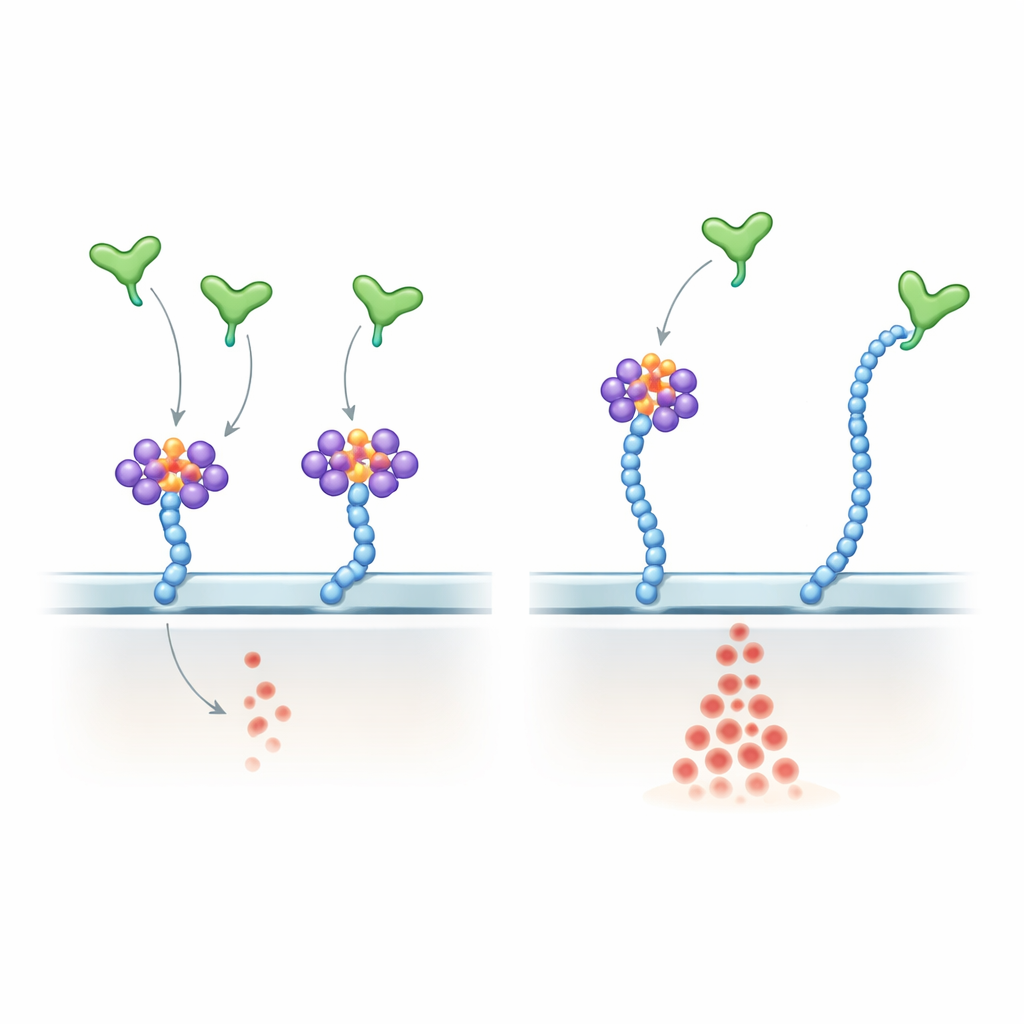
Dissekera hur VEGF‑A känner av RNA kontra socker
För att undersöka mekanismen visade författarna att VEGF‑A165 direkt binder utvalda små RNA, inklusive många kända glycoRNA, genom sin positivt laddade C‑terminala region—samma region som binder heparansulfat. De konstruerade en subtil version av VEGF‑A165 där viktiga argininrester i denna svans byttes ut mot lysiner. Denna mutant behöll sin övergripande positiva laddning och band fortfarande heparansulfatkedjor, men den bundet glycoRNA dåligt och blev i hög grad okänslig för RNas‑behandling. I endotelceller gav mutanten starkare och mer RNas‑resistent ERK‑aktivering än normal VEGF‑A165, vilket nära efterliknade effekten av att ta bort RNA från cellytan. I levande möss orsakade injektion av mutanten i ögat mer intensiv retinal kärltillväxt än den normala proteinet. I zebrafiskembryon störde överuttryck av den mutanta versionen av Vegfa normal kärlmönstring och ökade antalet endotelceller.
Från grundläggande mekanism till bredare implikationer
Slutligen visade författarna att sammansmältning av VEGF‑A:s heparanbindande svans med ett orelaterat signalprotein, Wnt3a, kunde omdirigera Wnt‑aktiviteten: att fästa den normala svansen minskade Wnt‑drivna utvecklingsförändringar, medan att fästa den RNA‑okänsliga svansen ökade dem. Tillsammans stödjer dessa experiment en modell där csRNP‑kluster, förankrade av specifikt sulfaterat heparansulfat, binder VEGF‑A och närbesläktade faktorer för att dämpa deras aktivitet. När RNA‑komponenten tas bort eller när tillväxtfaktorer förlorar förmågan att känna av RNA, tippar balansen mot starkare signalering och förändrad vaskulär utveckling i flera arter.
Varför detta är viktigt för hälsa och framtida terapier
För en icke‑specialist är huvudbudskapet att celler använder inte bara proteiner och socker, utan också små RNA visade på deras yta för att finjustera kraftfulla tillväxtsignaler som VEGF‑A. Dessa sockerförankrade RNA–protein‑kluster fungerar som justerbara bromsar på blodkärlsbildning och bidrar till att nya kärl gror där och när de behövs. Att rubba denna balans—genom att nedbryta ytrna eller förändra tillväxtfaktorers RNA‑bindande egenskaper—kan antingen överdriva eller felrikta kärltillväxt. Att förstå detta nyupptäckta kontrollager kan öppna dörren för terapier som mer precist kan justera angiogenes upp eller ner vid cancer, ögonsjukdomar, sårheling och regenerativ medicin genom att rikta in sig på ytrna, deras sockerstommar eller tillväxtfaktorernas RNA‑kännande regioner.
Citering: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Nyckelord: angiogenes, vasoendothelial tillväxtfaktor, heparansulfat, RNA på cellytan, glycoRNA