Clear Sky Science · sv
Utvecklingsmässig konvergens och divergens i mänskliga stamcellsmodeller av autism
Varför denna forskning är viktig för familjer och samhället
Autismspektrumstörning är känt för sin komplexitet: hundratals olika gener har kopplats till ökad risk, samtidigt som många personer med autism delar liknande svårigheter i kommunikation, social interaktion och beteende. Denna studie ställer en till synes enkel fråga med stora konsekvenser: när mycket olika genetiska förändringar ökar sannolikheten för autism, stör de då i slutändan den utvecklande människohjärnan på liknande sätt? Genom att använda små laboratorietillverkade modeller av människans cortex som är byggda av patienternas egna celler, följer forskarna hur tidiga fel i genaktivitet kan kanaliseras in i gemensamma vägar som förändrar hur hjärnceller föds, mognar och kopplas ihop.
Att odla miniatyrhjärnvävnad i laboratorium
För att angripa frågan samlade teamet in hud- eller blodceller från 55 personer: vissa hade välkarakteriserade sällsynta mutationer som starkt förknippas med autism, andra hade autism utan en känd större mutation, och ytterligare andra var opåverkade kontrollpersoner. Dessa celler omprogrammerades till inducerade pluripotenta stamceller, som kan bli nästan vilken celltyp som helst. Forskarna guidade dem sedan att bilda tredimensionella ”kortikala organoider” – små vävnadsbollar som efterliknar tidig utveckling av människans cerebrala cortex. Under 100 dagar utvecklades dessa organoider från mestadels stamliknande progenitorceller till nätverk rika på unga neuroner. Vid fyra tidpunkter längs denna tidslinje (dag 25, 50, 75 och 100) mätte teamet vilka gener som var påslagna eller avstängda i hundratals organoider och skapade en detaljerad film av molekylära förändringar under tidig hjärnutveckling.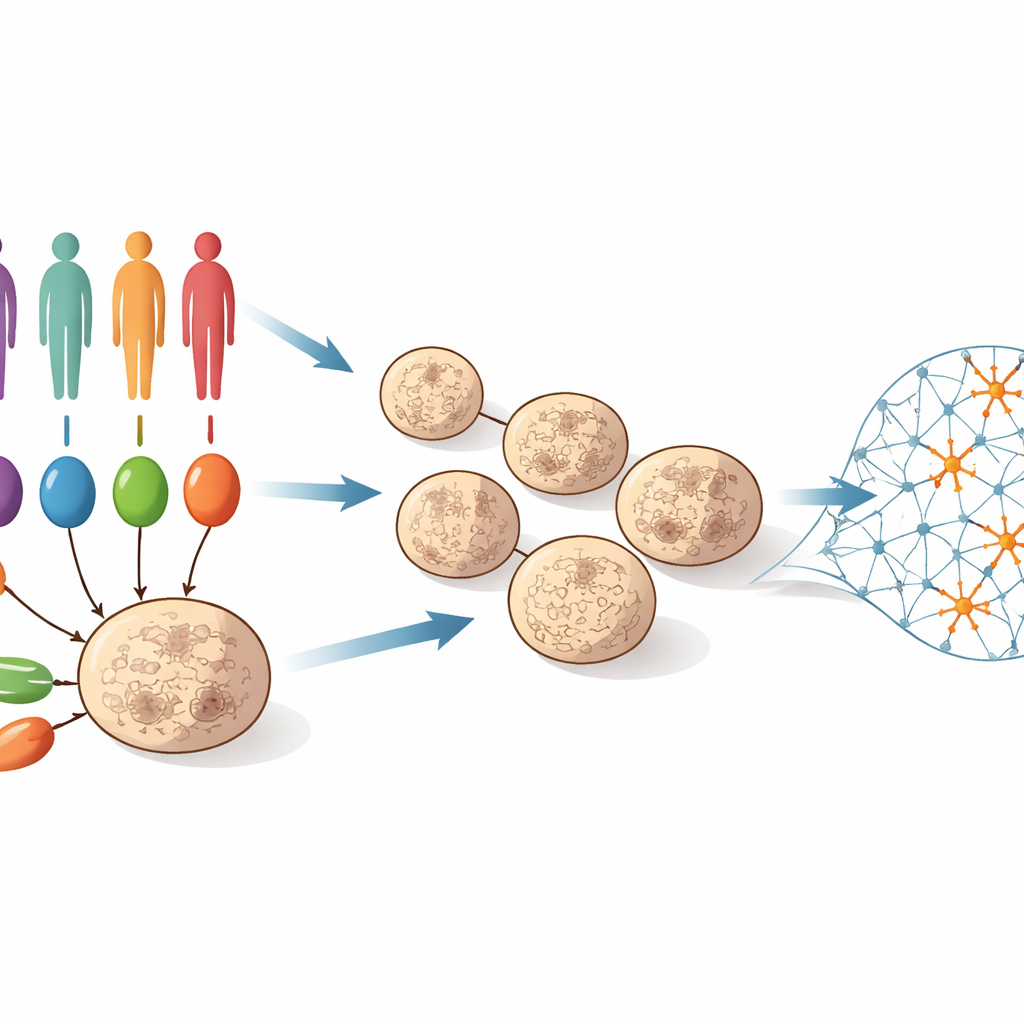
Många genetiska vägar, gemensamma tidiga avvikelser
Även om de autismkopplade mutationerna var mycket olika – inklusive stora bortfall eller dubbletter av DNA-segment och specifika genförändringar – visade organoider som bar samma mutation mycket reproducerbara mönster av genaktivitet. Tidigt i utvecklingen, särskilt runt dag 25, gav varje mutation sitt eget starka signaturmönster: hundratals till mer än tusen gener var felreglerade jämfört med kontroller. Ändå förändrade flera mutationer redan i detta tidiga skede överlappande uppsättningar av gener som är involverade i hur DNA paketeras och läses i cellerna. Dessa delade förändringar påverkade kända autismriskgener och andra gener kopplade till neurodevelopmentala störningar, vilket tyder på att olika mutationer börjar störa liknande cellulära maskinerier mycket tidigt i hjärnans bildning.
Konvergens när hjärnmodellen mognar
När organoiderna utvecklades mot mer mogna neuroner (vid dag 75 och 100) förändrades bilden. De mutationsspecifika skillnaderna blev mindre distinkta, medan likheterna blev starkare. I nära nog alla genetiska varianter av autism som studerades såg forskarna minskad aktivitet i gener viktiga för elektrisk signalering vid synapser – kommunikationspunkterna mellan neuroner – och ökad aktivitet i gener kopplade till celltillväxt och proteinproduktion. Subtila skift i proportionerna och mognadsstadierna av olika celltyper framträdde, vilket pekar på förändringar i tidpunkten för neuronbildning och mognad snarare än ett totalt bortfall av specifika celltyper. Vid den senaste tidpunkten visade tusentals gener ett gemensamt mönster av dysreglering över de olika sällsynta mutationerna, trots att mutationerna i sig påverkade olika ursprungliga gener.
En central kontrollhub som kopplar många autismgener
Vid en djupare analys använde teamet nätverksanalyser för att gruppera gener som tenderade att slå på och av tillsammans i ”moduler”. En modul i synnerhet, kallad M5, framträdde tydligt. Dess gener är mest aktiva tidigt i utvecklingen och är starkt berikade för autismriskgener, särskilt sådana som styr hur andra gener slås på eller av och hur DNA paketeras. I organoider från flera autismmutationsgrupper var denna modul konsekvent nedreglerad. Forskarna visade att många av proteinerna i M5 fysiskt interagerar och bildar en regulatorisk nav. Genom att använda CRISPR-baserade verktyg för selektivt dämpa 26 av dessa M5-regulatorer i mänskliga neurala progenitorceller bekräftade de att detta nav direkt kontrollerar stora uppsättningar av nedströmsgener, inklusive många ytterligare autism- och neurodevelopmental-riskgener, och att störning av det kan förändra vägar involverade i neuronbildning och synapsfunktion.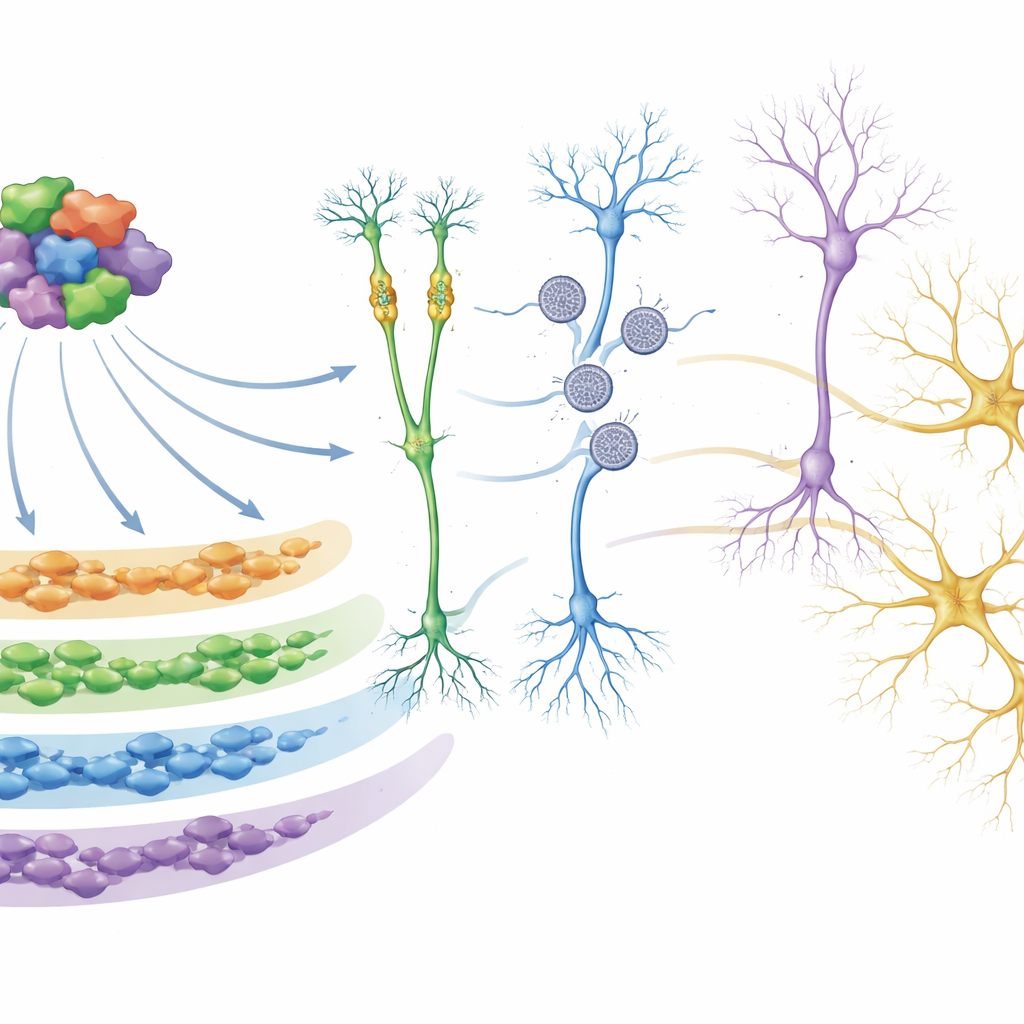
Vad detta betyder för förståelsen av autism
Detta arbete föreslår en enande bild: sällsynta, starkt verkande autismkopplade mutationer börjar med att störa olika delar av genomet, men deras effekter rör sig framåt genom ett delat tidigt kontrollnätverk som styr hur kortikala neuroner genereras och kopplas. Med tiden konvergerar dessa effekter till gemensamma utfall – försenad eller förändrad neuronal mognad och störda synaptiska program – även om de ursprungliga genetiska orsakerna skiljer sig åt. För familjer innebär detta att mycket olika diagnoser på DNA-nivå ändå kan påverka överlappande biologiska vägar i den utvecklande hjärnan. För forskare och kliniker erbjuder det identifierade regulatoriska nätverket ett fokuserat set av molekylära mål för framtida terapier som syftar till att återställa mer typiska mönster av hjärnutveckling över ett brett spektrum av autismrelaterade genetiska tillstånd.
Citering: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Nyckelord: autismspektrumstörning, hjärnorganoider, stamcellsmodeller, genreglering, neurodevelopment