Clear Sky Science · sv
Systematiska analyser av lipidmobilisering av humana lipidoverföringsproteiner
Hur celler håller ordning på sitt fett
Varje cell i din kropp är omsluten av fett‑rika membran, och tusentals olika fetter hjälper dessa membran att utföra allt från att skicka signaler till att driva energianvändning. Men dessa fetter är inte slumpmässigt utspridda: varje cellens inre kompartiment har sin egen speciella blandning. Den här studien ställer en enkel men långtgående fråga: hur förflyttar celler rätt fetter till rätt plats vid rätt tidpunkt, och vad händer när detta system inte fungerar?
Proteiner som skjutsar fetter
Celler förlitar sig på en stor familj molekyler som kallas lipidöverföringsproteiner, eller LTP:er, vilka kan plocka ut ett fettmolekyl från ett membran, dölja dess oljiga kropp i en skyddande ficka och leverera den till ett annat membran. Många humana LTP:er är kopplade till sjukdomar såsom cancer och neurologiska störningar, men för de flesta visste man inte vilka fetter de faktiskt transporterar. Författarna ville bygga en systematisk karta över vilka humana LTP:er som binder vilka lipider, och hur ökad aktivitet hos dessa LTP:er omformar hela uppsättningen fetter i en cell.
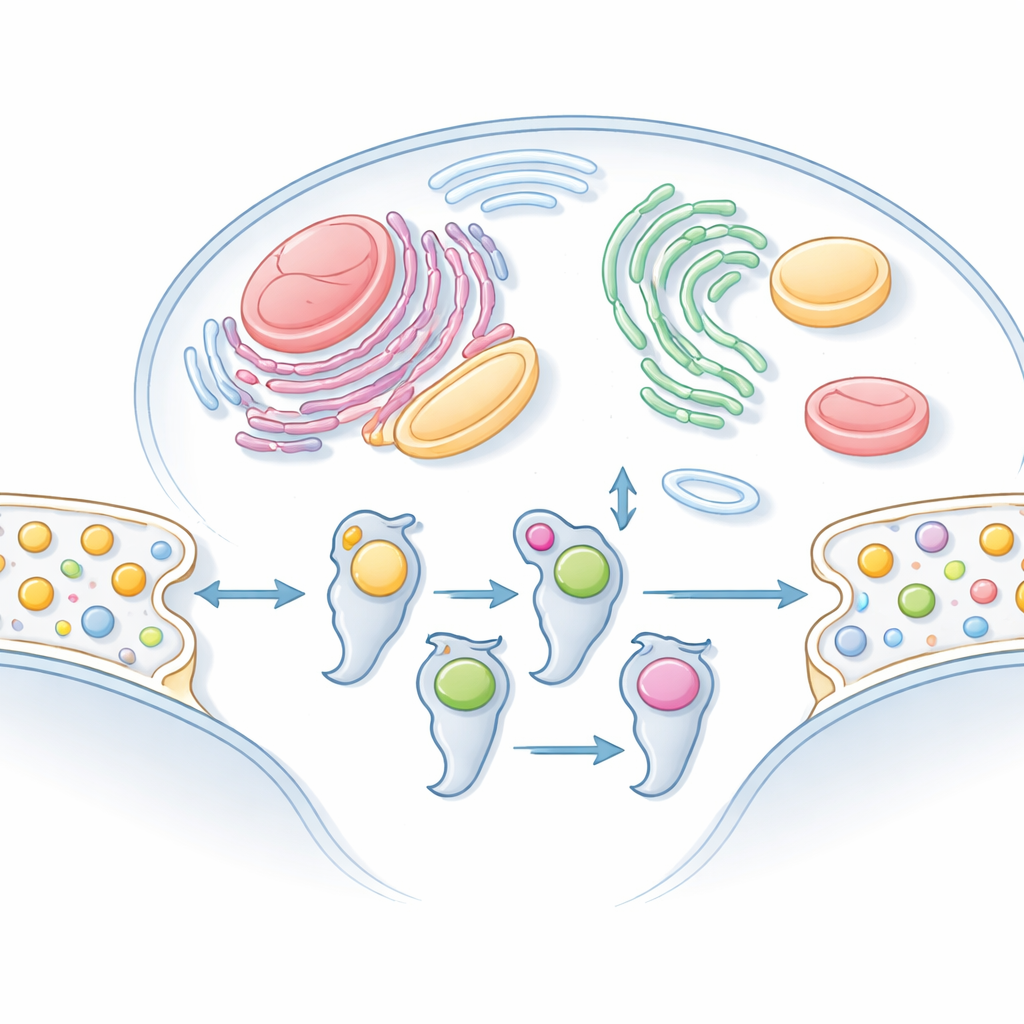
Att bygga en storskalig karta över lipidtransport
För att göra detta klonade teamet 101 humana LTP:er och uttryckte dem i två olika miljöer. I människoderiverade celler tillät de varje LTP att samla sig med de fetter som naturligt fanns närvarande. I ett provrörsexperiment blandade de renade LTP:er med artificiella membran gjorda av animaliska vävnadsextrakt. De renade sedan mer än 100 LTP–lipid‑komplex och identifierade de bundna fetterna med känslig masspektrometri. Genom att matcha protein‑ och lipid‑signaler över många separationssteg filtrerade de bort oavsiktliga medföljare och behöll endast lipider som konsekvent färdades med varje LTP. Resultatet blev ett katalog över LTP‑partners som täcker nio stora LTP‑familjer.
Nytt last och nya regler
Denna karta bekräftade kända partners—som vitamin A för dess bärarproteiner—men avslöjade också nya och ibland överraskande laster. En LTP kallad HSDL2, kopplad till rubbningar i fettlagring, visade sig mobilisera triacylglyceroler, de neutrala fetter som fyller våra fettceller. Andra LTP:er band signalmolekylära fetter som diacylglycerol, eller en särskild grupp ”eter”‑lipider som tillverkas via en distinkt väg. Många LTP:er visade sig hantera mer än en lipidklass, vilket antyder att de gör dubbel nytta: de kan flytta sin huvudsakliga last samtidigt som de hanterar hjälplipider som driver utbytesprocessen eller finjusterar metabolismen. När forskarna tvingade celler att överproducera individuella LTP:er förändrades nivåerna av både kända och nyligen upptäckta lipidpartners på förutsägbara sätt, vilket visar att de nykartlagda lasterna inte är laboratorieartefakter utan fungerar i levande celler.
Varför bara vissa fetter är rörliga
När de granskade hela datasetet noterade författarna att LTP:er inte behandlade alla varianter av en given lipid lika. De visade tydliga preferenser för fetter med kortare kedjor och med en eller två kemiska dubbelbindningar i dessa kedjor. Sådana fetter skapar små defekter i membranen som gör dem lättare att plocka ut, medan mycket styva eller starkt böjda kedjor är svårare att extrahera. Vissa LTP:er gick längre och föredrog extremt specifika kedjemönster. Till exempel föredrog ceramidtransportören CERT ceramider med vissa kedjelängder, inklusive sällsynta mycket långa arter som hjälper till att bilda tätt packade membranfläckar. En annan grupp, fosfatidylinositol‑överföringsproteinerna, favoriserade en art som bär en arakidonsyrakedja, en byggsten för många hormonlika signaler. Datorsimuleringar av LTP‑strukturer avslöjade hur kluster av särskilda aminosyror inne i bindningsfickorna skapar täta passformer för dessa utvalda kedjor.
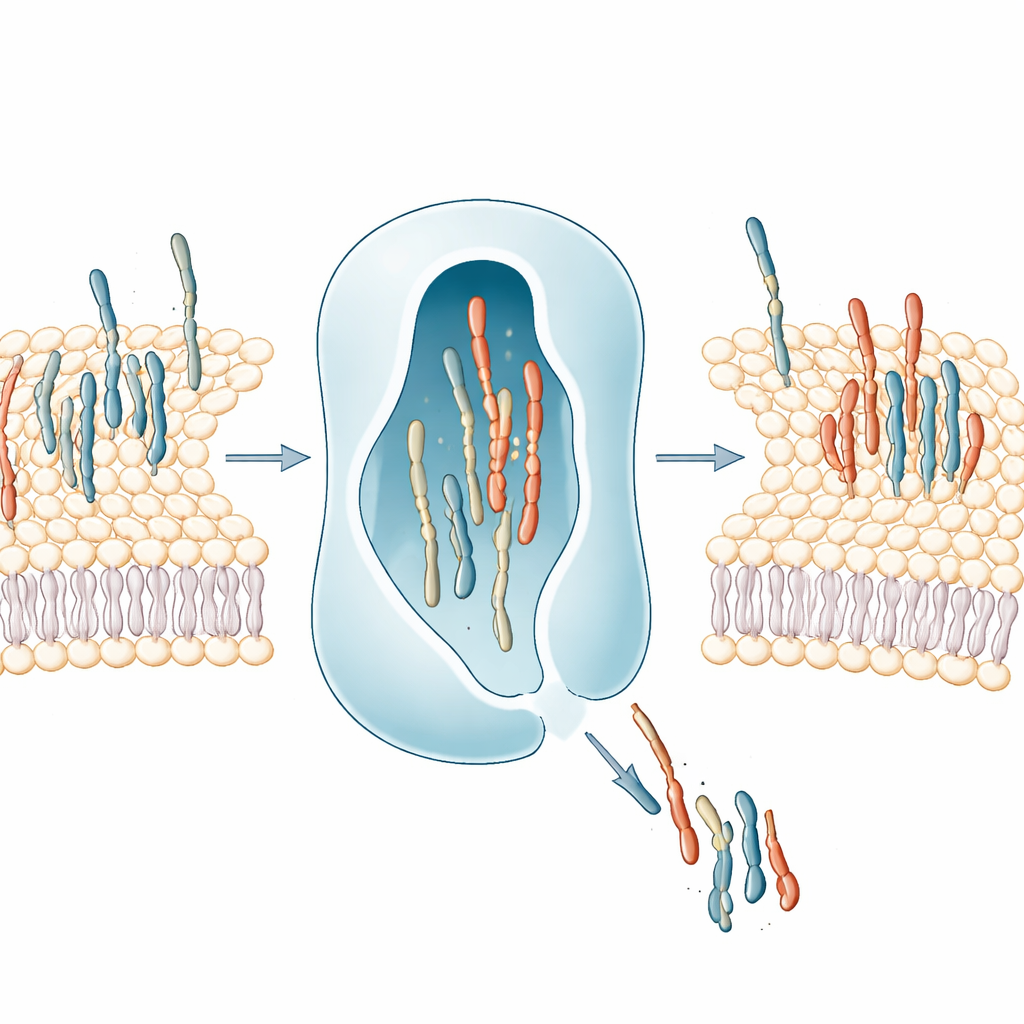
Kopplade lipider och samordnat cellbeteende
Studien undersökte också om olika lipider som bärs av samma LTP är relaterade i en cells liv. Genom att jämföra sin karta med stora befintliga dataset fann författarna att lipider som hanteras av samma LTP tenderar att stiga och falla tillsammans när metabolismen störs och tenderar att förekomma på samma platser i celler och vävnader. Detta tyder på att LTP:er hjälper till att samordna grupper av lipider som arbetar tillsammans, snarare än att flytta isolerade molekyler. Med andra ord kan varje LTP definiera ett litet ”nätverk” av fetter som färdas och verkar som en enhet.
Varför detta spelar roll för hälsa och sjukdom
För icke‑specialister är huvudbudskapet att celler inte bara tillverkar rätt fetter; de måste också förflytta noggrant utvalda fettarter till rätt membran, och de gör detta med ett förvånansvärt mångsidigt verktyg av överföringsproteiner. Detta arbete levererar den första breda, experimentellt grundade kartan över vilka humana LTP:er som bär vilka lipider, och avslöjar enkla regler—som en förkärlek för vissa kedjelängder och grader av omättnad—that avgör vilka medlemmar i den omfattande lipidpoolen som faktiskt är rörliga. Eftersom många LTP:er och deras lipidpartners är kopplade till cancer, immunsvar och hjärnfunktion, erbjuder denna resurs en utgångspunkt för att förstå hur subtila förändringar i fetttrafik kan få genomgripande effekter i sjukdom, och för att utforma framtida terapier som styr dessa mikroskopiska skyttar mot hälsosammare vägar.
Citering: Titeca, K., Chiapparino, A., Hennrich, M.L. et al. Systematic analyses of lipid mobilization by human lipid transfer proteins. Nature 651, 511–520 (2026). https://doi.org/10.1038/s41586-025-10040-y
Nyckelord: lipidöverföringsproteiner, cellmembran, lipidomik, membranmetabolism, ceramidtransport