Clear Sky Science · sv
Individualiserade mRNA‑vacciner framkallar varaktigt T‑cellsimmunitet som adjuvant vid TNBC
Ny hopp efter bröstcancerbehandling
För många kvinnor med en aggressiv form av bröstcancer som kallas trippelnegativ bröstcancer tar inte rädslan slut när cellgifterna och operationen är över. Denna cancer har hög risk för återkomst och spridning, ofta inom bara några år. Studien som beskrivs här prövar ett starkt individualiserat vaccin, byggt av varje patients egna tumörmutationer, för att undersöka om det kan lära immunsystemet att stå vakt i åratal och minska risken för återfall efter att standardbehandlingen avslutats.
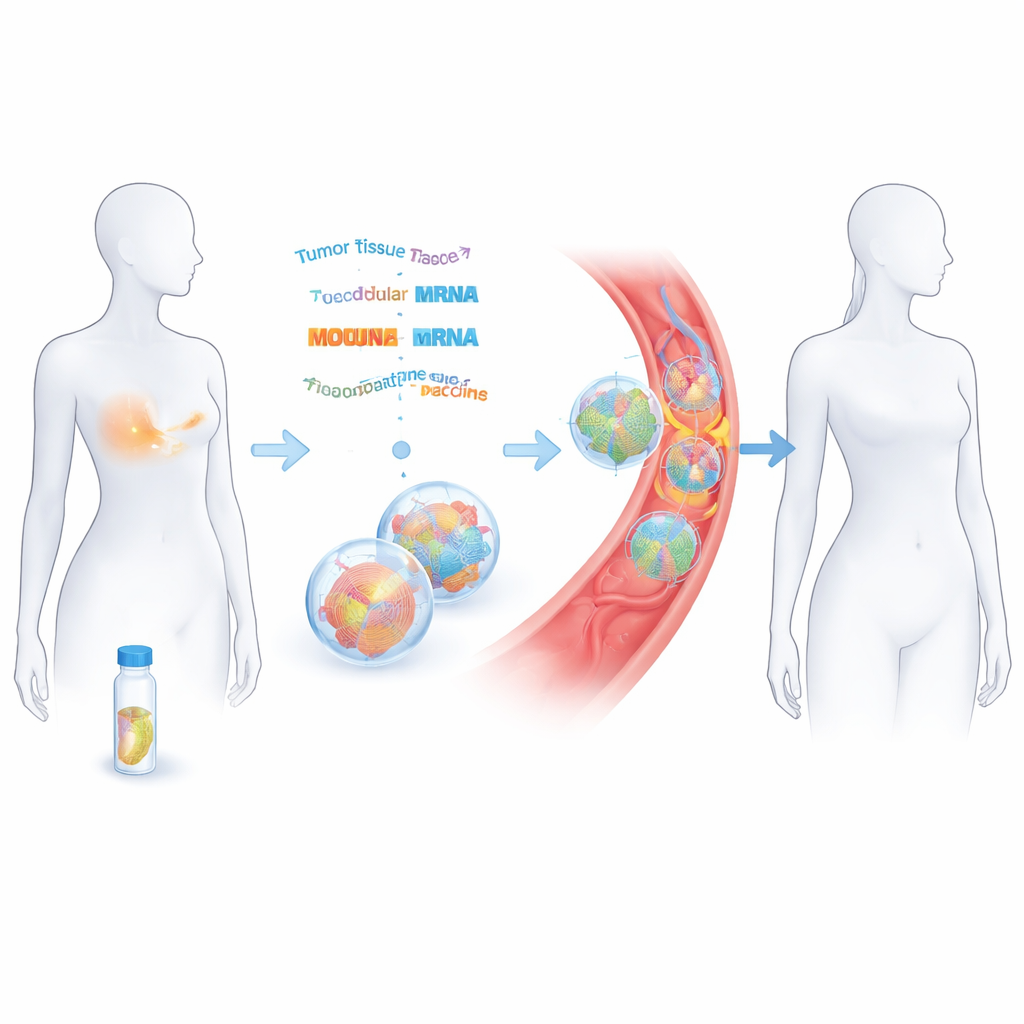
Att förvandla en borttagen tumör till ett skräddarsytt vaccin
Forskarna arbetade med 14 kvinnor som hade tidig stadium trippelnegativ bröstcancer och som redan hade genomgått operation och cytostatika i botande syfte. Från den borttagna tumörvävnaden läste de av DNA och RNA för att katalogisera cancerns unika mutationer. Med hjälp av datorverktyg förutsåg de vilka av dessa förändringar som kunde uppfattas som främmande av immunceller. Upp till 20 av dessa ”neoantigen” fogades sedan samman och kodades i två strängar budbärar‑RNA (mRNA), liknande principen bakom covid‑19‑vacciner men anpassade för varje patient. Dessa mRNA‑strängar förpackades i små fettdroppar och gavs intravenöst i åtta doser över ungefär två månader.
Hur vaccinet väcker immundefender
När mRNA kommer in i kroppen instruerar det immunsentineller kallade dendritiska celler att kortvarigt tillverka neoantigenproteinerna och visa fragment av dem på sin yta. Detta fungerar som en efterlyst‑affisch för T‑celler, immunsystemets primära cancerbekämpande kraft. Teamet tog blodprover före vaccination och vid flera tidpunkter efteråt för att testa om neoantigen‑specifika T‑celler dök upp och hur starka de var. Med känsliga laboratorieanalyser fann de att varje patient utvecklade nya eller förstärkta T‑cellsvar mot minst en av hennes valda mutationer, och de flesta svarade mot flera. I många fall utgjorde stora andelar av cirkulerande T‑celler — nivåer som vanligtvis ses endast vid kraftfulla cellterapier — nu celler som kände igen tumörspecifika mål.
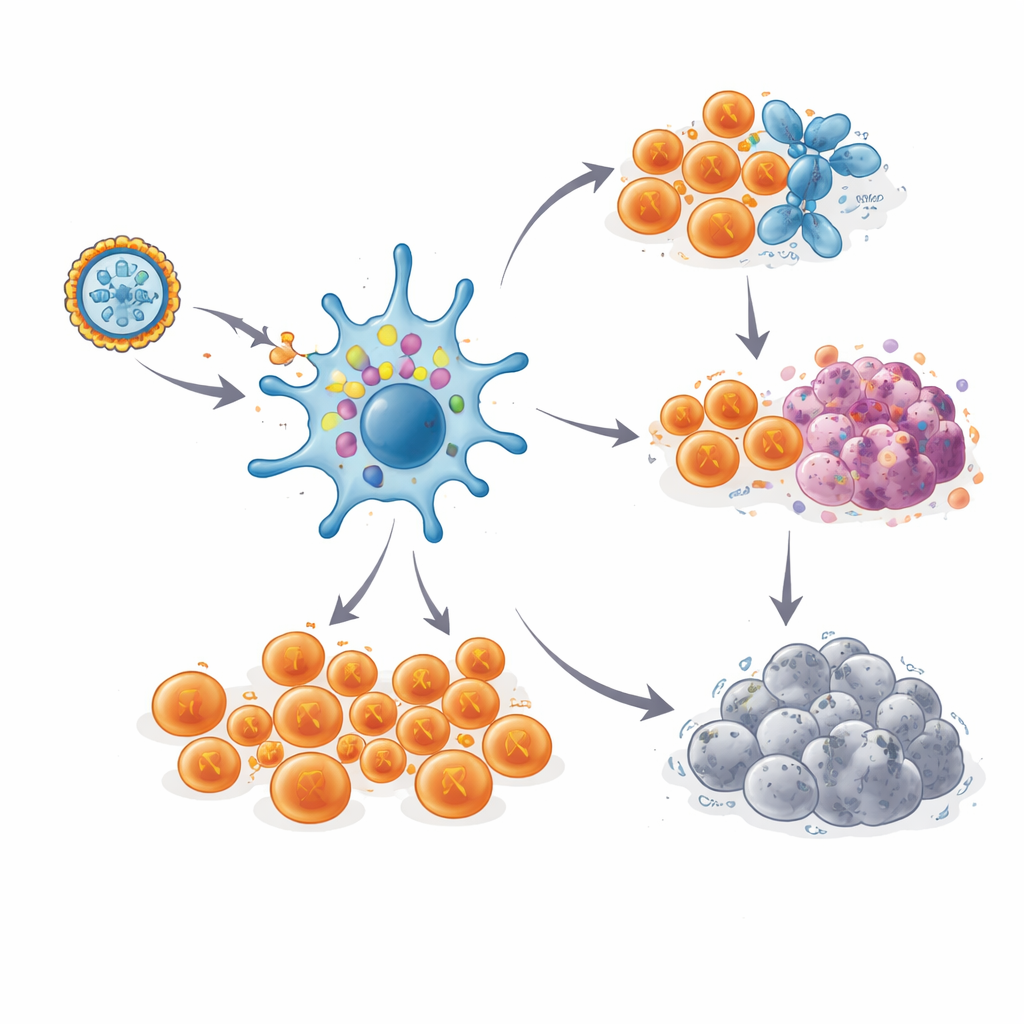
Långvarigt immunologiskt minne
Viktigt är att dessa T‑cellsvar inte avtog snabbt. Hos de flesta patienter nådde de starka svaren sin topp under vaccinationsperioden, sjönk något och bibehölls sedan på höga nivåer i ett till tre och ett halvt år, även utan uppföljningsdos. Genom att följa de unika receptor‑”streckkoderna” hos enskilda T‑cellskloner kunde forskarna spåra specifika neoantigen‑reaktiva celler i upp till sex år hos en patient som förblev fri från cancer. Detaljerade enkelcellsanalyser visade två huvudsakliga öden för dessa celler. Många blev högst beväpnade mördande T‑celler, redo att förstöra varje cell som bär rätt neoantigen. Andra utvecklades till en mer sällsynt, stamliknande minnespool med markörer för självförnyelse, vilket tyder på ett förråd som kan regenerera nya vågor av försvarare om cancerceller skulle dyka upp igen.
Vad som hände med patienterna
Efter en median uppföljning på strax över fem år från första vaccindosen hade elva av de fjorton kvinnorna inte upplevt återkomst av sin cancer; en av dessa avled av andra orsaker medan hon fortfarande var i remission. Tre kvinnor fick återfall, och deras fall ger ledtrådar till varför ett personligt vaccin ibland kan misslyckas. En patient utvecklade endast ett svagt T‑cellsvar och fick senare nytta av en annan immunterapi, en anti‑PD‑1‑antikropp, innan hon slutligen dog av utbredd sjukdom. En andra patient hade ärftlig risk och tumörer i båda brösten; endast en tumör användes för att designa vaccinet, och senare visade bevis att återfallet kom från den genetiskt skilda, ovaccinerade tumören. Den tredje patienten hade starka vaccine‑inducerade T‑celler som infiltrerade den återkommande tumören, men cancercellerna hade till stor del förlorat nyckelmolekyler som behövs för att visa neoantigen på ytan, och undvek därmed immunsystemets attack.
Varför detta arbete är viktigt för framtiden
Denna tidiga fas‑studie var liten och saknade en kontrollgrupp, så den kan inte bevisa att vaccinet ensamt förhindrade återfall. Den visar ändå att det är möjligt att bygga ett komplext, skräddarsytt mRNA‑vaccin från en patients egen tumör i vanliga sjukhusmiljöer, att det i allmänhet tolereras väl och att det kan utlösa kraftfulla, långlivade T‑cellsarméer mot flera tumörspecifika mål. Resultaten belyser också flyktvägar som tumörer kan använda, såsom att förlora sin antigenvisnings‑apparat eller att uppstå från otargeterade lesioner, vilket pekar mot kombinationer med andra immunterapier och mer omfattande tumörsekvensering. För patienter med trippelnegativ bröstcancer antyder detta arbete att ett skräddarsytt vaccin, givet efter standardbehandling, en dag skulle kunna hjälpa till att hålla sjukdomen borta genom att förvandla deras eget immunsystem till en varaktig, mycket specifik försvarslinje.
Citering: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Nyckelord: trippelnegativ bröstcancer, mRNA‑cancervacciner, neoantigenimmunterapi, T‑cellsimmunitet, tumöråterfall