Clear Sky Science · sv
Polyaminberoende metaboliskt skydd reglerar alternativ splejsning
Hur små molekyler hjälper celler att läsa sina gener
Inuti varje cell kan samma DNA‑manus läsas på många sätt, vilket gör att ett begränsat antal gener kan ge upphov till ett mycket stort utbud av proteiner. Denna flexibilitet bygger på en process som kallas alternativ splejsning, där RNA‑budskap redigeras innan de blir proteiner. I denna artikel visar forskarna att små, positivt laddade molekyler kallade polyaminer tyst styr detta redigeringssteg och fungerar som ett slags skyddande sköld som hjälper cellen att avgöra vilka RNA‑varianter som ska bildas. Eftersom alternativ splejsning är central vid cancer, hjärnfunktion och i stamceller, får upptäckten av detta dolda kontrollager omfattande konsekvenser för hälsa och sjukdom.
Små laddade hjälpämnen i varje cell
Polyaminer är små, flexibla molekyler med flera positiva laddningar. Cellen tillverkar dem från grundläggande näringsämnen, och de har länge varit kända som stöd för tillväxt och överlevnad, särskilt i snabbt delande celler som tumörer. Författarna frågade om polyaminer också fungerar som signaler, inte bara som bränsle. Genom att delvis blockera polyaminproduktionen i prostatacancerceller och i möss mätte de hur proteiner och RNA förändrades över tid. De fann att långt innan de totala polyaminnivåerna sjönk dramatiskt uppstod en stark våg av förändringar i proteinfosforylering — kemiska märken som slår på eller av proteinknappar — särskilt på komponenter i cellens RNA‑redigeringsmaskineri, spliceosomen.
Omkoppling av cellens RNA‑redigerare
Med fokus på RNA använde teamet djupsekvensering för att följa alternativ splejsning när polyaminsyntesen hämmdes. Hundratals RNA‑segment hoppades över eller inkluderades annorlunda, både i cancercellinjer, normala celltyper och i musvävnader. Dessa förändringar var inte bara en bieffekt av långsammare celldelning eller av en annan känd polyaminberoende process kallad hypusinering. Istället, när forskarna återförsåg cellerna med externa polyaminer, återgick många splejsningsskiften mot det normala. Både läkemedel och genetiska verktyg som sänkte polyaminer gav likartade splejsningsmönster, och att ytterligare minska polyaminer med en läkemedelskombination gjorde förändringarna ännu starkare, vilket bekräftar att effekten var tätt knuten till polyaminillgänglighet.
En dold måltavla: SF3‑splejsningsmodulen
För att lokalisera var i splejsningsmaskineriet polyaminer verkar jämförde författarna splejsningssignaturen som orsakades av polyaminminskning med en stor referenskarta genererad genom att individuellt stänga av mer än 300 kända splejsningsfaktorer. Den närmaste matchen pekade på en specifik del av spliceosomen kallad SF3‑subkomplexet, som hjälper till att känna igen viktiga signaler i RNA. Beräkningsmässig analys av offentliga protein–RNA‑bindningsdata stödde denna koppling: de RNA som påverkades i splejsning vid polyaminförlust var särskilt benägna att binda SF3‑proteiner. När teamet delvis inaktiverade SF3‑komponenter genetiskt eller med ett läkemedel, utplånades till stor del splejsningseffekterna av polyaminbrist, vilket visar att intakt SF3‑aktivitet krävs för denna nya regleringsväg. 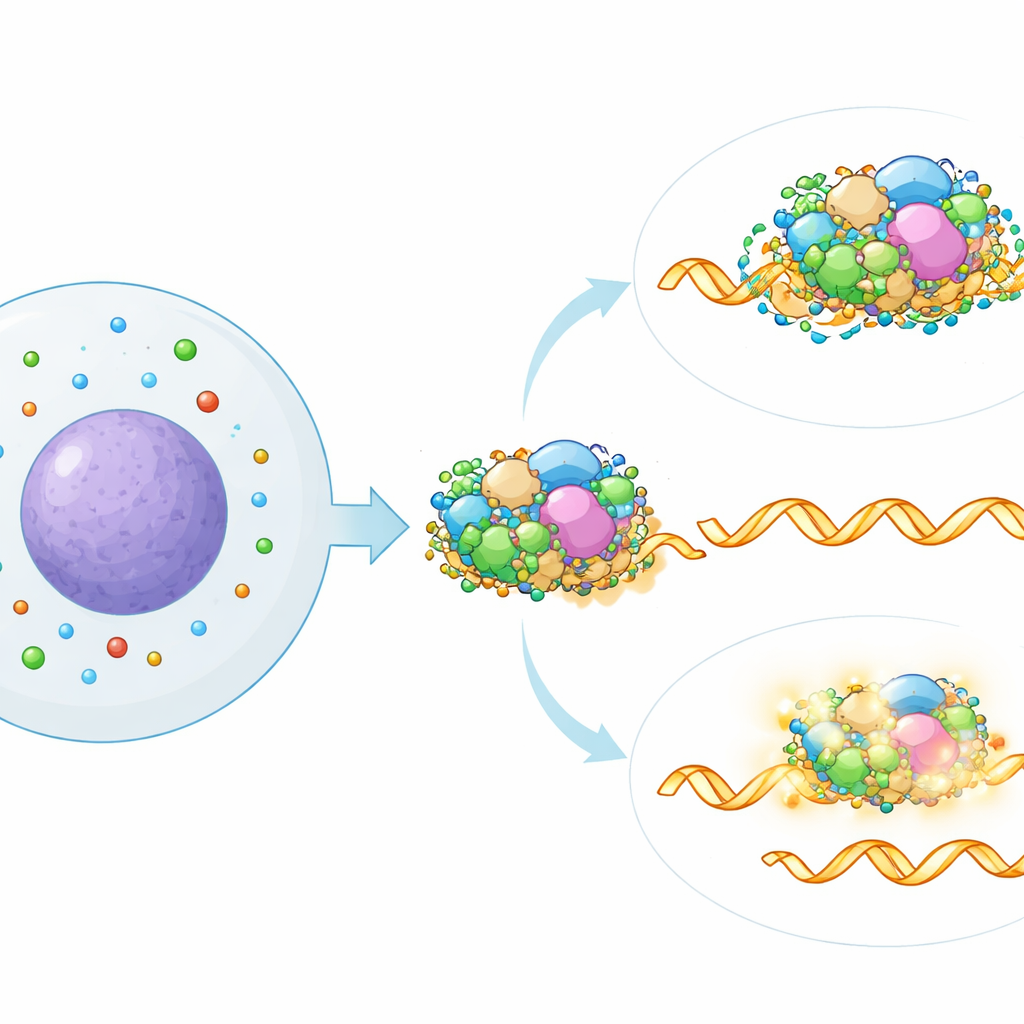
Metaboliskt skydd: hur polyaminer blockerar proteintaggning
Vid en närmare granskning noterade forskarna att de mest påverkade fosforyleringsställen på SF3‑proteinerna grupperade sig inom korta sekvenser rika på negativt laddade aminosyror. Molekylmodellering och kärnmagnetisk resonans visade att polyaminer lägger sig i dessa sura fickor, bildar flera elektrostatiska kontakter och delvis täcker närliggande serinrester där fosfatgrupper vanligtvis fästs. Denna fysiska ”omfamning” minskar tillgängligheten för proteinkinaser — de enzymer som sätter på fosfater. I provrörsexperiment blockerade tillsats av polyaminer direkt en kinas kallad CK1 från att fosforylera SF3‑proteiner. I celler dämpade hämning av CK1 och dess nära släkting CK2 de splejsningsförändringar som orsakades av polyaminförlust, och särskilt konstruerade möss vars SF3A3‑protein saknade tre viktiga fosforyleringsställen blev till stor del okänsliga för polyaminberoende splejsningsskift. 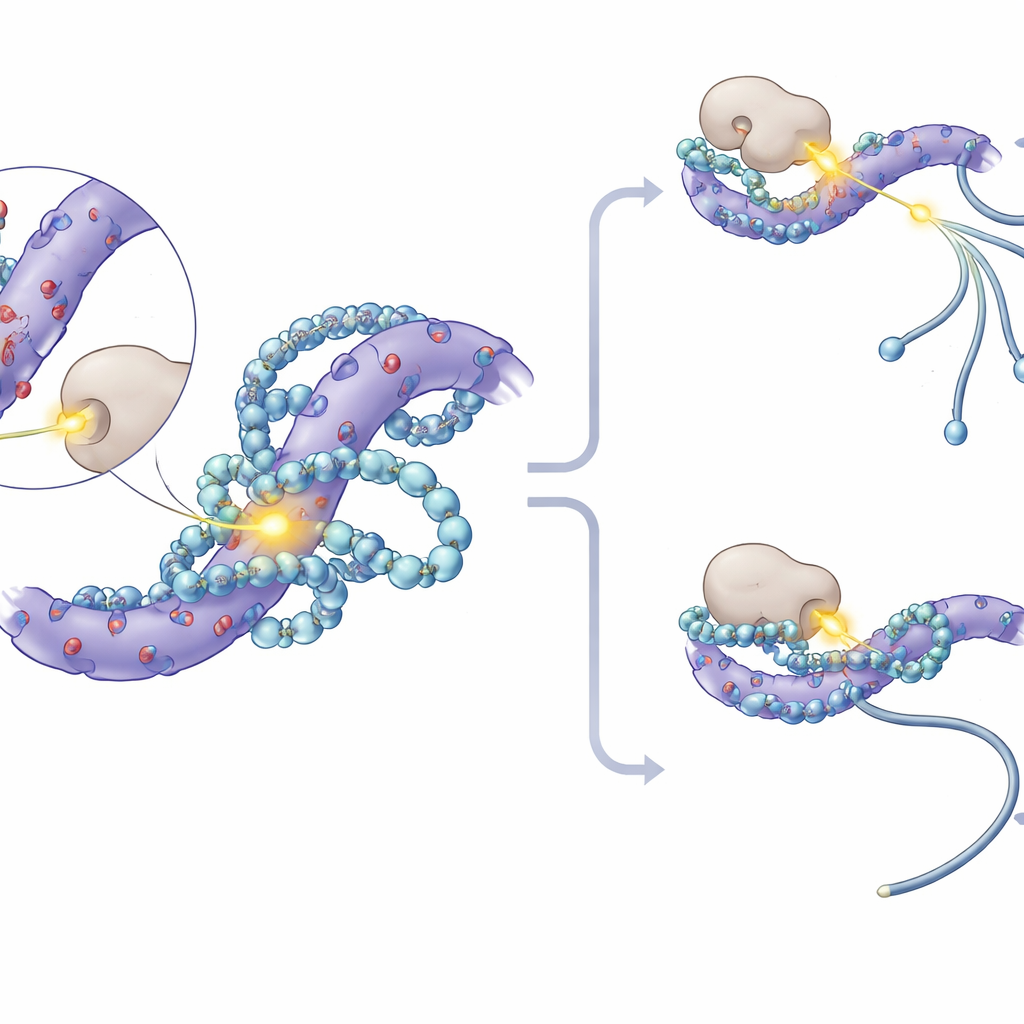
En designad molekyl som separerar funktioner
Studien introducerar också ett polyaminliknande läkemedel, BENSpm, som är mer starkt positivt laddat men samtidigt slår ner cellens egen polyaminproduktion. BENSpm band hårt till SF3:s sura fickor och blockerade kinasaktivitet, precis som naturliga polyaminer, men det räddade inte celltillväxt när riktiga polyaminer var knappa. Detta gjorde det möjligt för författarna att skilja klassiska polyaminfunktioner (stöd för tillväxt och metabolism) från den nyspecificerade skyddande rollen. I musens embryonala stamceller drev uttömning av polyaminer cellerna mot att förlora sin ”stemness”-markör Nanog och förändrade deras splejsningslandskap. BENSpm återställde både splejsningsprofilen och Nanog‑uttrycket trots fortsatt hämning av normal polyaminsyntes, vilket indikerar att metaboliskt skydd är ett avgörande krav för att bevara stamcellsidentitet.
Varför denna upptäckt är viktig
Enkelt uttryckt visar detta arbete att polyaminer fungerar som små skyddshandskar runt känsliga delar av nyckelproteiner i splejsmaskineriet. När handskarna är på kan kinaser inte lätt nå och märka dessa ställen, och cellens RNA‑redigering håller kursen. När polyaminer är låga tas handskarna av, fosforylering ökar och splejsningsmönster skiftar, med konsekvenser för både cancerceller och stamceller. Genom att definiera denna ”metaboliska sköldnings”-mekanism och tillhandahålla ett verktygsmolekyl som selektivt efterliknar den, öppnar studien dörren för nya sätt att finjustera genläsning utan att ändra DNA:t självt, och kan inspirera framtida terapier som riktar in sig på splejsning inom cancer och regenerativ medicin.
Citering: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Nyckelord: polyaminer, alternativ splejsning, RNA‑bearbetning, metabolisk signalering, reglering av stamceller