Clear Sky Science · sv
Vanlig variation i meiosgener formar mänsklig rekombination och aneuploidi
Varför kromosomfel i embryon spelar roll
Många graviditeter slutar innan de ens upptäcks, ofta därför att embryot har fel antal kromosomer. Denna studie ställer en förvillande enkel fråga med djupa konsekvenser för fertilitet och reproduktiv hälsa: hur påverkar vanliga DNA‑skillnader mellan människor sättet som ägg‑ och spermieceller blandar och delar kromosomer, och hur påverkar det i sin tur chansen att ett embryo får för många eller för få kromosomer? Genom att granska mer än hundratusen IVF‑embryon avslöjar författarna hur vanlig genetisk variation i ett fåtal gener subtilt kan vinkla oddsen åt ena eller andra hållet vad gäller dessa kromosomfel.
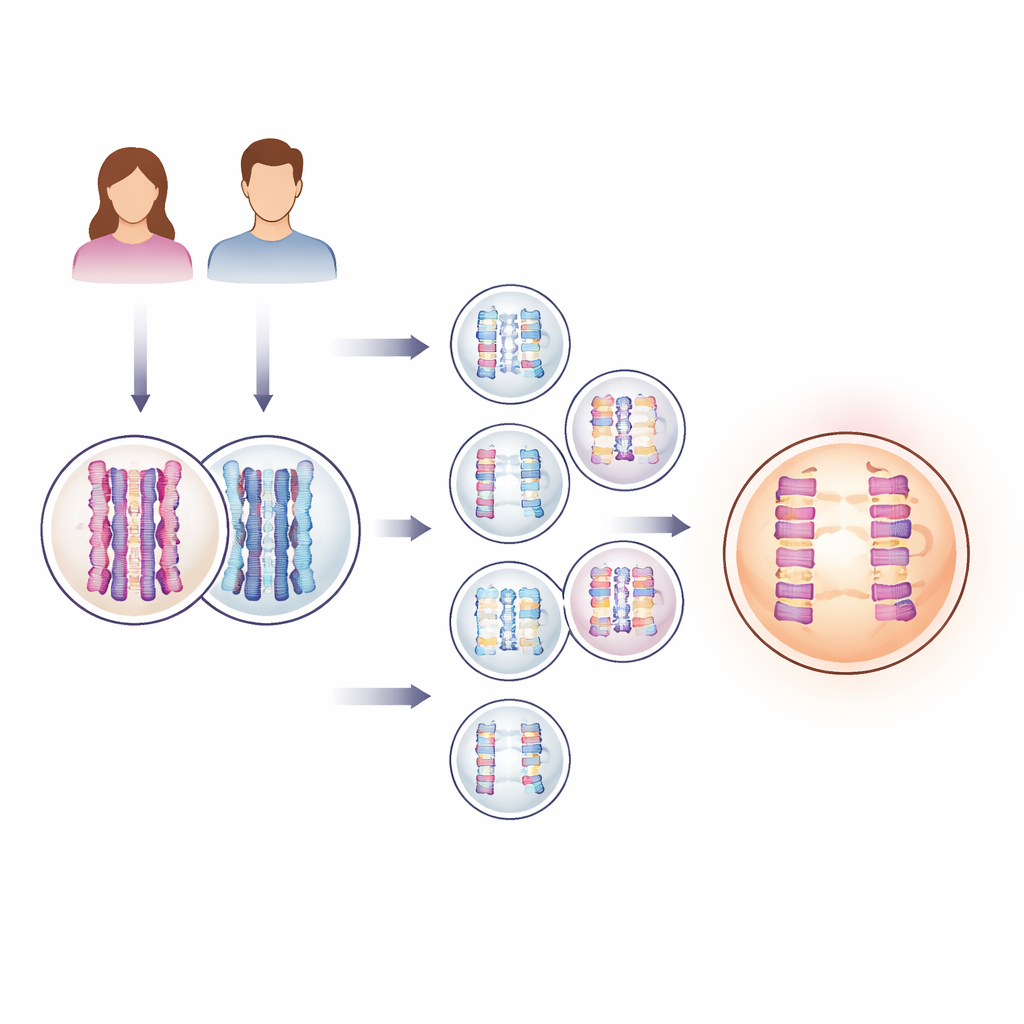
Inblick i tusentals IVF‑embryon
För att ta sig an ett problem som oftast utvecklas osynligt inne i människokroppen vände sig forskarna till genetiska testdata som rutinmässigt samlas in vid IVF. Kliniker tar ofta en biopsi från några celler i ett embryo några dagar efter befruktningen för att kontrollera kromosomproblem före överföring. Här analyserade teamet DNA från 139 416 sådana embryon, tillsammans med DNA från nästan 23 000 par biologiska föräldrar. Med en statistisk metod som följer block av föräldra‑DNA när de förs vidare till embryon kunde de både räkna ”crossovers” — punkterna där föräldrarnas kromosomer byter segment — och upptäcka när ett embryo hade vunnit eller förlorat en hel kromosom, ett tillstånd som kallas aneuploidi.
Hur vanliga är kromosomfel och vad påverkar dem?
Undersökningen visade att nästan 30 % av embryona bar på minst en aneuploid kromosom. De flesta av dessa fel härrörde från modern snarare än från fadern och involverade ofta specifika kromosomer som redan är kända för att vara problembenägna. Som väntat utifrån klinisk erfarenhet steg andelen embryon med maternella kromosomfel brant med moderns ålder, medan faderns ålder hade liten effekt. Avgörande var att när teamet jämförde embryon med normala kromosomantal med dem som hade fel, fann de att de felbenägna embryona tenderade att ha färre crossovers på sina i övrigt normala kromosomer. Detta stöder idén att crossovers har dubbel funktion: de skapar nya genetiska kombinationer, men fungerar också som fysiska förbindelser som hjälper kromosomer att separera ordentligt under äggbildning.
Vardagliga genetiska skillnader i viktiga gener spelar roll
Författarna sökte sedan i mödrarnas genom efter vanliga DNA‑varianter som korrelerade med hur ofta deras embryon var aneuploida. Ett utmärkande område låg nära en gen som heter SMC1B, som utgör en del av ett ringformat proteinkomplex som håller systerkromosomer ihop i ägg. Kvinnor som bar en viss version av denna DNA‑sekvens hade en något högre andel embryon med maternella kromosomfel, och denna risk ökade med åldern. Uppföljande analyser i stora genuttrycksdatamängder visade att den riskfyllda versionen av DNA‑sekvensen är kopplad till lägre aktivitet av SMC1B, tydligen genom subtila förändringar i hur en transkriptionsfaktor binder till dess promotor. Med andra ord kan en vanlig, icke‑störande justering av en regulatorisk brytare sänka nivån av ett kohesionsprotein tillräckligt mycket för att mätbart öka risken för felaktig kromosomsegregering.
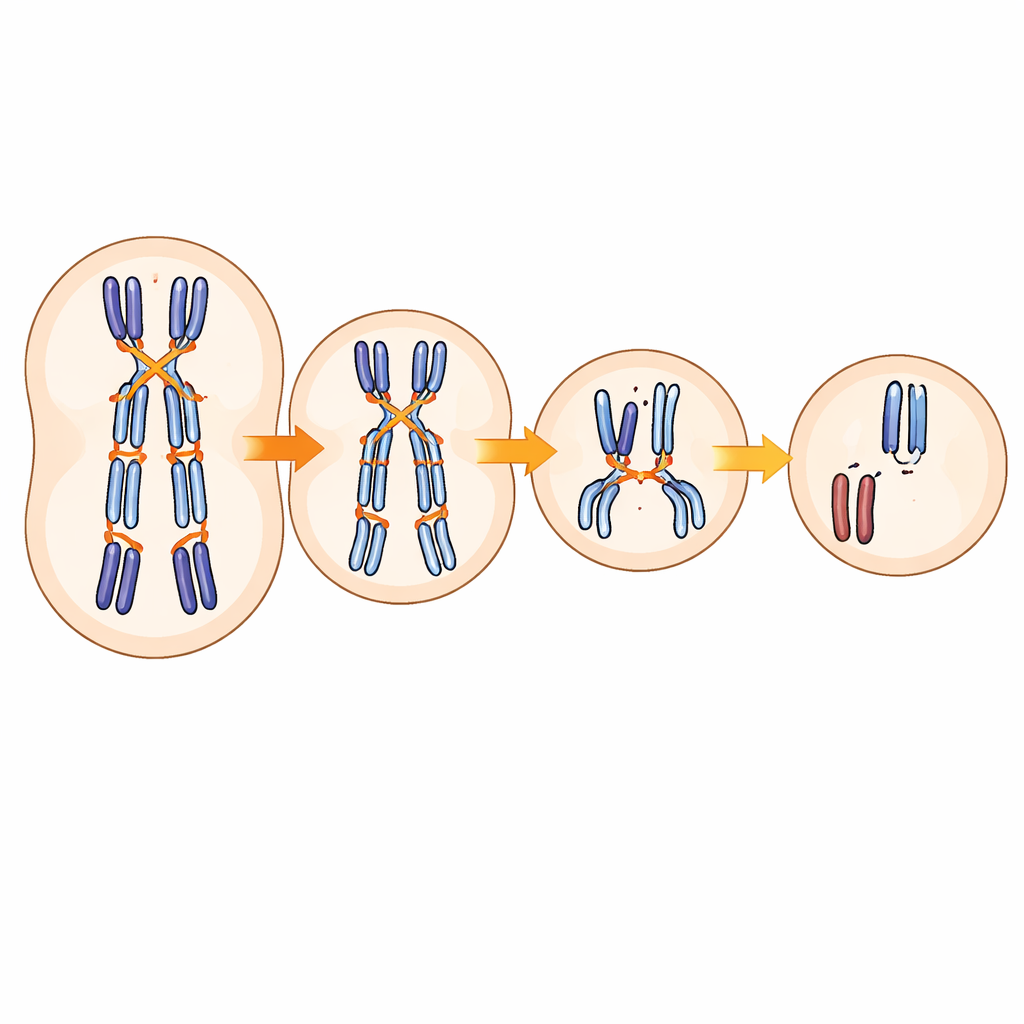
En gemensam genetisk tråd över fertilitetsdrag
Förutom SMC1B framhävde studien andra gener som hjälper till att alignera och koppla ihop kromosomer under meiosen, inklusive komponenter i det skelett som för ihop parade kromosomer och enzymer som markerar var crossovers kommer att ske. Varianter i dessa gener påverkade inte bara rekombinationsmönster och aneuploidirisken i embryon, utan visade även samband med tidpunkten för pubertet och klimakterium i stora populationsstudier. Samtidigt förklarade vanliga varianter sammantaget bara en liten del av den totala variationen i kromosomfel i embryon. Det tyder på att miljö, slumpmässiga händelser under äggutvecklingen och mer sällsynta genetiska förändringar sannolikt spelar stora roller, även om många av dessa påverkansfaktorer konvergerar mot samma molekylära maskineri.
Vad detta betyder för mänsklig fertilitet och evolution
För icke‑specialister är huvudbudskapet att samma genetiska processer som skapar hälsosam mångfald i vårt DNA också kan, när de finjusteras på olika sätt, öka risken för tidigt graviditetsbortfall. Detta arbete visar att vanliga ärftliga skillnader i ett fåtal meiosgener kan förskjuta balansen något, särskilt med stigande kvinnlig ålder, men ingen enskild variant avgör någons reproduktiva öde. Genom att kombinera massiva embryodatamängder med populationsgenetik tar studien också itu med ett evolutionärt pussel: varför varianter som ökar risken för icke‑viabla embryon kan förbli vanliga hos människor. Författarna menar att eftersom många sociala och miljömässiga faktorer suddar ut sambandet mellan embryonummer och faktisk familjestorlek, kan naturligt urval ha svårt att effektivt rensa bort sådana varianter. Tillsammans fördjupar dessa insikter vår förståelse för varför kromosomfel är så vanliga i mänsklig reproduktion och pekar mot biologiska vägar som i framtiden kan informera rådgivning eller interventioner.
Citering: Carioscia, S.A., Biddanda, A., Starostik, M.R. et al. Common variation in meiosis genes shapes human recombination and aneuploidy. Nature 651, 146–153 (2026). https://doi.org/10.1038/s41586-025-09964-2
Nyckelord: aneuploidi, meios, mänsklig fertilitet, kromosomrekombination, SMC1B