Clear Sky Science · sv
Ligand‑specifika aktiveringsbanor styr GPCR‑signalering i celler
Hur en receptor kan uppträda som många strömbrytare
Många av dagens läkemedel verkar på en stor familj av cellmembranproteiner som kallas G‑protein‑kopplade receptorer, eller GPCR:er. Dessa receptorer påverkar hjärtfrekvens, humör, andning och otaliga andra kroppsfunktioner. I årtionden behandlades de som enkla av/på‑brytare: ett läkemedel binder, brytaren växlas och en signal skickas in i cellen. Denna artikel visar att verkligheten är långt mer nyanserad. Med en ny sorts fluorescerande ”spion” inbyggd direkt i receptorn iakttar författarna i levande celler hur olika läkemedel för samma receptor längs distinkta aktiveringsvägar — som att välja olika rutter genom en stad — och framkallar olika signalmönster. Att förstå dessa dolda vägar kan hjälpa till att utforma läkemedel som ger önskad nytta samtidigt som biverkningar undviks.
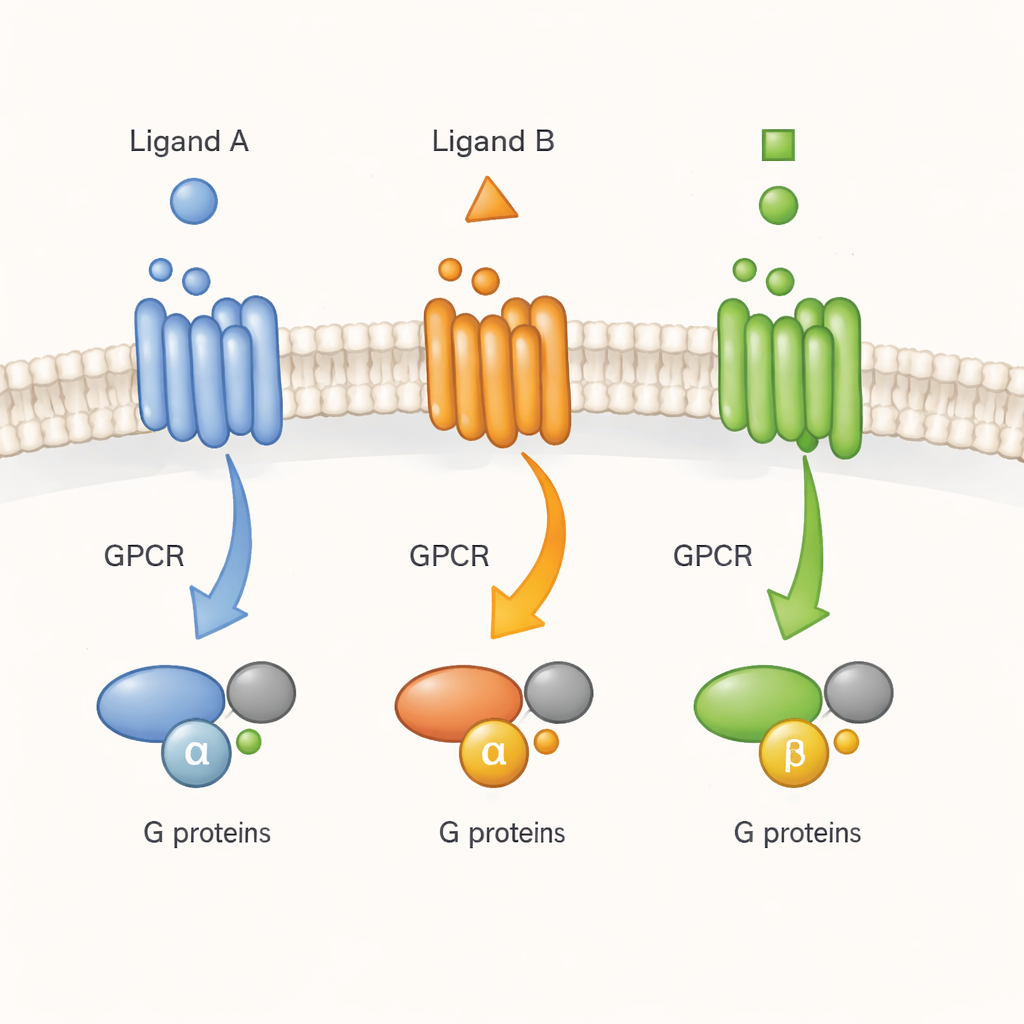
Att övervaka en cells dörrklocka i realtid
GPCR:er beskrivs ofta som molekylära dörrklockor: ett signalmolekyl (en ligand) ringer utifrån och receptorn förmedlar budskapet till G‑proteiner på insidan. Tidigare arbete med renade receptorer i detergenter hade föreslagit att GPCR:er inte bara växlar mellan en inaktiv och en aktiv form. Istället provar de många former som läkemedel kan stabilisera i olika grad. Men det var oklart om samma komplexitet finns i den trånga, dynamiska miljön i en levande cell. Här fokuserar författarna på en representativ receptor, M2 muskarinacetylkolinreceptorn, en viktig reglerare av hjärt‑ och nervaktivitet, och frågar om olika ligander driver den in i distinkta aktiva former som är betydelsefulla för verklig cellulär signalering.
Bygga små ljusrapporterare på receptor‑ytan
För att följa receptorernas rörelser utan att störa deras normala funktion använde gruppen genetisk kodexpansion, en teknik som låter dem infoga en specialdesignad aminosyra på valda positioner på receptorernas yttre yta. Detta kemiska ”ankare” kan kopplas till ett litet fluorescerande färgämne i levande celler. Genom att skanna 72 positioner och behålla endast sådana som fortfarande uppträdde som normala receptorer byggde de en panel av sju M2‑receptorvarianter, var och en försedd med ett enda färgämne vid en annan yttre slinga. När den naturliga budbäraren acetylkolin applicerades steg eller sjönk färgens intensitet vid dessa platser på karaktäristiska sätt och avslöjade hur varje del av receptorens yttre yta försköts när signaleringen började. Avgörande var att dessa märkta receptorer fortfarande kunde aktivera G‑proteiner och genomgå normal internalisering, vilket visar att biosensorerna var trogna snarare än störande.
Läkemedel lämnar distinkta ”konformationella fingeravtryck”
Forskarna jämförde sedan flera läkemedel som alla aktiverar M2‑receptorn men med olika styrka: kroppens egen acetylkolin, en mycket stark syntetisk agonist kallad iperoxo, och två svagare partiella agonister, arekolin och pilokarpin. Varje läkemedel gav ett unikt mönster av fluorescensförändringar över de sju rapportörsplatserna — ett konformationellt fingeravtryck. Vid de flesta positioner följde rörelsens storlek hur starkt läkemedlet aktiverade receptorn. Vid två platser var relationen dock inverterad: de svagare läkemedlen gav de största förändringarna, medan det starkaste läkemedlet gav nästan inga. Ett sådant beteende kan inte förklaras av ett enda aktivt tillstånd. Istället indikerar det att samma receptor i levande celler kan anta flera distinkta aktiva former, vissa föredragna av starka läkemedel, andra av svaga.
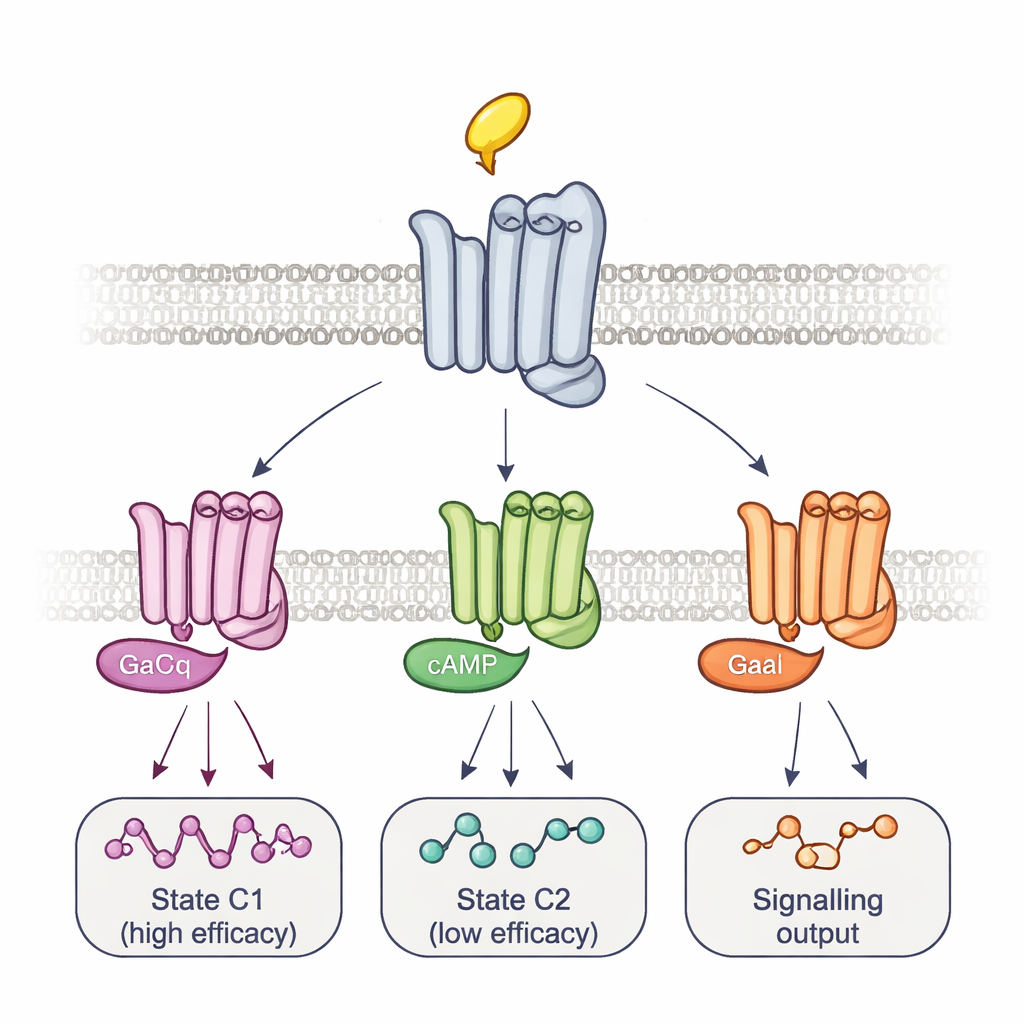
Flera komplex och tidsbestämda vägar till signalering
För att koppla dessa former till faktisk signalering förändrade teamet själva G‑proteinerna. Genom att överuttrycka ett mutant G‑protein som bildar mycket täta, långlivade komplex med receptorer raderades selektivt signalen från vissa rapportörsplatser samtidigt som andra förstärktes. Detta mönster, tillsammans med tidpunkten för fluorescensförändringarna, avslöjade minst två huvudtyper av receptor–G‑protein‑komplex: ett snabbbildande, hög‑effektivt komplex och ett långsammare, låg‑effektivt. Olika läkemedel försköt balansen mellan dessa komplex och använde till och med olika intermediära steg för att nå dit, vilket spårade läkmedelsspecifika aktiveringsbanor. Med en separat bioluminescens‑analys som övervakar en panel av 14 G‑protein‑subtyper visade författarna att dessa jämvikter hjälper bestämma inte bara hur starkt ett läkemedel aktiverar signalering i stort, utan också vilka exakta G‑proteiner som slås på. Till exempel aktiverade arekolin föredraget vissa Go‑proteiner, medan pilokarpin starkt gynnade det låg‑effektiva komplexet.
Varför detta spelar roll för bättre läkemedel
För icke‑specialister är huvudbudskapet att en enskild receptor inte bara är en enda strömbrytare utan en samling närbesläktade brytare, var och en nåbar via olika vägar och kopplad till något olika nedströms effekter. Denna studie ger en direkt bild av dessa vägar och tillstånd i intakta celler, snarare än i förenklade provrörssystem. Genom att kartlägga hur specifika läkemedel snedvrider receptorn mot särskilda komplex och G‑protein‑partner får forskare en ritning för att designa ”smartare” läkemedel — föreningar som puffar receptorer i tillstånd som driver hjälpsamma signaler samtidigt som de undviker de som kopplats till biverkningar. Den fluorescerande biosensorstrategin som utvecklats här bör kunna anpassas till många andra receptorer och öppnar ett fönster mot läkemedelsverkans realtidskoreografi i levande celler.
Citering: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Nyckelord: GPCR‑signalering, ligand‑effektivitet, G‑proteiner, konformationsbiosensorer, läkemedelsforskning