Clear Sky Science · sv
Upplösning av DNA-origamis strukturella integritet och farmakokinetik in vivo
Att iaktta små DNA-maskiner inne i kroppen
DNA kan vikas som papper till små tredimensionella former, en teknik som kallas DNA-origami. Dessa nanostrukturer kan programmeras att bära läkemedel, vacciner eller signalmolekyler med utomordentlig precision. Men när de injiceras i kroppen, förblir de intakta tillräckligt länge för att fungera, eller faller de snabbt sönder? Denna artikel presenterar ett nytt sätt att iaktta dessa DNA-maskiner i aktion i levande djur, och avslöjar hur länge de överlever, hur de färdas genom blodomloppet och till och med vilka delar av varje struktur som bryts först.
Varför vikning av DNA kan förändra medicinen
DNA-origami utnyttjar samma basparningsregler som lagrar vår genetiska information, men använder dem för att bygga objekt i nanostorlek. Forskare kan arrangera proteiner, läkemedel eller immunstimulerande signaler på dessa objekt som knoppar på en Lego-platta och skapa mycket kontrollerade terapier för cancer, autoimmuna sjukdomar och infektioner. För att sådana precisa behandlingar ska vara säkra och effektiva måste myndigheter och forskare veta hur intakta dessa strukturer förblir i kroppen och hur snabbt de avlägsnas—tillsammans känt som deras farmakokinetik. Befintliga spårningsmetoder fäster vanligtvis fluorescerande färgämnen eller räknar helt enkelt DNA-fragment, vilket kan få sönderdelat skräp att se ut som fullt intakta nanostrukturer. Fram till nu har det inte funnits något praktiskt sätt att avgöra, i levande djur, om de ursprungliga DNA-origami-formerna fortfarande är hela.
Ett molekylärt ”integritetstest” för DNA-origami
Teamet utvecklade en metod de kallar PLASTIQ, en förkortning av proximity ligation assay for structural tracking and integrity quantification. Huvudidén är att låta DNA-origamin rapportera om sitt eget tillstånd. På specifika positioner i varje struktur placerar forskarna par av korta DNA-staplar som sitter axel mot axel längs en helix när origamin är korrekt vikt. En av varje par bär en liten kemisk tagg som gör att de enzymatiskt kan förenas, eller ligeras, men endast om de fortfarande hålls nära varandra av en intakt scaffold-sträng. Om strukturen smälter, går sönder eller blir uppäten av enzymer, glider dessa två bitar isär och kan inte längre ligeras. Efter ligering amplifieras de förenade paren med standard polymeraskedjereaktion och kvantifieras med känslig qPCR eller sekvensering, vilket omvandlar närvaron av intakta lokala segment till mätbara signaler från endast några mikroliter blod.
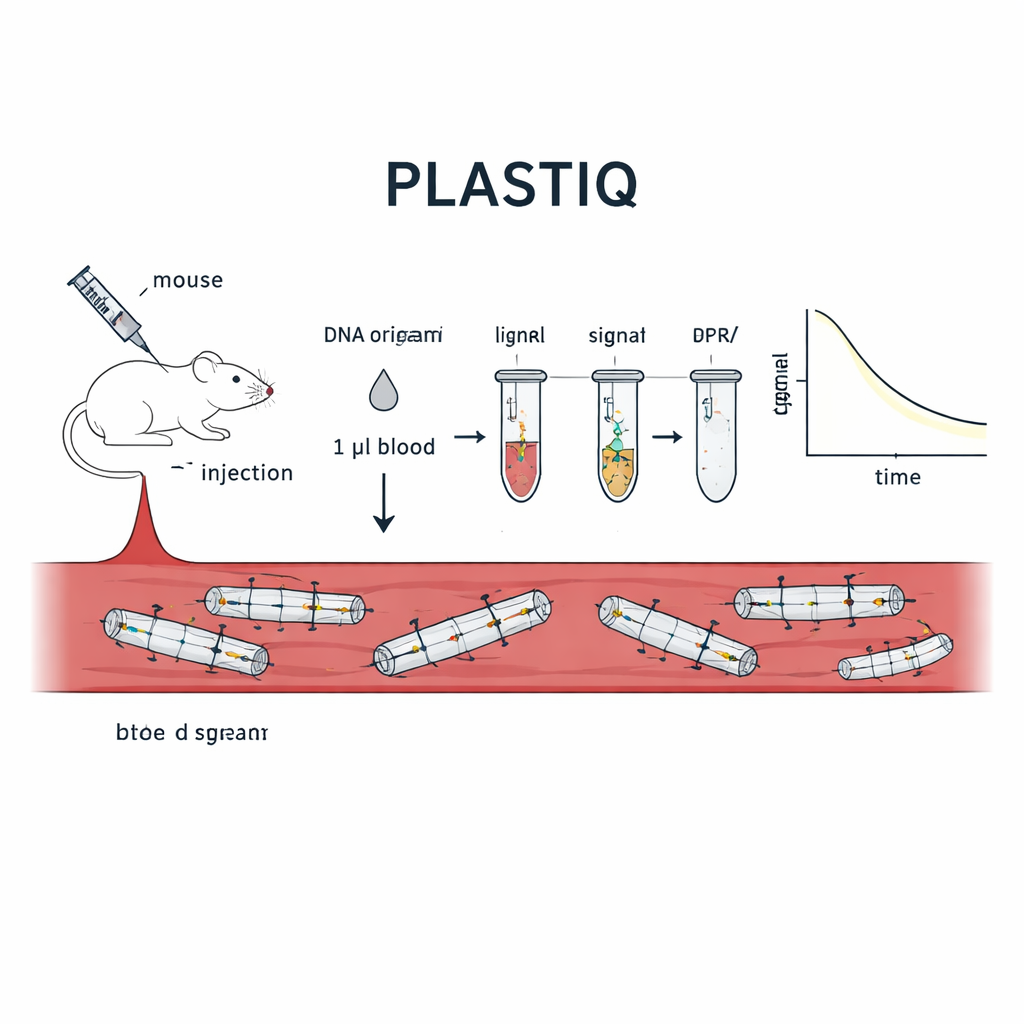
Tillämpning av testet i levande möss
För att bevisa att PLASTIQ verkligen mäter strukturell integritet tillämpade författarna först metoden på enkla stavformade DNA-origamidesigner i provrör. Signaler dök upp endast när stavarna var intakta och försvann efter värmeinducerad utfällning, medan mer traditionella DNA-baserade tester fortfarande registrerade DNA oavsett form. De injicerade sedan dessa stavar i möss via olika vägar—direkt i blodomloppet, i bukhålan, i muskeln och under huden—och tog bara en mikroliter blod vid olika tidpunkter. PLASTIQ visade hur koncentrationen av intakta strukturer steg och sedan sjönk, beroende på injektionsvägen, i linje med allmänna förväntningar från läkemedelsfarmakologi men med mycket finare strukturell detalj. Metoden var känslig ned till 0,01 femtomolar, men krävde minimal mängd blod, vilket möjliggjorde upprepade provtagningar från samma djur över timmar.
Test av skyddande beläggningar och dolda svaga punkter
Många grupper försöker skydda DNA-origami genom att belägga dem med polymerer som PEG, korslänka strängar med ultraviolett ljus eller tillsätta kemiska bindemedel, men det har varit svårt att se hur mycket dessa knep faktiskt hjälper in vivo. Med PLASTIQ visade författarna att PEG-belagda stavar i blodomloppet förblir intakta något längre än nakna stavar men också rensas bort snabbare när de når cirkulationen, och att beläggningen inte hindrar PLASTIQ-enzymerna från att göra sitt jobb. Genom att kombinera PLASTIQ med enkla matematiska modeller extraherade de absorptions- och elimineringshastigheter för olika injektionsvägar och beläggningar, och kunde till och med simulera upprepad doseringsregim. De drev sedan metoden vidare med en dubbel-lagad tunnformad origami, packad tätare på insidan än utsidan. PLASTIQ-mätningarna visade att staplar på den exponerade yttre ytan förlorade integritet snabbare än de som vände mot inre kammaren, vilket direkt bekräftar att begravda helices är skyddade från nedbrytande enzymer i blodet.
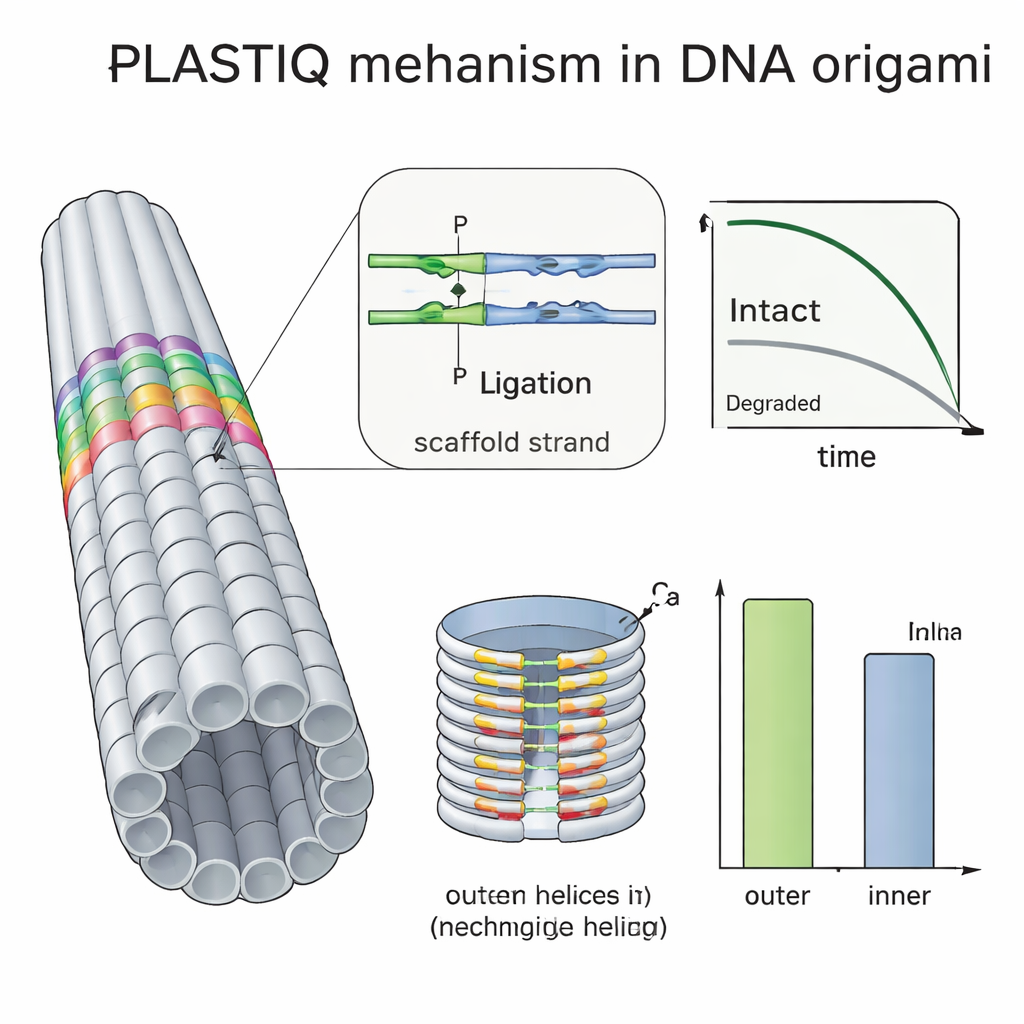
Vad detta betyder för framtida DNA-baserade terapier
För en icke-specialist kan PLASTIQ ses som en strukturell hälsokontroll för nanoskaliga DNA-enheter som färdas genom kroppen. Istället för att bara fråga ”finns det DNA här?” frågar den ”är detta DNA fortfarande vikt till det precisa objekt vi designade?”. Genom att svara på den frågan med hög känslighet från små blodprover ger PLASTIQ läkemedelsutvecklare ett sätt att optimera design, beläggning och dosering av DNA-origami-baserade läkemedel och vacciner. Med tiden kan sådan detaljerad, kvantitativ insikt i hur dessa nanostrukturer beter sig i verkliga biologiska miljöer hjälpa till att förvandla DNA-origami från ett elegant laboratoriekoncept till pålitliga, myndighetsvänliga terapier.
Citering: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Nyckelord: DNA-origami, nanomedicin, läkemedelsleverans, farmakokinetik, nanoteknik